秦凯医生的科普号
- 精选 胰腺癌的外科治疗—谈谈我对局部进展期胰腺癌手术的看法
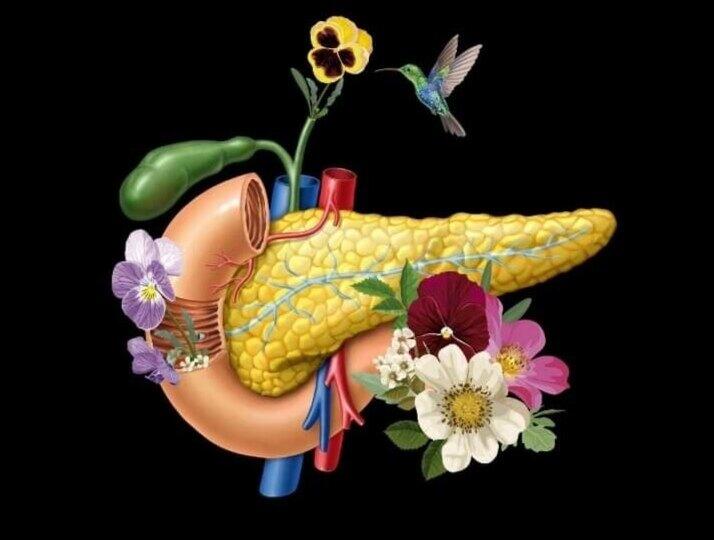
手术是唯一正真可以治疗胰腺癌的手段,胰腺癌切除后的5年生存率可以达到20%~30%,而不切除的只有不到5%,胰腺癌总体预后差,每年基本上发病多少,死亡多少,因此治疗道路上我们胰腺外科医生实在是任重而道
 金佳斌 副主任医师 上海瑞金医院 普外科7584人已读
金佳斌 副主任医师 上海瑞金医院 普外科7584人已读 - 精选 胰腺导管内乳头状黏液性肿瘤(IPMN)
作者:钱剑锋秦凯金佳斌胰腺导管内乳头状黏液性肿瘤(intraductalpapillarymucinousneoplasm,IPMN)为分泌粘液性蛋白的肿瘤,其发自胰腺导管系统,其中起源于胰腺主胰管的为主胰管型IPMN(mainduct-IPMN,MD-IPMN),起源于胰管侧支的为分支胰管型IPMN(branchduct-IPMN,BD-IPMN),两者均涉及的称为混合型IPMN(mixedtypeIPMN,MT-IPMN)。IPMN在男女中比例相近,更常见于老年人群,发病年龄通常大于50岁[1]。就诊患者常有慢性胰腺炎的症状,其他典型症状包括腹痛、体重下降、黄疸等,约25%的患者则无症状,其造成慢性胰腺炎的主要原因是因为IPMN分泌的粘液造成了胰管的排泌不畅,而胰管阻塞后造成了胰腺的炎症。偶发的小BD-IPMN一般不会引起明显症状。根据肿瘤导管上皮细胞的异型程度可以将IPMN分为良性导管内乳头状粘液腺瘤、交界性导管内乳头状粘液性肿瘤或导管内乳头状粘液性肿瘤伴上皮中度不典型增生、非浸润性癌和浸润性导管内乳头状粘液性腺癌4类,浸润性癌即胰腺恶性肿瘤,因此IPMN又通常被认为是胰腺癌的癌前病变,但不同类型的IPMN其恶性程度存在一定差异。2018年欧洲胰腺囊性肿瘤指南中将黄疸、强化附壁结节(≥5mm)、存在实性成分、细胞学阳性、主胰管直径≥10mm列为高危因素,提示恶性。IPMN的鉴别在大的胰腺中心一般不难,增强CT和MR结合就可以做到,必要时需行超声内镜进一步查看胰管内强化附壁结节。主胰管型IPMN的恶变风险较大,约57%-92%[2],一旦诊断高度怀疑建议手术切除。对于主胰管部分受累的IPMN,在考虑到完整切除可疑病灶的同时尽可能保留正常胰腺组织,因此通常先行胰腺部分切除(胰十二指肠切除术或胰体尾切除术),术中应等待冰冻切片结果评估胰腺切缘。若胰腺切缘为高度不典型增生或癌,则需进一步切除甚至行全胰切除术(我们中心此类患者一般首选机器人微创),若切缘为较低级别的不典型增生可视情况不行进一步切除[3]。主胰管弥漫性扩张并不意味着全胰腺受累,是否应行全胰切除术应结合术中切缘结果及患者一般情况,老龄患者可能难以耐受手术风险并可能出现难以控制的高血糖。MT-IPMN的恶性风险与MD-IPMN类似,因此处理原则相似。分支型IPMN在影像学上通常表现为一个囊肿或一簇囊肿样改变,主胰管不扩张。可见于胰腺各部位,但更常见于头部,尤其是钩突和颈部,有研究指出多达64%的患者为多灶性[4]。与主胰管型和混合型IPMN相比,BD-IPMN的生物学行为温和,据报道,手术切除后示高度不典型增生或浸润性癌的约12-30%[5,6]。BD-IPMN的恶性风险和以下特征相关:大小>3cm、附壁结节、实性成分、有分隔或有症状,相关指南也将其列为手术适应症[7,8]。不存在风险因素的患者往往仅需定期随访而无需手术。多灶性BD-IPMN部分可累及整个胰腺,若囊肿集中于胰腺部分,可以选择胰十二指肠切除术或胰体尾切除,而对散在于胰腺各部位的囊肿,建议对存在高危因素的胰腺段行手术切除,而余下囊肿可进一步随访[9]。由于IPMN手术后恶性和复发风险很高,特别是MD-IPMN和MT-IPMN,因此建议术后病人终身随访。低度不典型增生的IPMN复发率为5-10%,而高度不典型增生的复发率则>50%[10]。对于进展为癌的IPMN且无淋巴结转移者,其预后优于PDAC[11]。IPMN还根据组织学分类为胃、肠、胰胆管或嗜酸细胞型,组织学亚型可预测IPMN的生物学行为,胃亚型预后最好,大多数BD-IPMN为胃型,而胰胆亚型预后最差[12]。【参考文献】1.D‘Angelica,M.,etal.,Intraductalpapillarymucinousneoplasmsofthepancreas:ananalysisofclinicopathologicfeaturesandoutcome.AnnSurg,2004.239(3):p.400-8.2.Tanaka,M.,etal.,Internationalconsensusguidelinesformanagementofintraductalpapillarymucinousneoplasmsandmucinouscysticneoplasmsofthepancreas.Pancreatology,2006.6(1-2):p.17-32.3.Pancreas,T.E.S.G.o.C.T.o.t.,Europeanevidence-basedguidelinesonpancreaticcysticneoplasms.Gut,2018.67(5):p.789-804.4.Salvia,R.,etal.,Branch-ductintraductalpapillarymucinousneoplasmsofthepancreas:tooperateornottooperate?Gut,2007.56(8):p.1086-1090.5.Crippa,S.,etal.,Mucin-ProducingNeoplasmsofthePancreas:AnAnalysisofDistinguishingClinicalandEpidemiologicCharacteristics.ClinicalGastroenterologyandHepatology,2010.8(2):p.213-219.e4.6.Pelaez-Luna,M.,etal.,Doconsensusindicationsforresectioninbranchductintraductalpapillarymucinousneoplasmpredictmalignancy?Astudyof147patients.AmJGastroenterol,2007.102(8):p.1759-64.7.Tanaka,M.,etal.,InternationalConsensusGuidelinesforManagementofIntraductalPapillaryMucinousNeoplasmsandMucinousCysticNeoplasmsofthePancreas.Pancreatology,2006.6(1):p.17-32.8.M,T.,etal.,RevisionsofinternationalconsensusFukuokaguidelinesforthemanagementofIPMNofthepancreas.Pancreatology:officialjournaloftheInternationalAssociationofPancreatology(IAP)...[etal.],2017.17(5):p.738-753.9.Rodriguez,J.R.,etal.,Branch-ductintraductalpapillarymucinousneoplasms:observationsin145patientswhounderwentresection.Gastroenterology,2007.133(1):p.72-9;quiz309-10.10.Europeanevidence-basedguidelinesonpancreaticcysticneoplasms.Gut,2018.67(5):p.789-804.11.Salvia,R.,etal.,Main-ductintraductalpapillarymucinousneoplasmsofthepancreas:clinicalpredictorsofmalignancyandlong-termsurvivalfollowingresection.AnnSurg,2004.239(5):p.678-85;discussion685-7.12.Castillo,C.F.d.andN.V.Adsay,IntraductalPapillaryMucinousNeoplasmsofthePancreas.Gastroenterology,2010.139(3):p.708-713.e2.
 金佳斌 副主任医师 上海瑞金医院 普外科9814人已读
金佳斌 副主任医师 上海瑞金医院 普外科9814人已读 - 精选 胰腺囊肿的诊治
钱剑锋秦凯金佳斌胰腺囊性肿瘤(pancreacticcysticneoplasms,PCNs)是以胰腺细胞增生且其分泌物形成潴留囊肿为特征的一类疾病,这类肿瘤多为良性或低度恶性肿瘤,少数存在恶变的风险,其主要包括导管内乳头状黏液性肿瘤(intraductalpapillarymucinousneoplasm,IPMN)、浆液性囊腺瘤(serouscysticneoplasm,SCN)、黏液性囊性肿瘤(mucinouscysticneoplasm,MCN)、实性假乳头状肿瘤(solidpseudopapillaryneoplasm,SPN)等。其发病率随着年龄逐年升高,据报道,40岁以下的PCN患病率为0.5%,40-79岁的患病率为25%,80岁或80岁的患病率则超过37%。随着近年来影像技术的发展以及健康体检的普及,PCNs的发现率日益增多。目前尚缺乏特异性高、敏感性强的肿瘤指标用以区分PCNs亚型或识别有恶性潜能的PCNs。CA19-9的升高常提示肿瘤的恶变倾向,当CA19-9≥37U/ml时可能提示恶性,如侵袭性IPMN。影像学依然是诊断PCNs的主要方式,对于怀疑胰腺占位的患者,我们一般推荐完善胰腺增强CTA及增强MR,必要时联合MRCP检查,通常来说胰腺增强MRI为诊断PCNs的首选检查,但对于肿瘤实质成分、壁结节的检测、鉴别PCNs与慢性胰腺炎相关的假性囊肿、对于某些怀疑恶性需评估血管受累情况时,胰腺增强CT检查也有一定优势,单一的的显像技术并不能完全诊断,诊断往往需要多种影像技术的相辅相成,但显像技术仍有限制,如对一些孤立、直径较小的肿瘤难以区分。此时可以联合超声胃镜检查(endoscopicultrasonography,EUS)提高诊断率,同时借助EUS下的相关操作可以进一步为PCNs的诊断提供依据,如通过细针穿刺(fine-needleaspiration,FNA)可以进行囊液分析并获取细胞学及病理结果。PCNs是否需要治疗一直是关注的重点,根据目前颁布的相关国际指南和我国诊疗经验,通常对以下几种情况建议手术:细胞学检查阳性和/或存在EUS确认存在三个高危特征中的其中两个即实性成分、胰管扩张>5mm和囊肿大小>3cm,另外对有症状的患者建议切除,如黄疸、肿瘤导致的腹痛、反复胰腺炎等。肿瘤大小是否重要一直存在争议,因为研究表明≥3cm的囊肿并不一定预示着恶变倾向。对于<3cm且无高危特征的囊性肿瘤,建议MRI随访1年,然后每2年1次,共5年,对于其后是否可终止随访尚存在争议,可视患者自身情况决定。对于>3cm且无高危特征的囊性肿瘤,可同样进行随访。各指南对PCN的管理逐渐趋于保守,随访或者手术治疗的选择主要取源于人们对恶性风险的评估,但至今,人们对PCNs的自然病程和预后尚不完全清除,PCNs类型的确诊还是要依靠术后病理,除此之外,是否选择手术还需要考虑几个因素:患者整体健康情况、有无合并症和患者的预期寿命,由于PCNs的发病率随年龄升高而升高,部分患者发现者多为高龄,合并基础疾病,能否承担手术风险需要多方面权衡。目前,手术仍是治疗PCNs的主要方式。由于该类肿瘤往往与周围组织无粘连,肿瘤界限清楚,少有血管侵犯,微创手术是首选。机器人操作灵活度高且在精细吻合、对细小血管缝合止血上存在优势,而这恰恰是胰腺手术的难点所在。目前胰腺各常用术式均可通过机器人进行。在保留胰腺实质的手术中,机器人的优势更加突出。根据胰腺肿瘤所在位置的不同,传统的标准胰腺切除术可分为胰十二指肠切除术和胰体尾切除术,大量研究已证明其均可通过机器人实现,且手术结果与传统开腹手术无明显差异。对于PCNs,除了保证手术切除率,另一个治疗目标是尽可能保留正常的胰腺组织和周围脏器,从而让患者尤其是年轻患者获益,改善长期生活质量。对此常用的术式包括保脾胰体尾切除术、胰腺剜除术、胰中段切除术、保留十二指肠的胰头切除术等,越来越多的病例提示了机器人系统在该类手术中的优势。
秦凯 主治医师 上海瑞金医院 普外科3004人已读 - 精选 侵犯血管的复杂胰腺神经内分泌肿瘤,如何手术处理
复杂的胰腺神经内分泌肿瘤G2,位于胰颈部,一发现就侵犯门静脉周围侧枝形成,手术好比在血管丛林里作战,出血会让你疯掉。 第一次看到我也怂了,不敢开刀。追问病史曾经索坦治疗一度缩瘤33%,可惜错过手术时机,这次我和病人一起决定,再试一次索坦,果然有效,但是机会转瞬即逝,看这CT对比,一个月不到,肿瘤血供即将恢复。 马上当机立断手术,原本的全胰腺切除修正为保留头尾脾脏的胰腺中段大部分切除联合门静脉切除重建(根据术前的定位定性影像精准切除),术后血糖正常!更幸运的是,清扫淋巴结21枚只有一枚转移,与术前双显扫描也符合。抓住肿瘤的生物学行为特点,及时的手术干预,一定能获得良好的效果,祝出院后恢复顺利!
 金佳斌 副主任医师 上海瑞金医院 普外科2497人已读
金佳斌 副主任医师 上海瑞金医院 普外科2497人已读 - 图文文章 侵犯动脉的胰腺神经内分泌肿瘤,如何治疗
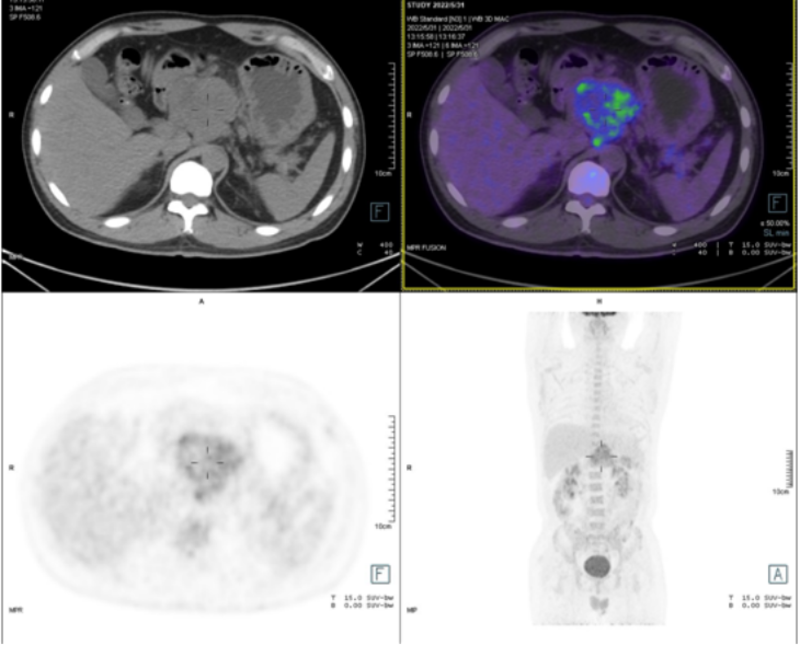
(姜毓,金佳斌,瑞金pNETMDT团队)患者青年男性,2022年5月20日当地医院CT提示胰头部肿大,局部可见团块低密度灶,大小约6551mm,病灶局部包绕、推移邻近腹腔干、脾动脉及肝总动脉,脾动脉局部稍毛糙变窄。穿刺病理报告提示胰腺神经内分泌肿瘤G2(ki6715%)。生长抑素受体显像提示胰腺头颈部团块,生长抑素受体表达不均匀增高。2022年6月至我院胰腺神经内分泌肿瘤专病门诊就诊,诊断无功能胰腺神经内分泌肿瘤(NF-pNET),分级G2(ki6715%),双显像提示NETPET评分P2可能,分期T4N0M0-III期。这是一例典型的局部进展期pNET(可参考我之前写的《局部进展期胰腺神经内分泌肿瘤的外科治疗——瑞金经验》,临床上并不少见,根治性手术切除是最重要的治疗手段。对于这类患者一般有两种处理方式:直接手术or转化治疗后再手术。孰优孰劣并无定论。本例患者如选择直接手术,技术上可行,但因为肿瘤侵犯范围较大,腹腔干、肝动脉、肝十二指肠韧带侵犯,肿瘤浸润胰腺范围也很大,很有可能需行全胰腺切除,手术创伤巨大,对患者生活质量及后续可能需要的治疗(如TAE等介入治疗)影响较大,因此经过MDT讨论后决定先行新辅助治疗后再手术。胰腺神经内分泌肿瘤新辅助治疗目前也有很多探索,比较常用的方案包括抗血管生成靶向药、化疗、PRRT等。综合本例患者的病理、影像等资料,MDT讨论后决定行卡培他滨+替莫唑胺(CapTem)的经典口服化疗方案。经过4个疗程的新辅助化疗,患者的肿瘤显著缩小,达到预期效果,MDT决定手术。2022年10月入院评估,CT提示胰腺肿瘤较前显著缩小(65cm缩小至3.53.5cm)。虽然肿瘤仍然侵犯腹腔干、肝动脉等大血管,但惊喜的是胰腺颈部似乎是正常的,原定的全胰切除方案修正为胰体尾联合脾脏切除+肝动脉及腹腔干外鞘剥离。为何一定要保留腹腔干?如果联合腹腔干切除,其实手术技术上更容易,风险也相对更可控。但切除腹腔干会对患者后续可能需要的治疗(如肝脏局部介入治疗)产生影响,因此在技术可行的前提下我们会尽最大努力保留腹腔干动脉。由于保留了胰头和消化道的连续性,患者术后的生活质量会好非常多!2022年10月20日患者成功进行了胰体尾联合脾脏切除+胆囊切除。术中通过鞘内解剖完整剥离了肝动脉及腹腔干外鞘,因肿瘤侵犯严重,通过部分腹腔干重建成功保留了腹腔干-肝总动脉,为了保护血管,术中我们重建了肝动脉及腹腔干外鞘。术后病理神经内分泌瘤(NET):G2,肿瘤大小:4.0×3.5×3.0cm;SSTR2A(+),Ki67(约3%+),无淋巴结转移,腹腔干外鞘及肝总动脉外鞘见肿瘤累及(幸好做了剥离)。术后患者恢复顺利,无胰瘘等并发症,术后10天拔除引流管出院。因为本例患者属于局部晚期,可以看到我们的治疗策略和局部晚期的胰腺癌类似,但因为动脉外鞘有肿瘤累及,因此随访策略还是采取比较积极的方案,术后第一年每三个月随访一次。辅助治疗尽管目前仍有争议,我们还是推荐患者进行为期12个月的SSA辅助治疗方案。
 金佳斌 副主任医师 上海瑞金医院 普外科2213人已读
金佳斌 副主任医师 上海瑞金医院 普外科2213人已读 - 已行胆肠/胃肠转流后的胰腺手术怎么做
很多胰头癌或壶腹癌,初次手术探查后发现肿瘤不可切除,不管是技术原因还是肿瘤原因,手术做不下去,此时除了做活检(建议尽量做),都会为了病人好做胆肠和胃肠转流,原因是患者后续排黄疸,吃饭不至于梗阻,殊不知,病人都期望可以手术切除肿瘤,初次手术无果后,也会积极寻求办法:化疗,放化疗结合等等。几个疗程下来,奇迹发生了,肿瘤缩小,转移消失,血管间隙显露。。。判定,可切除。那么问题来了,做了一系列转流后,再做胰十二指肠切除术能做吗,答案是能;好做吗,答案是不好做。第一例患者:女性,60岁,2020年9月腹痛外院检查发现胆总管中下段占位,于外院手术,术中评估手术困难,行活检+胆囊切除+胆肠转流+胃肠转流,术后3月开始放疗,同步单药卡培他滨化疗,3月后改为吉西他滨+卡培他滨,后又换顺铂+吉西他滨,2022年2月开始口服卡培他滨+索凡替尼,5月开始PD1+白蛋白紫杉醇+奥沙利铂…2022年7月入住我科评估手术。评估是个可切除的胰头壶腹癌,于是完善术前准备后原切口开腹手术。虽然做过转流,手术困难,但是经过仔细解剖发现,原来的肠袢尚健康,合理的离断肠袢后,原有的肠袢用于行胰肠吻合恰好,病人术后11天出院,病理示胰头癌,淋巴结都阴性。第二例患者,男性,65岁,2021年2月因黄疸至当地医院影像学发现胰头占位,当地手术,术中应该也是困难进行不下去而行活检+胆囊切除+胆肠转流+胃肠转流,同时还加做肠肠Braun吻合,术后2周开始AG方案化疗+腹腔热灌注,术后3月开始放疗28次,至2021年9月休息,2022年3月因肿瘤指标升高行Folfirinox化疗4个疗程,至6月份更改方案为白蛋白紫杉醇+PD1+仑伐替尼,7月至我院评估。评估下来没有转移,血管还好,所以也没什么理由拒绝手术,然而手术异常困难,术中按照常规解剖胰腺下缘,居然找不到肠系膜上静脉!!!,后来通过先找到门静脉,断胰腺颈部,才逐渐显露肠系膜上静脉,表面粘连非常致密,提示原来解剖过。这例患者由于胆肠袢很短,胃肠转流后又加做肠肠Braun吻合,再次重建碰到很大难题,如果照搬第一例患者的吻合,会出现食物反流到胆胰袢后续反复发作的胆管炎甚至胰腺炎,于是我们将食物袢结扎阻断,另行肠肠吻合。最后病理提示胰腺癌化疗后改变,淋巴结2枚转移。由于此类手术往往信息不对等,最后的手术团队并不清楚前一次的手术团队真正做了些什么,第一例手术,粘连松解大概花了1小时,而第二例则花了3小时,手术的粘连往往取决于上次手术进行的程度,如果仅作活检和转流,往往你粘连不会太困难;如果大作特做,奔着切除的目的而去,则困难度++++以上两例患者的共同点是第一次手术都做了转流,术后都做了一系列辅助治疗,放化疗搞了个遍(居然也能有效!),这个其实反面提示肿瘤预后可,值得进一步治疗(也就是手术),最后,如果你问我这样的手术愿不愿意做,我不太愿意,高风险,吃力不讨好;该不该做,我说该做,手术时机到了,错过对这个病人来说可能就是错过一生。
 金佳斌 副主任医师 上海瑞金医院 普外科920人已读
金佳斌 副主任医师 上海瑞金医院 普外科920人已读 - 图文文章 局部晚期的胰腺癌,该怎么治疗
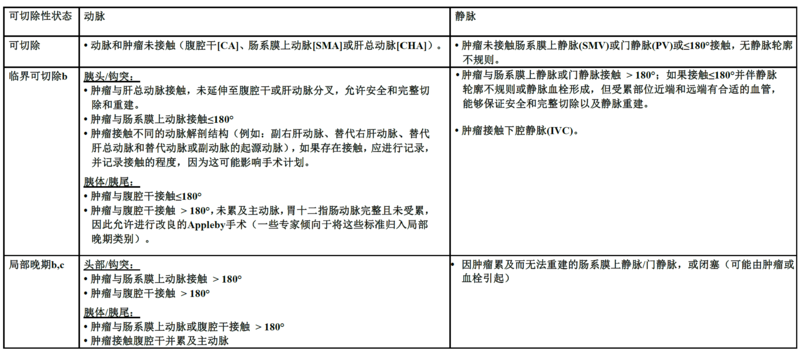
胰腺癌侵犯大动脉又叫局部进展期,大动脉指的是腹腔干(CA),肠系膜上动脉(SMA),肝总动脉(CHA)。局部进展期,分为可切除和不可切除,不可切除的只能化疗或放化疗;可切除的当前普遍也是建议先化疗的,
 金佳斌 副主任医师 上海瑞金医院 普外科4239人已读
金佳斌 副主任医师 上海瑞金医院 普外科4239人已读 - 侵犯腹腔干或肝总动脉的胰颈体癌手术方式选择
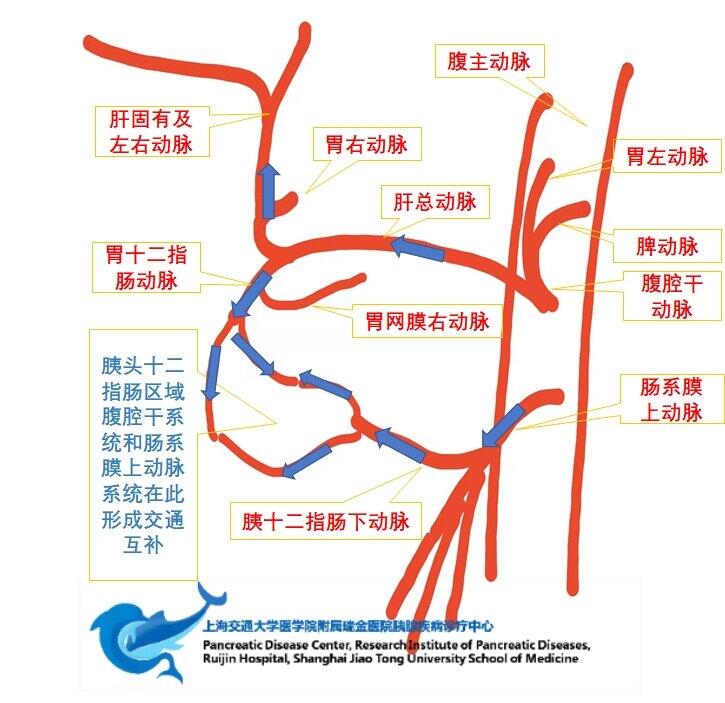
箭头表示血流信号,正常情况下胰头接受腹腔干和肠系膜上动脉两个系统的供血,所以血供极其丰富(手术也极容易出血,术后也是),当联合腹腔干的胰体尾癌切除,如果胃十二指肠动脉未受侵犯,则可以切断并切除肝总动脉以及腹腔干,同时胃左动脉和脾动脉也会一并切除,此时肝脏的血供全部靠肠系膜上动脉供应,胃的血供全部靠胃网膜右动脉供应(如胃右动脉在,也部分供应,但流量很小),该手术称为Appleby术,即胰体尾联合腹腔干切除。所以我们在读片的时候,首先看腹腔干,如果侵犯了,再看肠系膜上动脉,如果肠系膜上动脉侵犯了,这个手术就到天花板了!在成熟的胰腺中心,开展该术式,并不增加并发症和死亡率,但是对手术的评估和术后管理提出了更高的要求。
 金佳斌 副主任医师 上海瑞金医院 普外科3102人已读
金佳斌 副主任医师 上海瑞金医院 普外科3102人已读 - 图文文章 胰腺实性假乳头状肿瘤的治疗
胰腺实性假乳头肿瘤(Solid pseudopapillary neoplasm,SPN)是一种罕见的胰腺肿瘤,约占所有胰腺外分泌肿瘤的1-2%,往往呈低度恶性,好发于年轻女性。SPN最早由Frantz于1959年报道,故也称为Frantz肿瘤,后于1996年由WHO组织统一命名为实性假乳头肿瘤,其可以发生于胰腺的各个部位,包括胰腺头部,体部以及尾部。 胰腺实性假乳头肿瘤患者常无明显症状,多数为体检或做其他脏器检查时发现,少数肿瘤居大的患者会有一定压迫症状(包括腹胀,腹痛,进食后饱胀感等),极少数患者有皮肤巩膜黄染等阻黄表现。绝大部分的患者血肿瘤指标无明显异常。腹部增强CT或者胰腺增强MRI常具有典型的表现,肿瘤常呈囊实性,包膜完整部分钙化,部分肿瘤囊内伴有出血,具体影像学表现视肿瘤内囊性、实性及出血成分比例而有所不同。近年来,超声内镜的发展也对胰腺实性假乳头状肿瘤的术前诊断有很大帮助。 胰腺实性假乳头肿瘤目前最有效的治疗方法是手术切除,患者手术后预后较好,甚至对于部分伴有转移或者存在血管侵犯的患者,仍推荐手术治疗。由于大部分的患者为年轻女性,往往对于微创手术的需求较高。对于胰腺体尾部的SPN,腹腔镜已有所开展,但对于胰头部的SPN,微创手术仍有一定挑战,而随着达芬奇机器人系统在胰腺外科领域的应用,其治疗胰头部SPN成为可能。目前瑞金胰腺中心已开展机器人手术治疗胰腺实性假乳头肿瘤200余例,处于国际领先水平。图1为一例胰腺颈部实性假乳头状肿瘤病例行保留功能的胰腺切除术图2为一例巨大胰腺实性假乳头肿瘤病例
秦凯 主治医师 上海瑞金医院 普外科2002人已读






