孔连宝医生的科普号
- 精选 实体肿瘤立体定向微创治疗
孔连宝 教授、博导、副院长南京医科大学第一附属医院(江苏省人民医院)南京医科大学第三附属医院(南京医科大学附属逸夫医院)(一)CT帮助下的智能立体定向微创射频手术智能立体定向手术系统是国人发明研究出的国际先进科研项目,主要用来脑部功能外科手术治疗帕金森综合征和癫痫等。并用来针对肝脏和其它器官的实体肿瘤的微创射频治疗,不需要开腹手术。该手术结合计算机软件处理系统,可三维显示入路组织结构,并与机械臂有机结合,手术微创,简单直观,易行可靠。(二)射频消融手术的特点射频消融的范围要超过肿瘤边缘1厘米,才能达到肿瘤完全坏死的目地。一次电极针的射频消融的范围是直径5厘米,3厘米以下的肝脏肿瘤可以达到一次电极插入后射频消融完全覆盖。而对超过3厘米以上的肝脏肿瘤就需要调整电极针作甚少6次的射频消融,而且残瘤率和复发率都明显的升高。所以最适合的病人肝脏肿瘤要小于3厘米,肝脏肿瘤的数目在3个以下。如果肝脏肿瘤大小超过5厘米,还是首先考虑外科手术切除为佳。(三)如何实施射频消融治疗?(1)麻醉 可在静脉麻醉或者联合局麻下进行。(2)引导 CT帮助下的智能立体定向微创射频技术进行。(3)消融途径 不需开腹,经皮穿刺。(4)消融范围 穿刺置入射频电极后,按射频发射仪说明书进行操作完成消融过程,消融范围一定要完全覆盖肿瘤范围,并超出其边界1厘米。(四)术后复查一般不适用超声观察,因为超声很难准确判断凝固坏死的范围。应采用一个月后用增强CT扫描来判定治疗效果,扫描显示凝固坏死的区域密度降低,6个月后会进一步缩小,如果发现治疗区域周围有一厚而不规则的增强的晕环,说明治疗不足还需要再次治疗。一般术后1个月作一次增强CT检查,如果发现有肿瘤复发可再次治疗。同时也能抽血中肿瘤标记物动态观察有无升高的情况,指标升高也显示有肿瘤复发。
孔连宝 主任医师 江苏省人民医院 肝胆中心1742人已读 - 引用 对于胆囊结石的几点个人建议,供病友参考(修订版)
现在肝胆外科医生看门诊遇到最多的问题之一就是能否做“保胆取石”手术。保胆手术的愿望非常好,是最容易让病人接受的观念,因为既能“成功保胆”又能清除结石,似乎是最接近医学以人为本的目的。但不是任何胆结石或胆囊息肉都可以做保胆手术的,现在由于网络信息发达,病人就医前都会在网上自己查询信息,加上有些医院和医生的大力推广和宣传,病人看病前就已经有了先入为主的观点,让医生看病时百口难辩,你说不能保胆病人还可能会误认为医生本身不能做这个手术。在这里,我对有关胆囊结石的治疗谈谈我个人的观点,供病友们参考!以下有10条,如果耐心不够,可以参考关于是否有胆囊的好处大小不等式:正常胆囊>无胆囊>功能不良的病变胆囊,也就是,没有胆囊(胆囊切除)要比保留一个有病的功能不良的胆囊更好!1、保胆手术是新手术吗保胆手术其实并不是一个新手术,对于胆囊结石的治疗,1867年最早创立的手术就是切开胆囊取石,病人症状得到缓解,但是并不代表治愈了胆结石,十有八九病人胆囊结石复发,那时候的医生也就无能为力了,直到1882年德国的外科医生Langenbuch才第一个完成了胆囊切除手术,直至现在胆囊切除术仍然是治疗胆囊结石及其它胆囊疾病的最主要的方法。到1987年腹腔镜胆囊切除术的成功改变了胆囊切除手术的历史,现在腹腔镜胆囊切除术已经广为开展,在我国县一级医疗中心就能施行。在这100多年期间也有不少老前辈探索过保胆取石的做法,但仍然是面对结石复发的难题无法解决,所以胆囊切除术仍然是胆囊结石的标准治疗措施。2、胆囊结石形成的原因胆囊结石形成的原因非常复杂,各个病人不能一概而论,在这里我也不多说了,因为说也无法说清,反正不是把石头拿了就能好的事。很简单的想想就可以明白,大家出生的时候都是没有胆结石的,好好的胆囊以后才长出来的结石。而长了结石之后,胆囊粘膜多少都会有炎症改变,或结石的残渣沉积,就算把结石拿得干干净净,复发结石的比例肯定还是很很很高的。原来没有结石的胆囊都能长出结石,取出结石后又没明确病人的长结石的原因而控制结石的复发,所以结石的复发几乎是不可避免,并不是说把结石全部拿干净就行了。不否认肝胆外科医生利用现在的技术手段可以把结石拿干净,但是绝不是把结石生长的机制拿干净了,所以再复发也就可以理解了!(有点绕口,不知道你能明白否!)3、胆囊结石的危害胆囊结石最常见的害处就是经常引起右上腹部的不舒服或疼痛、胆囊炎发作,严重者可能导致胆囊化脓,坏死,穿孔,弥漫性腹膜炎,长期的胆囊结石还有一定比例的致胆囊癌,胆囊癌的恶性程度非常高,结果很差,在临床上还是可以经常见到由于胆囊结石没有治疗最终成为胆囊癌的病人。在这里我更要强调的就是没有症状的胆囊结石。细小的胆囊结石还可能从胆囊管进入胆总管内继发胆总管结石,还可能继发急性胰腺炎,严重的话也是非常痛苦的病,甚至危及生命。4、胆囊结石如何选择手术方法之我见胆囊切除术:胆囊结石有过炎症发作或是泥沙样结石的,建议行胆囊切除,因为保胆取石的复发率太高,甚至可达到80%以上,最后还是要行胆囊切除的,只不过是本可一次手术解决的问题分为两次手术而已。保胆取石手术:对于孤立性或数量少的的无症状性结石,而且胆囊功能良好,超声检查和手术中所见胆囊外观正常的,本人保胆意愿强烈并且有一颗准备结石复发的心(指结石复发的心理准备)是可以施行保胆取石手术,但是手术后还是要坚持复查。现在还缺乏可靠的循证医学证据来证明胆囊结石可以做保胆手术,只是又掀起一个研究的阶段,有些医生迎合病人的心态有些过高称赞了保胆手术的效果。病人本身并不懂这些,一厢情愿认为既保住了胆囊,又拿掉了石头,以为就治好了胆结石,我个人认为需要慎重。 建议只是在以上情况下,病人个人愿望坚持要保胆的情况下,医生可以考虑,但必须与病人交代复发的可能性很高,以后可能还需要胆囊切除。从医生的角度,我觉得还是建议胆囊切除为妥。有人说结石还小不需要手术,其实胆囊结石如果大超过10mm了反而相对比较“安全“,一般只是引起单纯的胆囊炎,而小于10mm的结石最容易引起胆囊管嵌顿,或排出到胆总管引起胆管炎甚至急性胰腺炎,相对来讲害处更大,更需要尽快处理。还要强调的是无症状的胆囊结石的问题:很多医生包括现在的教科书都认为无症状的胆囊结石可以不手术,但不手术必须严密观察,而不是置之不理。其实如果胆囊结石有症状表现的,病人可能总免不了经常看医生或及时做胆囊切除手术了,反而解决了问题,相反,正因为无症状所以病人不去关注,往往结石存在时间很长,10年、20年或30年,等到有症状时再查发现成胆囊癌了,而且往往就是晚期,这就会彻底改变整个人生过程,我在临床上见得太多例子了,实在可惜。我的观点是如果你是体检非常及时和认真的人,至少每半年能做一次肝胆超声检查,可以选择继续严密观察,一旦发现变化及时手术,如果做不到这点最好尽早行胆囊切除吧,以绝后患!5、胆囊息肉胆囊息肉与结石不同,一般胆囊息肉并不伴有胆囊炎症,胆囊功能是正常的,如果胆囊息肉是单发的,或多发数量较少局限于胆囊的某一局部的,可以施行保胆切除息肉,但是如果息肉散发胆囊多处,或者处于胆囊颈管处的,可能保胆并不容易,需要具体情况看,因为胆囊息肉不能单纯把息肉摘除了事,而是应该连息肉的根部一起切除才行,多个散发的息肉不可能在胆囊各处挖除。而胆囊颈管细小,切除之后就难以修复,也是需要胆囊切除的。胆囊息肉切除,如果息肉体积大或可疑癌变应该术中活检,如果有恶变可能,及时加行胆囊切除术或胆囊癌根治术。6、胆囊结石能否药物治疗很多病人问这个问题,但是很不幸,胆囊结石一旦形成,至少目前还没有药物能够将结石缩小或消除,如果有医生说能,那只能是这个医生对胆囊结石的形成和结构还不太清楚或是个单纯卖药的“医生”(注意:这里的医生是带引号的,其实可能根本不是医生),当然,如果几年,至少几十年或百年后是否有这种可能,这是我们医生和病人共同的愿望。例外的是有些早期少量的泥沙样结石或胆固醇沉积应用利胆药或熊去氧胆酸有可能减少或暂时性消除,但长期效果不确定,如果存在胆囊炎还是建议手术为好。7、胆囊结石能否碎石排石还有些病人问碎石治疗是否可行,胆囊结石与输尿管或肾的泌尿系结石不同,肾结石或输尿管结石碎了可以随尿液排出。胆囊结石如果碎石排石,则是排到胆总管里,胆总管结石比胆囊结石的危害更大,手术也更复杂,也就是说,把胆囊结石碎石排入胆总管似乎是把小病变大病的做法。因为结石如果堵塞了胆总管,那就可能会造成黄疸,形成胆管炎、胰腺炎,危害很大,甚至是要命的病了,所以建议病家有胆结石千万别听有些“医生”忽悠能用药排石或什么新方法碎胆石(我觉得真的医生一般都不会这么说的,这么做的基本都是假医生骗钱的,比如通过百度竞价排名靠前的PT系医院,当然也有真的“医生”是过分相信自己的药效的)。8、开腹手术还是腹腔镜手术毫无疑问现在90%以上都是腹腔镜胆囊切除,但是腹腔镜手术除了与病人病情和解剖结构有关外,也与医生的技巧还是有关系的,自开展腹腔镜胆囊切除术以来,发生胆道损伤的比例大概是1~5‰!9、胆囊切除后有什么危害胆囊做为一个人体器官肯定是有它存在的价值和功能的,是储存、浓缩胆汁,以备在不进食的时候将肝脏排泌的胆汁储存备用,在进食时再一次性排出来以利消化食物。这也明白了为什么做胆囊超声时需要早上空腹,让胆囊充盈起来才好观察,进食后胆囊内胆汁排出去了就不好看清楚了。所以在胆囊切除后就失去了胆囊的储存胆汁的功能,最大的影响可能就是胆囊切除后不能大吃大喝,以免胆汁排泄不够而致消化不良。如果这就是你想保胆的原因,那请你想想你现在有这个含有结石的胆囊是不是就能大吃大喝呢!10、保胆的理由(1)胆囊结构和功能良好;(2)病变能完全去除:息肉切除或结石能完全清除;(3)如果是结石自己愿意承受再次手术的可能风险。这三条如果齐全,你可以试试,当然还要你的医生愿意做这种手术!以上仅供病友们参考,如果同行专家有不同观点或更好建议,希望讨论或批评指正,一切为了病友的利益!本文系冷建军医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载。
冷建军 主任医师 北京大学首钢医院 肝胆胰外科4.2万人已读 - 医学科普 从ERAS谈我对患者的几点建议
从ERAS谈我对病人的几点建议 首先,我来简单介绍一下ERAS,所谓ERAS,即加速康复外科,通过减轻术后应激反应、合理管理疼痛、早期回复饮食和早期活动等措施来减少术后并发症,缩短术后住院时间,减少医疗费用,这样就达成了病人和医生双赢的局面,因此ERAS不仅与义务工作者相关,也与病人密切相关,下面我根据ERAS的一些观点谈一些与病人相关的几点建议: 一、关于术后饮食 传统观念和老百姓一般认为手术以后直至肛门排气(即放屁)方可饮食,但询证医学证据表明,术后早期拔出胃管、早期进食及营养支持治疗都能促进患者胃肠功能恢复及全身营养状态提升。因此建议拔出胃管后当天开始进流质食物,逐渐由半流质、软食过渡到正常饮食。一般的,肝脏病人术后是不会放置胃管的,那么对这类病人,我的建议是术后可以少量饮水,因为胃肠道本身也会分泌一定的液体,每次饮一至两小口,待肛门排气后有流质半流质逐步过渡到正常饮食。此外,对于任何手术的病人,如果自己没有饮食禁忌,那么术后的饮食也是没有忌口的,正常饮食即可,尤其对于营养相对较差的,我们还建议需是当加强营养,肉类,虾类,鱼类以及牛奶.蒸鸡蛋等均是我们推荐的食物,对于胆道系统的手术,尤其是胆囊胆管结石术后放置T管的,因为引流的胆汁中含盐量较多,我们建议这类患者饮食可适当偏咸,以补充体内的盐分。 二、关于术后活动 有病人觉得做了手术“元气大伤”,尤其在我们医院和我们科,往往病人做的手术都是一些大手术,这就更增加了他们术后在床上的时间,延迟了下床活动的时机。事实上,长期卧床会增加肺部感染、栓塞的并发症发生率。早期活动促进肌肉骨骼等多系统功能恢复,可以预防肺部感染、褥疮和深静脉血栓形成,同时促进胃肠功能恢复。因此在这里我强烈建议我们的病人在术后在医生和护士的指导下早期进行下床活动,合理规划有效、安全的早期活动。当然,手术毕竟是对身体的床上,术后的活动也应该因人而异、循序渐进,对于年纪较大和身体较弱的,可以适当延迟下床活动的时机,从床上的伸腿、侧身等活动过渡到在床边坐起及靠近床边的站立,最后逐步过渡到一般性活动;而对于年轻人和身体素质较好的人,我们也不建议一开始就进行超量的活动,曾经就有一个病人因为术后过于“自信”,术后第二天就在走廊走了好几个来回,结果搞得自己心慌头晕。因此我建议手术以后既要早下床、早活动,同时注意量力而行、循序渐进。 三、关于止痛药的使用 关于止痛药,不少人谈之色变,认为用多了会上瘾,或者认为完全没有必要使用。实际上,术后良好的镇痛可以提高患者生命质量,缓解紧张和焦虑,且提高早期禁食、早期活动等依从性,加快机体机能恢复,相反,术后镇痛不足反而于患者的回复不利。因此,我的建议是患者术后若有明显的疼痛就要及时告知我们的医生,以便我们有目的、有需要的应用镇痛药物。
孔连宝 主任医师 江苏省人民医院 肝胆中心6108人已读 - 典型病例 急性肝功能衰竭肝移植术后出现肝昏迷消化道出血抢救成功
患者,女性,52岁,因急性肝衰而入院,总胆红素最高达600多,人工肝做了六次,凝血功能差,肝移植术后恢复慢,出现免疫抑制药毒性症状,肝性脑病、病毒感染、反复上消化道出血、大量腹水、腹腔感染等并发症,经多学科(ICU、消化内镜、介入科、感染科等)协作,抢救成功!恢复出院。获省人民医院年度危重病人重大抢救奖。
 孔连宝 主任医师 江苏省人民医院 肝胆中心3008人已读
孔连宝 主任医师 江苏省人民医院 肝胆中心3008人已读 - 学术前沿 微波消融在肝脏外科的拓展应用
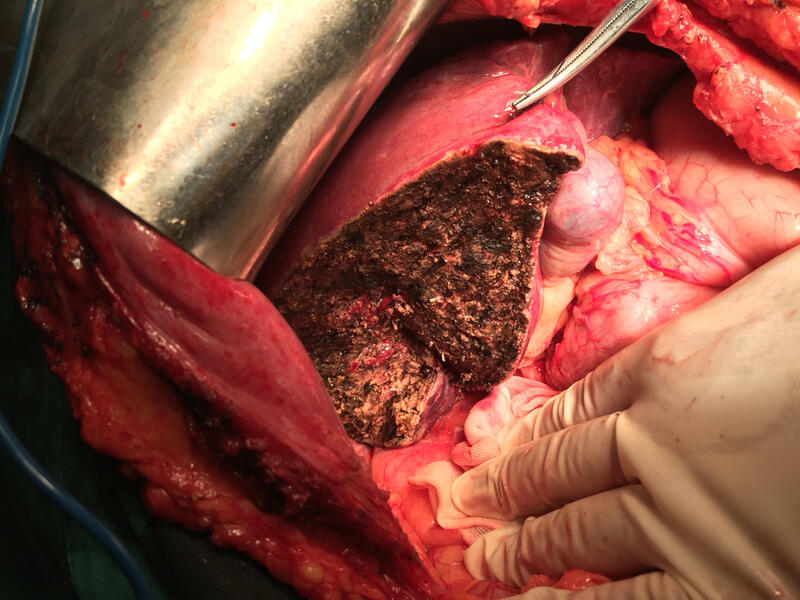
1:肝脏表面肿瘤可以在腹腔镜下消融达到根治;2:肝切除创面止血,最大限度保留正常肝组织,减少术后并发症的发生;3:肝脏肿瘤切除后创面消融,减少肿瘤复发;4:巨大肝肿瘤切除时,结合微波消触可减少术中出血和肝门阻断时间,有利术后恢复。近年来开展此项新技术去年获江苏省卫计委新技术引进二等奖。
 孔连宝 主任医师 江苏省人民医院 肝胆中心1133人已读
孔连宝 主任医师 江苏省人民医院 肝胆中心1133人已读 - 学术前沿 锌原卟啉对肝癌细胞株HepG2顺铂化疗敏感性的影响
血氧红素酶-1(HO-1),又称热休克蛋白32,是血红素分解的起始酶和限速酶,具有抑制各种细胞凋亡、抗炎及抗氧化应激[1-3]等重要生物学作用。本研究应用HO-1特异性抑制剂锌原卟啉(ZnPP)联合顺铂(CDDP)干预人肝癌HepG2细胞,探讨ZnPP抑制HO-1表达对肝癌细胞CDDP化疗敏感性的影响及其可能的机制。一、材料与方法1.材料:CDDP和ZnPP购自sigma公司;HO-1和内参照β-actin引物由invitrogen合成;Annexin V-FITC/PI凋亡检测试剂盒购自Biouniquer公司;RT-PCR试剂盒购自Toyobo公司;HO-1单克隆抗体购自北京博奥森公司。2.细胞培养:采用人肝癌HepG2细胞株为实验对象,进行常规培养。3. MTT法检测细胞生长抑制率:以每孔6×103个细胞接种于96孔板,细胞贴壁后加药。ZnPP终浓度为1、10、20、50和100μmol/L;CDDP终浓度为1、2.5、5、10和20μg/ml;联合用药组先加ZnPP(终浓度20μmol/L)1h后再加上述CDDP各浓度。另设不加药物的对照组,每个剂量设七个复孔。48h或72h后加MTT(5mg/ml)20μl/孔,孵育4h后弃去上清,每孔加DMSO 150μl,于490nm波长测定A值,计算细胞生长抑制率。抑制率(%)=(1-实验组A 值/对照组A 值)×100%4.流式细胞术(FCM)检测细胞凋亡率:以每孔1.2×105个细胞接种于六孔板内,设不加药对照组、ZnPP(20μmol/L)组、CDDP(5μg/ml)组和联合用药组(ZnPP 20μmol/L+CDDP5μg/ml)。加药培养48h后收集细胞,按照Annexin V-FITC/PI凋亡检测试剂盒说明书操作。5. RT-PCR检测细胞HO-1mRNA表达:实验分组同上,加药培养24h后提取总RNA,取等量RNA逆转录为cDNA。HO-1上游引物5′-GCTCTTTGAGGAGTTGCAGG-3′,下游引物5′-GTGTAAGGACCCATCGGAGA-3′,产物长度196bp;β-actin上游引物5′-TTGCGTTACACCCTTTC TT-3′,下游引物5′-TGT CACCTTCACCGTTCC-3′,产物长度150bp。基因扩增的反应条件:95℃预变性10min;94℃1min ,59℃40s ,72℃1min ,循环27次,72℃延伸10min。产物在1.5%的琼脂糖上电泳,利用Syngene系统进行图像分析。6.Western blot检测细胞HO-1蛋白表达:实验分组同上,加药24h后收集细胞提取蛋白,通过Western blot分析HO-1蛋白表达变化。将结果扫描入计算机分析吸光度。7.细胞内活性氧检测:实验分组同上,加药后继续培养24 h,胰酶消化离心收集细胞,按活性氧检测试剂盒说明书操作。8.统计学方法:所有实验数据以均值±标准差(x(-)±s)表示,应用方差分析进行样本间的两两比较,P <0.05有统计学意义。二.结果1.各组细胞抑制率比较:不同浓度的CDDP均能抑制HepG2细胞增殖,具有剂量依赖性,随着浓度增加抑制率得到增强。ZnPP(20μmol/L)联合不同浓度CDDP,对肝癌细胞抑制率均明显高于单用药组(P <0.05)。2.各组细胞凋亡率比较:单用ZnPP(20μmol/L)或DDP(5μg/ml)48h后, 细胞凋亡率均较对照组升高,分别为9.61%和25.35%( 对照组:1.79%);联合用药后细胞凋亡率显著升高,达51.46%,与单用药组比较差异有统计学意义(P <0.05)。3.各组细胞中HO-1mRNA表达变化:对照组中可见HO-1mRNA表达,应用ZnPP后细胞中HO-1mRNA表达降低;而应用化疗药物CDDP后,HO-1mRNA表达明显升高,联合应用ZnPPIX可逆转此现象,提示外源性应用HO-1特异性抑制剂ZnPPIX能够抑制HO-1mRNA表达。4.各组细胞中HO-1蛋白表达变化: HO-1蛋白表达变化与其mRNA表达一致。5.各组细胞内活性氧变化:对照组细胞内活性氧水平较低,应用ZnPP或CDDP后活性氧升高,与对照组比较分别增加了0.51±0.05和0.59±0.04倍;联合用药后能活性氧显著提高,较对照组提高了2.37±0.19倍,与单用药组比较有统计学意义(P <0.01)。三 讨论本实验结果显示ZnPP对HepG2细胞生长抑制作用呈剂量依赖性,同时细胞中HO-1mRNA和蛋白表达下调,细胞内活性氧产生增加,提示ZnPP抑制HepG2细胞生长活性可能与降低细胞HO-1表达,增加细胞内活性氧产生有关。应用化疗药物CDDP后,细胞内HO-1表达增高,联合应用ZnPP抑制细胞HO-1表达后,细胞内活性氧和细胞凋亡率较单用药组显著增加,表明ZnPP能够通过阻断细胞内HO-1表达增加细胞化疗敏感性,其机制肯能与增加细胞内活性氧有关,与在其他肿瘤细胞[5]中报道一致。但Hill M[6]等在乳腺癌细胞中也发现,人为降低HO-1表达能促进肿瘤生长,提高HO-1表达则降低肿瘤生长。HO-1在不同肿瘤细胞中作用不同,可能与组织细胞特异性有关,具体机制还有待于进一步研究。总之,合理调控肿瘤中HO-1表达有望为肝癌治疗提供一个新的思路。参考文献:[1] 陈晓波,李永翔,董维平等.血红素氧合酶-1基因转染对大鼠胰岛培养的影响.中华实验外科杂志,2007,24:415-416[2] 刘胜春,姚榛祥,孙正魁.锌原卟啉对种植性乳腺癌细胞凋亡的影响.中华实验外科杂志,2006,23:525-527[3] 陈洪元,张黎,程力,等.短发夹RNA沉默血红素氧合酶-1基因表达对胃癌细胞系SGC-7901生物学行为的影响.中华实验外科杂志,2009,26:199-201[4] Mayerhofer M,Gleixner KV,Mayerhofer J, et al. Targeting of heat shock protein 32 (Hsp32)/heme oxygenase-1 (HO-1) in leukemic cells in chronic myeloid leukemia: a novel approach to overcome resistance against imatinib.Blood,2008, 111:2200-2210[5] Hill M,Pereira V,Chauveau C,et al. Heme oxygenase-1 inhibits rat and human breast cancer cell proliferation: mutual cross inhibition with indoleamine 2,3-dioxygenase. FASEB J, 2005, 19:1957–1968.
孔连宝 主任医师 江苏省人民医院 肝胆中心3666人已读 - 论文精选 抑制核因子-κB对大鼠吻合肝动脉部分肝移植模型的保护作用
前期的实验证实吻合肝动脉的大鼠部分肝移植术与不吻合肝动脉的大鼠部分肝移植术相比能明显减轻肝脏早期的缺血再灌注损伤(IRI)[1],我们在建立吻合肝动脉的大鼠部分肝移植模型的基础上,对抑制核因子-κB (NF-κB) 在吻合肝动脉的部分肝移植模型早期IRI中的作用进行研究。一.材料及方法1.实验动物分组:选取清洁雄性Spraque- Dawley 大鼠120只(由南京医科大学实验动物中心提供),体重225~250g,配成60对。术前12h禁食,4h禁水。采用改良的二袖套法建立吻合肝动脉的小移植物模型,参照文献 [2, 3],供体肝中叶为移植肝,其重量相对受体肝重量约37%(34%-43%)。60只受体大鼠随机分成A、B、C三组,对照组(A组,20只):术后分别在30min, 2, 3, 6和12h 等5个时间点处死4只大鼠并采取肝组织及血清样本;缺血预处理组(IP)组(B组,20只):供体及受体鼠术前分别阻断肝门血供15min,再灌注20min,余同对照组;二硫代氨基甲酸吡咯烷(PDTC,购于Sigma 公司)组(C组,20只):供体及受体鼠术前15min 尾静脉注射PDTC15mg/kg,余同对照组。2.观察指标及方法:NF-κB 的测定采用免疫组化法,先将常规石蜡切片脱蜡至水,高温下抗原修复,加入NF-κB p65 单抗(购于美国Santa Cruz公司),进行免疫组化染色。染色结果判定:NF-κB p65 活化细胞表现为胞浆、胞核黄或棕黄染色。按试剂盒说明书测定丙二醛(MDA)含量和超氧化物歧化酶(SOD)活性(购于南京建成生物工程研究所)。ELISA 方法检测肿瘤坏死因子α (TNF-α)在血清中的表达。病理学检查:肝组织采取石蜡切片,H-E染色做常规病理学检查。3.统计学方法:运用SPSS12.0软件进行分析,数据以均数±标准差( ±s)表示。两组间均数比较用t 检验。二.结果1.肝组织免疫组化染色结果:B 组和C 组(图B 和C )肝组织中NF-κB p65 细胞阳性率较A 组(图A )明显降低(P0.05)。图1免疫组化染色 ×2002.血清TNF-α :B 组和C 组血清TNF-α 含量明显低于A 组(P0.05)。见表1表1 术后血清TNF-α 表达水平(pg/mL, ±s )组别0.5h2h3h6h12hA 84.7±19.8*150.6±31.6*232.6±41.7*218.3±56.1*191.3±37.1*B64.3±18.7*111.4±21.5*163.4±51.4*157.5±47.8*139.8±33.9*C59.3±22.4*121.6±32.7*161.9±49.7*151.3±51.0*132.5±38.5*注: *表示在同时间点B 组或C 组与A 组比较 P
孔连宝 主任医师 江苏省人民医院 肝胆中心2103人已读 - 论文精选 超声刀技术在肝肿瘤切除术及活体肝移植术中的应用
超声刀技术在肝肿瘤切除术及活体肝移植术中的应用孔连宝【摘要】 目的:观察超声刀技术在肝肿瘤切除术及活体肝移植术中应用的临床效果。方法:回顾性对比采用超声刀技术和未采用超声刀技术在肝肿瘤切除术及活体肝移植术中临床效果差异。结果:采用超声刀技术的肝部分切除术病人组与未采用超声刀技术组的病人相比术中出血量、术后24小时引流量明显减少,术后一周天冬氨酸氨基转移酶(ALT)明显降低。结论:超声刀技术在肝肿瘤切除术及活体肝移植术中是一种安全、有效的工具,可进一步推广及运用。【关键词】 超声刀;肝肿瘤切除术;活体肝移植 The application of ultrasonic dissector (CUSA) in hepatectomy and partial liver transplantation KONG Lian-bao, WANG Xue-hao,ZHANG feng, LI Xiang-cheng, JIANG Wei-wei Liver Transplantation Center, The First Affiliated Hospital of Nanjing Medical University, Nanjing 210029, China 【Abstract】 Objective: To evaluate the clinical effect of Ultrasonic Dissector (CU SA) in hepatectomy and partial liver transplantation. Methods: The clinical data were retrospectively analyzed among group of with ultrasonic dissector (CUSA) and without CUSA method. Result: The intraoperative bleeding and postoperative drainage of the CUSA group were significantly less than the group of without CUSA method. The (ALT) of with CUSA group also is lower than without CUSA group. Conclusion: CUSA is a kind of safe and effective instrument in hepatectomy, which should be suggested to apply in clinic. 【Key words】 Ultrasonic Dissector (CUSA); Hepatectomy; Partial liver transplantation 如何有效地减少出血是肝肿瘤切除术及活体肝移植供体手术重要环节。外科医生手术方法的不断改进,新手术器械的不断出现及应用,切肝时的出血量较以往已明显减少。超声刀(CuSA)具有振荡切割、冲洗、吸引等种多功能,适合在肝脏外科手术中使用,近几年来越来越受到手术者的青睐,我们在熟练掌握超声刀技术后,1995年开始将该技术运用于中国首例活体肝移植供体的肝部分切取术,在2004年又将该技术运用于肝脏肿瘤切除术,2004年至今共对56例肝脏肿瘤的病人和17例活体肝移植供体采用超声刀(CuSA)技术进行肝脏手术,取得了令人满意效果,报道如下: 1 资料与方法 1.1 一般资料 采用超声刀(CuSA)技术进行肝脏手术的病例:56例肝脏肿瘤的病人(观察组A)中男性37例,女性19例,年龄28~67岁,平均年龄51.7岁,良性肿瘤(血管瘤)13例,恶性肿瘤43例;17 例活体肝移植供体(观察组B)中男性7例,女性10例,年龄33~47岁,平均年龄38.3岁。记录术中出血量、术后24小时引流量、肝功能等生化指标和术后并发症等,并与该时期其他未使用超声刀的肝肿瘤切除术的212例病人(对照组)进行比较。 1.2 手术方法 手术中无肝硬化和伴有肝硬化的肝组织,超声刀输出功率分别控制在40w[1]和50~60w。采用全身麻醉,右肋缘下或经腹直肌切口,进腹后对肝脏周围韧带进行离断,充分暴露手术视野,肿瘤患者术中根据肿瘤大小及位子决定是否进行肝门阻断,肝移植供体不进行肝门阻断,用高频电刀切开肝被膜后,以超声刀进行切割,侧面注水,吸引碎肝组织和液体。以血管钳分别钳夹2毫米以上的血管及胆管,用1号线结扎较粗管腔双扎或缝扎,肝移植供体采用钛夹来钳夹2毫米以上的血管及胆管,直至肿瘤病人完整切除肿瘤或肝移植供体部分肝脏切取完成,且以高频电刀电凝创面或以大网膜覆盖创面。观察组56例肝脏肿瘤的病人中左外叶切除术2例,左半肝切除术9例,右半肝切除术23例,肝段切除术22例;观察组17例活体肝移植供体,左半肝切取术8例,右半肝切取术不带肝中静脉的7例,右半肝切取术带肝中静脉的2例。 1.3 统计学方法 采用SPSS12.0软件进行数据分析,数据均以Mean±SD表示,两组间比较采用t检验,P直肠癌保肛手术中应用的对比研究[J]。中华普通外科杂志,2007,22(11):875-876。 [4]. 温浩,张金辉,曹峻。螺旋水刀和超声刀在肝叶切除术中的应用[J]。肝胆外科杂志,2005,13(6),410-411 [5]. Wei AC, Tung-Ping, Poon R, et al. Risk factors for perioperative morbidity and mortality after extended hepatectomy for hepatocellular carcinoma [J]. B r J Su rg, 2003, 90 (1): 33-41 [6]. Koo BN, Kil HK, Choi JS, Kil, et al. Hepatic resection by cavitron ultrasonic surgical aspirator decreases the incidence and severity of venous air embolism [J]. Anesth Analg, 2005, 101 (4) : 966 – 970 [7]. Fan ST, Lo CM, Liu CL, et al. Safety of donors in live donor liver transplant- ation using right lobe grafts [J]. Arch Surg, 2000, 135(3): 336 -340
孔连宝 主任医师 江苏省人民医院 肝胆中心4586人已读





