张巍医生的科普号
- 精选 肝癌的介入治疗有哪些?
癌症是全世界的一个主要死因,2020年近1000万例死亡由癌症导致。原发性肝癌是全球第六大常见恶性肿瘤,占肿瘤致死率的第三位,五年生存率不足20%。更可怕的是,中国肝癌的发病率与死亡率接近全球的二分之一。问:那为什么肝癌如此可怕?答:因为肝脏是一个不存在末梢神经的“沉默器官”,像一个默默工作的老黄牛,不像胃肠、心脏等器官那样一旦受损便会剧烈疼痛,但是很少人会在早期就说肝疼,而感觉到疼痛不舒服去医院就诊,一旦确诊为肝癌,往往都是中晚期了,失去了外科手术切除的机会。问:谁是肝癌的高危人群?答:提醒大家,肝癌早期症状不明显,高危人群要定期检查!尤其乙肝患者、乙肝病毒携带者;40岁以上有慢性肝炎病史的男性;肝硬化患者,长期嗜酒者;喜欢进食腌制品者;有肝区不适、疼痛等症状,曾检测甲胎蛋白有过异常,但未证实是肝癌者。对于肝癌的高危人群,定期做肿瘤指标、超声、磁共振等检查,做到“早发现早治疗”。问:如果发现是中晚期的肝癌,在这样的情况下,患者就没有治疗的机会了吗?答:事实并非如此,其实现在的介入治疗以及多学科的综合诊治,是挽救肝癌患者的有效手段,部分患者可以缩小肿瘤,达到降期的目标,接受外科手术切除。问:目前介入治疗肝癌都有哪些方法?各有哪些优势?答:这里就为大家介绍下介入治疗肝癌的几种方法:1. 经动脉化疗栓塞术(TACE)先在大腿根部或者手腕区域局部麻醉,再穿刺此处股动脉或桡动脉,将导管装置插入,导丝沿着动脉一路上行到达肝动脉,一步步进入肿瘤的供血动脉。到此处,我们的武器就到达了肿瘤细胞的门口了,向导管内注入提前混合的栓塞剂和化疗药物,这些药物被精准的送进肿瘤里。使用栓塞剂封堵肿瘤供血动脉,达到饿死肿瘤的目的。相比起全身化疗,TACE进行的局部栓塞化疗使局部药物浓度强大N倍,但副反应更少了,疗效更好了。在这样饥饿疗法和局部化疗的双重打击下,相当一部分肝癌细胞被消灭殆尽。由于原发性肝癌的血液供应90%至95%来自肝动脉,因此把肿瘤的供血动脉堵掉,让断了血供的肿瘤慢慢萎缩,这是治疗肝癌的有效方法之一。目前TACE治疗已经被公认为中晚期肝癌的首选治疗。据2008至2009年中国肝癌特征和治疗分析调研结果显示,我国的肝癌患者接受的治疗中,介入治疗占61.9%,手术治疗占50.38%,在介入治疗当中,TACE占91.44%。采用局部靶向药物灌注、肿瘤血管栓塞方式集中杀灭肿瘤细胞,最大限度地降低肿瘤负荷(减少恶性肿瘤数量、体积)。近年来,后续联合其他局部治疗手段、靶向药物和免疫治疗可有效地改善了患者的生存质量,延长了生存时间,并可逆转部分患者肝癌分期,使不能切除的肝癌病例转化为可切除的肝癌病例。另外,近年来钇90放射微球可以通过肝动脉,将放射性树脂微球注射于肿瘤区。相较于传统的体外放射,不仅提高了对肿瘤局部的杀伤力,而且辐射范围小、半衰期短,大大减少了对正常肝组织的危害。钇90治疗可实现肿瘤缩小和余肝增大的双重效应,不仅可显著改善中晚期肝癌患者的生存质量,而且在肝癌的降期治疗方面发挥着越来越重要的作用。 2. 肝动脉化疗灌注治疗(TAI/HAIC)和TACE一样,这一方法同样也是经股动脉插管,不同之处在于是将化疗药物长时间、缓慢、持续地注入肿瘤供血动脉,目前临床上灌注时间长达数小时至数十小时不等。这一技术既能减少全身的副反应,又能增加局部药物浓度而对肿瘤造成定点打击。常常作为一种姑息治疗,在晚期肝癌患者中应用,有部分患者也获得了肿瘤缩小,成功降期,能够接受后续手术治疗。 3. 碘125粒子植入碘125粒子是一种体积很小的放射性物质,将其直接植入到肿瘤里,能够持续性的发出损伤射线,杀伤不同时期的肿瘤细胞和肿瘤周围细胞,而几乎不损伤正常组织。碘125粒子植入治疗只需对患者进行局部麻醉,操作简单,不会造成太大的创伤,安全性较高。传统的外照射因放射野大、正常组织耐受量低,其疗效常受到一定的限制。局部放射性粒子植入技术作为传统外照射放疗及化疗的一种补充治疗手段,具有近期疗效好、微创、副作用小、安全性高的特点。对于一些位置不好切除,局部转移或复发的,粒子植入有较好的效果。针对门脉主干因癌栓形成闭塞的肝癌患者,为了对门脉癌栓有更好的治疗作用,门静脉支架联合粒子条植入应运而生。在门静脉主干癌栓部位植入一枚金属支架,同时在支架和门静脉血管壁之间植入粒子条,这样在打通门静脉改善肝功能的同时,又持续近距离放射治疗抑制癌栓生长的作用。 4.消融治疗肝癌消融治疗包括热消融技术(射频消融和微波消融)、冷冻消融技术等。热消融是经皮肤穿刺进入肝内病灶,利用高温热效应,通过组织中极性分子尤其是水分子的振荡加热肝组织,从而在靶区内引起热凝固,通俗点说就是烧死肿瘤,能达到与肝癌切除、肝移植相媲美的根治效果。尤其是对于单发小肝癌,消融效果可与外科切除相媲美。对位于重要脏器和大血管旁的复杂肿瘤有较好的安全性。对于大肝癌或巨块型肝癌,则可以将TACE治疗与局部消融治疗序贯、或同时配合,特别是结节型、团块型肝癌,同样能大大提高肿瘤的完全坏死率,减轻TACE重复次数过多造成的肝损害。此外,对于肝癌手术切除术后复发或肝功能储备功能差不能耐受手术切除的肝癌患者,消融亦是一种较为理想的微创治疗方法。 问:以上几种介入治疗肝癌的方法该如何选择?答:对于选择介入治疗方法,要结合患者的一般体力状态、肝功能、凝血功能的情况,还有CT或磁共振表现出的肿瘤的大小、位置等等,有可能选择某一种介入治疗方法,也有可能选择几种治疗联合在一起,现在也会结合靶向、免疫治疗等药物,通过肝癌多学科诊疗(MDT)模式的讨论来制定,帮患者接受到更高效、全面、个体化的治疗,达到控制肿瘤,延长生存期的目标。
张巍 副主任医师 上海中山医院 介入治疗科470人已读 - 精选 肝癌介入治疗的进一步思考
文章来源:《介入放射学杂志》,2019,28:507-510作者:马婧嶔,颜志平,复旦大学附属中山医院介入治疗科肝细胞肝癌(HCC)是全球最常见恶性肿瘤之一,发病率居恶性肿瘤第6位,死亡率居第2位,每年约有59万余人死于HCC[1]。20世纪70~80年代林贵等[2- 3]在国内率先应用选择性血管造影诊断原发性肝癌、肝动脉栓塞治疗原发性肝癌以来,肝癌介入治疗逐步在我国得到推广发展。经过近40年努力,针对肝癌的介入治疗从经动脉途径的经导管动脉化疗栓塞术(TACE)到肿瘤消融、放射性粒子植入等局部治疗,从肝癌病灶治疗到门静脉、下腔静脉及胆道肿瘤性病变治疗,从病灶局部治疗到伴发症状、并发症的全身治疗,已形成较完整体系[4- 9]。肝癌介入治疗取得了很大成就,但有些方面也需要进一步思考。1对肝癌另类理解肝癌可视为一种慢性疾病,患者多有慢性肝病基础,因此治疗难以做到真正治愈,需要反复多次治疗并终身随访[10]。医患双方均要有长期治疗、终身随访的心理准备,在制订治疗规划及方案时实现可持续发展。2肝癌介入治疗目标临床医疗的终极目标是治愈疾病。由于肝癌具有肿瘤恶性程度高、起病隐匿、多伴发肝病基础等特点,多数患者在诊断明确时已处于中晚期,失去了手术治疗机会。以介入为主综合治疗中晚期肝癌比较合理的目标是控制肿瘤生长,延长有质量的生存期。3治病救人再考量治病是手段,救人是目的。肝癌治疗并非简单地针对肿瘤病灶进行治疗,保护正常肝脏功能、维持患者正常社会功能、延长患者高质量生存期是肝癌治疗的根本。因此,在制定肝癌治疗方案时,必须考虑治疗肿瘤与维持正常机体功能的平衡,“带瘤生存”是一种治疗策略,即让患者带着得到控制的肿瘤较高质量地生存[11],这是一种无奈却又实在的选择。4规范化与个体化治疗由于不同患者情况不尽相同,个体化治疗永远是临床医疗的根本,但个体化治疗必须建立在规范化治疗基础上。应根据患者一般状况(年龄及机体状况)、病灶情况、经济条件、社会及家庭情况、所在医院条件、经治医师情况(技术及沟通能力)等因素进行个体化治疗;根据肿瘤病灶控制情况、机体恢复状况来平衡生存时间与生存质量,从而合理掌握治疗间期,达到既控制肿瘤,又兼顾机体功能的目的。虽然中晚期患者机体与肿瘤有时会达到相对平衡,但这种平衡是很脆弱的。为此,对相对稳定的肿瘤患者不要过度干预,以免破坏平衡,导致情况恶化。但对有进展的肿瘤,则应考虑给予重点治疗,以达到新的平衡。5重视综合治疗肝癌生物学特性决定了肝癌治疗是长期、多学科、多方法的综合治疗,包括外科手术切除、肝移植、介入治疗(TACE、消融、放射性粒子植入等)、放疗、系统治疗(中医、靶向治疗、抗病毒治疗、免疫治疗、生物治疗)等[12]。实施综合治疗的最佳途径是多学科综合诊疗(multi- disciplinary treatment,MDT)会诊,但必须建立在各学科平等基础上,以实现真正意义上的MDT。通过MDT会诊可为某患者制定一整套比较完整的诊治方案,包括疾病诊断、分型、目前状况、亟需解决的问题、可采用的疗法、可能出现的问题与应急预案、如何实施治疗及随访观察等。此外,MDT会诊必须确定对该患者治疗的总负责医师,以免出现谁都能管但谁都不管的局面。6重视肝癌治疗社会适应证及效价比社会发展导致了现今医疗模式的改变,社会因素在医疗中的作用越发明显,原先的生物医疗模式已向社会医疗模式转化。为此,严格把握疾病的社会适应证和医疗适应证同样重要。社会适应证是根据对患者经济状况、医疗依从性及家庭、社会、医院等医疗环境的综合评估确定的,其结果分为优、良、中、差4级。临床医疗实践中应重视对患者肝癌治疗社会适应证的评估结果。由于社会适应证的要素大多无法量化,把握好患者社会适应证并不简单,要花时间了解情况、掌握信息、全面综合评估后才能明确。肝癌治疗方式方法多种多样,疗效也不尽相同,医疗费用差异巨大。由此产生的效价比也差异巨大。肝癌治疗效价比有时很难用客观指标统一衡量,与患方经济状况和治疗意愿关系甚大。因此效价比必须因人而异,根据不同患者社会和医疗适应证,选择最合适的治疗方案与策略,提高肝癌治疗效价比。7重视肝功能及储备影响肝癌患者治疗方案制定的第一要素就是患者肝功能。肝癌患者肝功能受多重因素影响,如是否伴发肝病基础、有无病毒活动、肿瘤占位效应、门静脉受累情况及接受何种治疗等。7.1肝癌伴门静脉癌栓治疗门静脉癌栓理想的治疗目标是直接杀灭、抑制癌栓,控制肿瘤在门静脉系统进一步浸润,同时尽可能复通受累门静脉,并恢复其正常血流,从而改善肝功能,甚至使正常肝组织代偿增生,为后续治疗增加肝功能储备;降低门静脉压力,减少门静脉高压出血危险,使肝癌病灶治疗变得更有意义。肝癌伴门静脉癌栓治疗方法多样,包括TACE、腔内近程放疗(门静脉支架术结合125I粒子条/125I粒子支架植入)、外放疗等。文献报道门静脉癌栓生长速度为每月约(0.5±0.1)cm,门静脉分支部分阻塞至主干完全阻塞平均时间仅需6周。门静脉分支癌栓内植入125I粒子条,其17 mm辐射距离对邻近肿瘤病灶行近程放疗能有效抑制癌栓进展,避免或延缓癌栓累及门静脉主干。另外,机械性闭塞病变肝叶门静脉1、2级分支,协同TACE靶动脉栓塞及125I粒子持续辐射能使患侧肝叶萎缩,达到类似“内科性肝叶切除”效果[9,13- 17]。7.2肝癌伴动脉-门静脉分流治疗动脉-门静脉分流(APS)是肝癌病灶特征之一,在分流量大的患者,高压动脉血流进入门静脉,引起动力性门静脉梗阻,导致肝外门静脉高压。对肝癌伴明显APS患者,栓塞治疗能有效减少高压的动脉血入门静脉,解除动力性门静脉梗阻,减轻门静脉高压,控制、预防门静脉高压消化道出血,缓解腹泻、腹胀及腹水等,改善肝功能。因此,针对有明显APS的消化道出血,应首选简单、有效的栓塞治疗。栓塞材料选择多种多样,微粒微球、明胶海绵、α-氰基丙烯酸正丁酯(NBCA)胶、无水乙醇及无水乙醇处理过的明胶颗粒等均可应用,应根据不同APS量及瘘口大小选择合适的栓塞材料与直径。8适度治疗与精细TACE适度治疗是临床医疗的基本原则,如何把握治疗的度是衡量一名临床医师成熟的重要指标,在中晚期肿瘤患者治疗中尤为重要。对于肝癌患者,如一般状况良好,各项检查结果均支持可积极治疗,可予精细TACE;反之,适度TACE是一较好选择。精细TACE是以微导管技术为基础,采用类CT技术全面监测靶血管精确插管及术中栓塞效果。精细TACE同时要求合理应用各类栓塞材料,如碘油、微球、载药微球及90Y微球等。其优点是能够定点治疗肿瘤病灶,减少周围正常肝组织损伤,尤其适合小病灶治疗;其缺点在于对设备和器械要求更高,同时相对传统TACE更耗时。适度TACE是对部分肝癌病灶行TACE,或对整个病灶作减量化疗栓塞,待患者一般情况改善后适时再行TACE。这是基于术者对患者整体状况及肝功能综合评估后主动作出的治疗决策,而非技术原因所迫。适度TACE可平衡肿瘤治疗与保护肝功能两者关系,以避免消灭了肿瘤但造成肝功能不可逆损伤情况。适度TACE是以降低打击肿瘤力度为代价,因此一定要掌握好“度”,不宜随意应用。消融术最初是作为根治性治疗手段,目前也越来越多地应用于减瘤荷治疗[18]。适度消融以降低打击肿瘤力度,甚至刺激肿瘤快速生长为代价,一定要掌握好“度”,且应与其它治疗联合。本中心近年来开展大肝癌(直径>5 cm)和巨块型肝癌(直径>10 cm)消融同步联合TACE治疗取得了较好疗效,疾病无进展生存时间约为(6.3±1.5)个月,中位生存时间为14个月,6、12、18个月生存率分别为91.3%、81.5%、48.0%[19]。9理性对待新型栓塞材料微导管及类CT技术使靶血管超选择达到一个顶峰,精细TACE出现使得TACE疗效明显提高,但同时也遭遇瓶颈。栓塞材料成为新的研究重点,临床上应正确理解、合理应用新型栓塞材料,如普通微粒微球、载药微球、放射性微球等。微粒类栓塞材料可有效阻断侧支循环形成,栓塞效果明确,应作为主要栓塞材料之一。与碘油乳剂能进入肿瘤组织内不同,微球只能栓塞肿瘤血管,越近肿瘤末梢血管栓塞效果越好,应根据不同肿瘤血管和不同血供程度选择不同粒径微球。与上述微粒类栓塞材料不同,90Y微球辐射纯β射线,以辐射剂量达到要求为终止目标,而不是栓塞[20- 21]。微球杀伤力与其粒径成负相关,但与其安全性成正相关。兔VX- 2模型研究结果显示,10~300μm和300~500μm粒径微球组肿瘤生长率与500~700μm和700~900μm粒径微球组比较,差异均有显著统计学意义(P<0.01);100~300μm和300~500μm粒径微球组肿瘤坏死均以重度坏死为主,其中100~300μm粒径微球组肿瘤坏死最明显[22]。这表明>500μm粒径微球偏大,难以栓塞微循环血管,要达到更有效地阻断肿瘤血供、抑制肿瘤生长目的,选用粒径≤500μm微球较为合理;100~300μm粒径微球可造成正常组织严重坏死,因此适合精确超选择插管至肿瘤供血动脉进行栓塞;300~500μm粒径微球虽较大,但仍能造成肿瘤明显坏死,且安全性较好,较适于超选插管不理想患者。兔VX- 2肿瘤模型的血供不能代表所有临床病例情况,实际应用中仍应根据肿瘤病灶血供和超选择插管情况选择合适微球,对血供丰富的病灶可选择粒径300~500μm微球,而对能精确超选择插管至肿瘤供血动脉的病灶则选择粒径相对较小微球,甚至40~120μm粒径微球。综上所述,超选择插管,选择合适种类、粒径微粒联合碘油乳剂可提高疗效,减少并发症。载药微球和放射性微球为肿瘤TACE提供了更好的栓塞材料,值得进一步研究。TACE包括碘油+微粒类栓塞剂,目前仍是主要肿瘤介入治疗方法。中晚期肝癌介入治疗不仅是针对肿瘤病灶的治疗,更是对治疗与功能保留的平衡。带瘤生存虽不完美,但很实在,延长有质量的生存期是临床治疗现实目标。当前医疗环境的改变,也促使临床上更要注意治疗的社会适应证及效价比。参考文献(略)
张巍 副主任医师 上海中山医院 介入治疗科1882人已读 - 典型病例 肝血管瘤介入治疗
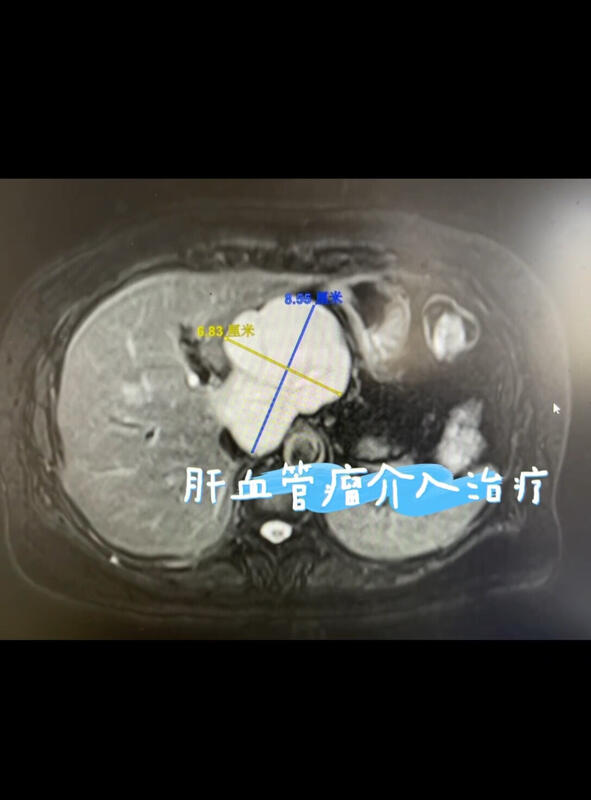 张巍 副主任医师 上海中山医院 介入治疗科209人已观看
张巍 副主任医师 上海中山医院 介入治疗科209人已观看 - 案例 小肝癌的介入治疗
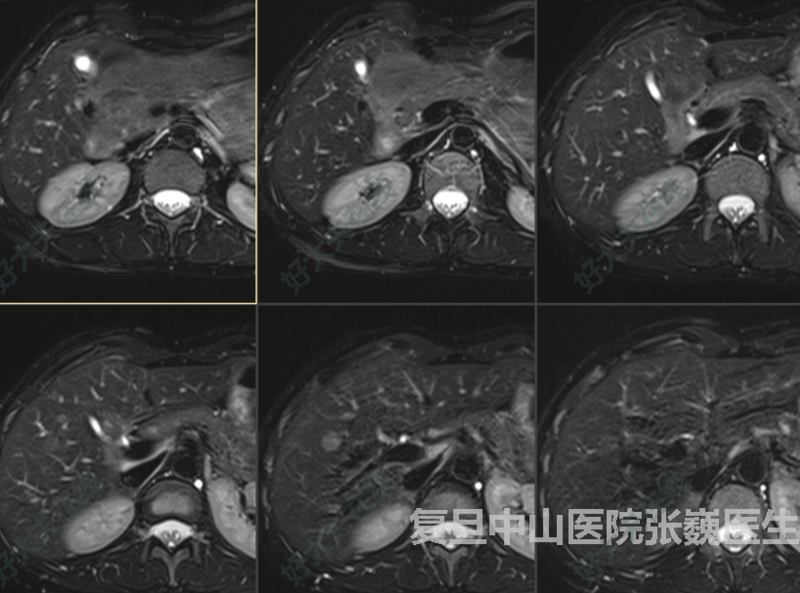
治疗前 因腹部隐痛行MRI提示肝MT,位于肝右叶,病灶直径1.2cm,外科会诊考虑手术创伤大,患者选择射频消融,但B超常规扫描不易发现。故拟行血管造影明确病灶位置,再行射频消融,另经血管造影可以明确肝内有无其他病灶。 治疗中 常规超声扫描不易发现,故拟行血管造影明确病灶位置,再行射频消融,另经血管造影可以明确肝内有无其他病灶。 治疗后 治疗后4年 消融后随访未见复发
 张巍 副主任医师 上海中山医院 介入治疗科208人已读
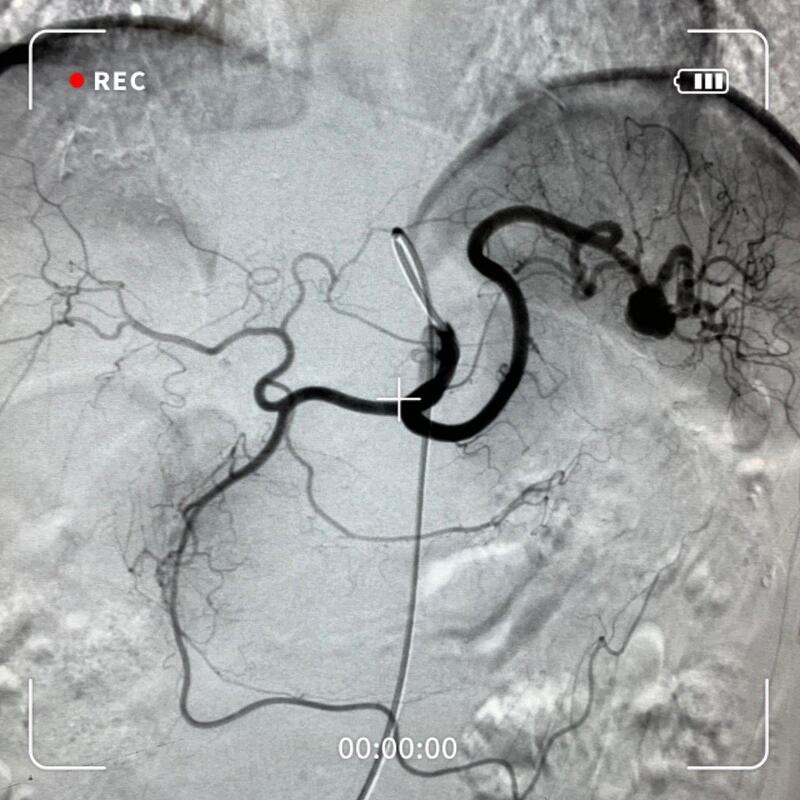
张巍 副主任医师 上海中山医院 介入治疗科208人已读 - 典型病例 脾动脉瘤介入治疗一例
通过介入微创治疗的方法栓塞脾动脉瘤!
 张巍 副主任医师 上海中山医院 介入治疗科2417人已读
张巍 副主任医师 上海中山医院 介入治疗科2417人已读 - 医学科普 异常凝血酶原在肝癌诊断中的价值
甲胎蛋白(AFP)是目前公认的最特异的原发性肝细胞癌(HCC)标记物。但存在假阳性和假阴性的问题。因此,寻找新的肝癌标记物,是肿瘤工作者的迫切任务。PIVKA-II是维生素K缺乏或拮抗剂-II诱导的蛋白质(Protein Induced by Vitamin K Absence or Antagonist-II),又称异常凝血酶原(DCP),可出现于维生素K缺乏或肝细胞肝癌(HCC)患者的血清中,由于癌细胞对凝血酶原前体的合成发生异常,凝血酶原前体羧化不足,从而生成大量的异常凝血酶原。 有研究表明:HCC患者血清中PIVKA-II的阳性率为高于AFP的阳性率,PIVKA-II与AFP并无相关性,二者对诊断HCC具有互补性,联合二者用于辅助诊断HCC,灵敏度可提高至71%。HCC患者血清AFP和PIVKA-II均可用于监测HCC的治疗效果及预测肿瘤复发的风险。但PIVKA-II阳性的患者肝内转移、门静脉侵袭和肝静脉瘤血栓形成以及包膜浸润的发生率较高。PIVKA-II血清半衰期约40~72小时,比AFP短3~5天,能更及时反映HCC的疗效。随访HCC患者治疗后AFP和PIVKA-II水平,发现治疗后PIVKA-II水平恢复正常组其5年及长期生存率比异常组明显提高。另有研究表明,经外科手术切除等治疗后,PIVKA-II水平降低并维持低水平者HCC复发风险显著降低。因此PIVKA-II用于预测患者预后有较高的价值。 目前,国内外的指南已把PIVKA-II列为肝癌检测极其重要的指标。《亚太肝病学会》、《日本肝病学会》均已将PIVKA-II写入指南中,推荐用于高危人群的筛查、肝癌的辅助诊断、监测治疗效果、作为预后和复发的预测工具。对于慢性HBV、HCV感染或肝硬化患者等HCC高风险人群,建议应用肝脏超声检查、AFP和PIVKA-II水平检测进行HCC的监测,每6个月复查一次;对于HBV或HCV肝硬化患者等极高风险人群,则应将间隔缩短为每3~4个月。中国最新《慢性乙肝防治指南》2015年版中,推荐使用PIVKA-II作为诊断HCC的重要指标,可与AFP互为补充提高HCC的早期诊断率。
张巍 副主任医师 上海中山医院 介入治疗科1.6万人已读 - 医学科普 植入式静脉输液港的临床应用
近年来肿瘤疾病呈现高发概率的趋势,对于人们生命健康以及生活质量造成严重影响。医学技术日新月异的今天,肿瘤患者的生存期不断得以延长,恶性肿瘤患者需要经常接受大量输液进行治疗,但是长期进行输液会使患者血管弹性变差,另一方面当前绝大部分的化疗药物对于患者的血管有较大刺激,长时间使用会导致患者出现静脉内膜损伤,影响治疗效果。对患者使用外周静脉注射方法进行输液,其中患者如果有肥胖、水肿或者是患者想要找出浅静脉存在有一定难度,故此建立可靠的深静脉通道,对于肿瘤患者的治疗起重要作用。植入式静脉输液港(central venous port access system,CVPAS)是一种可植入皮下长期留置在体内的静脉输液装置,主要由供穿刺的注射座和静脉导管两部分组成,导管末端位于中心静脉。输液港是专门为需要长期及重复输液的患者设计,适用于化疗药物、肠外营养(TPN)的静脉注射或连续输注,还可以用于抗菌素、血液制品、普通静脉补液及采血等几乎所有的静脉治疗,是一种可以完全植入体内的闭合静脉输液系统,可以减少反复静脉穿刺的痛苦和难度,防止刺激性药物对外周静脉的损伤,并且患者日常生活不受限制,可以沐浴,大大提高了其生活质量。因感染率低,无裸露部分,患者生活质量高,近年来在国内逐渐开展。操作流程上所有的静脉输液港植入术均在专用导管室或手术室完成。以颈内静脉及锁骨下静脉入路为例:(1)体位,病人取平卧位,需要穿刺侧的肩部稍垫高,头偏向对侧;(2)消毒,颈部、胸壁和肩部常规碘酒、酒精消毒,铺无菌单;(3)麻醉,2%利多卡因穿刺部位皮下局部浸润麻醉;(4)穿刺过程,锁骨下静脉穿刺点选择锁骨中外1/3下方部位穿刺;颈内静脉穿刺选择胸锁乳突肌下端分叉与锁骨形成的三角形区域内,斜向同侧乳头方向进针穿刺;在超声引导下确认血管后,实时引导行静脉穿刺术,穿刺针进入静脉后,经穿刺针置入导丝后经DSA透视明确导丝顺利进入上腔静脉,沿导丝置入静脉港导管鞘后抽出导丝,置入静脉港导管,回抽确认静脉回血后再次经DSA透视,确认静脉港导管末端位于上腔静脉与右心房交界处。(5)建立港穴,于同侧锁骨下方偏外侧皮肤、皮下组织行局部浸润麻醉,切开皮肤、皮下组织后于皮下脂肪层钝性游离,形成假体腔穴,用隧道针自港穴至穿刺点做皮下隧道以使静脉港导管穿过,连接导管与静脉港出口并上锁固定。最后注射器抽吸静脉港回血顺利,脉冲式注入肝素盐水无渗漏,缝合切口,无菌敷料覆盖切口。术后应注意:观察病人呼吸、心率、意识、发绀及发烧等情况;观察伤口情况,敷料保持干燥;术后第二天伤口换药,如有出血、渗血、渗液时,及时更换敷料;术后7-10天拆线,现在不少医生都使用可吸收线,进行皮内缝合,避免的患者拆线的烦恼。植入式静脉输液港作为一种新的输液方式,适用于需要长期或重复输液(或输血) 、完全肠外营养等患者,恶性肿瘤化疗患者建立输液港能保证患者化疗及其他输液需要,相对于传统浅表静脉或中心静脉置管等方式输液,化疗静脉炎、渗漏、导管堵塞等并发症发生率明显降低,尤其对于反复输液导致浅表静脉条件差无法再进行输液的患者更为适宜。从临床报道来看,输液港一次穿刺成功率高,适宜长期留置,这对于提高患者生活质量、减少护理人员工作量具有明显优势,减少反复静脉穿刺能提高患者治疗依从性。
张巍 副主任医师 上海中山医院 介入治疗科3677人已读 - 医学科普 TACE治疗肝癌的理论基础及适应症
原发性肝癌是世界上常见的恶性肿瘤,其中以肝细胞性肝癌(hepatocellular carcinoma,HCC)为最多。HCC的治疗分为手术切除和非手术治疗,但临床中HCC早期症状通常不明显,绝大多数发现时已处于中晚期,或者由于伴有较重肝硬化、肝功能异常等条件限制,使临床发现的HCC能够获得手术切除机会的不足25%,并且手术后复发率较高。对于不具备手术切除条件的病人,目前临床上多采用以介入治疗为主的非手术方法,经肝动脉化疗栓塞术(Transarterial Chemoembolization,TACE)是最主要的选择。TACE治疗HCC的理论基础:正常肝组织的血供70%-75%来自门静脉,仅25%-30%来自肝动脉。而HCC的血供95%-99%来自肝动脉,结扎或栓塞肝动脉后,肿瘤血供减少90%,而正常肝组织血流量只减少35%-40%,不影响正常肝组织血供。肿瘤组织对于缺血、缺氧敏感性较高,并且由于肿瘤血管多较正常血管增粗,而且血流缓慢,具有虹吸现象,可以使化疗药物和栓塞剂较多地滞留在肝癌血管组织内。因此TACE治疗一方面经肝动脉选择性地将化疗药物注入肿瘤的供血动脉内,使肿瘤组织中的药物浓度比周围正常肝组织高5-10倍,使肝肿瘤细胞坏死,而对正常肝组织影响较小。另一方面经导管注入栓塞剂使毛细血管床、小动脉和动脉主干被栓塞,造成肿瘤局部供血中断或明显减少,减少了血流对化疗药物的冲洗,延长药物与肿瘤的接触时间,使肿瘤局部缺血、坏死。使用碘油栓塞时,正常肝组织中Kuffer细胞可短时间内将碘油吞噬,而HCC组织中缺乏Kuffer细胞,因此碘油可选择性的长时间在肿瘤组织内滞留,增加药物的接触时间,促进肿瘤的坏死。HCC血供复杂,主要有肝动脉供血,门静脉亦参与供血,肿瘤的中心由肝动脉供血,而周边部位、周边的子灶等由门静脉供应给部分血液。因此单纯动脉栓塞不足以杀死全部癌细胞,须结合门静脉治疗才能提高疗效。肝动脉和门静脉之间有丰富的交通支,通常情况下不开放,只有当碘油量超过一定界限后,该交通支才开放使碘油通过交通支进入门静脉,达到肿瘤动脉与门静脉双重栓塞的目的。因此用微导管超选择性插管于肝动脉亚肝段支,注入碘油乳剂使肝肿瘤病灶内充满碘油,并溢入瘤周的门静脉小分支,从而达到肝动脉和门静脉双重栓塞的效果,可造成小肝癌所在肝段或亚肝段的完全性缺血性梗死状态,明显提高治疗效果。TACE治疗HCC的适应症:在临床中TACE主要适用于不能手术切除的中晚期HCC,无严重肝肾功能障碍,无严重的凝血功能异常的情况,其包括:巨块型肝癌,肿瘤占整个肝脏的比例<70%;多发结节型肝癌;门静脉主干未完全阻塞或虽完全阻塞但肝动脉与门静脉间代偿性侧支循环形成;手术切除后复发;肝肿瘤破裂出血及肝动脉-门脉静瘘造成门静脉高压甚至出血。另外在如下情况也可以应用TACE:肝癌手术或肝移植术前后为增强治疗效果,减少复发的预防性治疗;小肝癌,但全身状况不适合或者不愿意手术。
张巍 副主任医师 上海中山医院 介入治疗科7836人已读





