杨中华医生的科普号
- 精选 脑出血后遗症不要悲观!
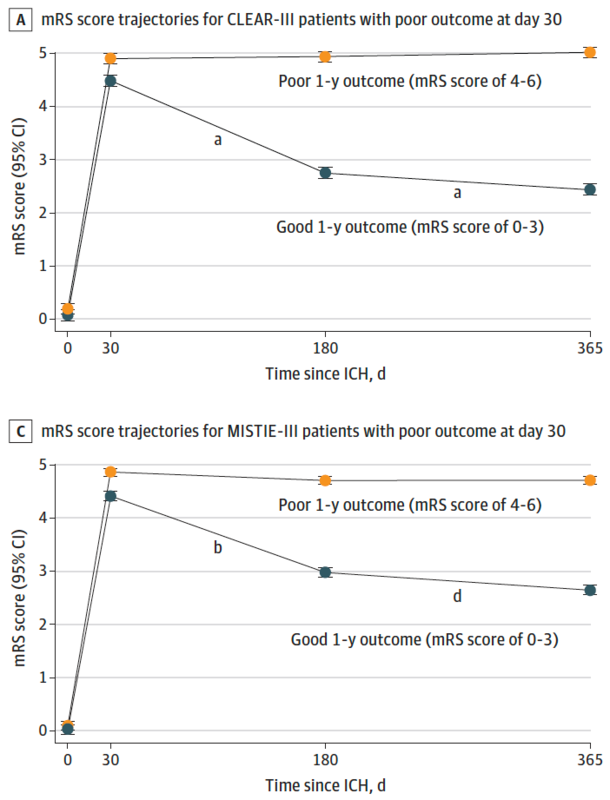
一般会在入院后判断脑出血(ICH)患者的预后,并且大多数预测模型都是预测短期结局。然而,严重脑出血的幸存者发病之初往往残疾严重,90天mRS中位数为5,将来会恢复到什么程度并不清楚。在一项基于人群研究的荟萃分析中,12%至39%的ICH幸存者在1年后获得了功能独立。然而,大多数关于ICH长期预后的研究都是单中心研究,很少探讨最初严重残疾的ICH患者的长期康复情况。对于这些患者及其治疗者来说,长期预测和决策具有重要意义。2022年9月来自美国的WendyC.Ziai等在JAMANeurology上公布了他们的研究结果,目的是探讨发病之初严重残疾的ICH和脑室出血(IVH)幸存者1年的恢复过程。这项事后分析纳入了两项随机对照试验(CLEAR-III和MISTIE-III)所有个体患者数据。在999名入选患者中,把13例未进行30天mRS评分排除后,724名30天mRS4-5分的患者存活。另外9名患者因丢失1年mRS评分而被排除在外。最终合并队列中共715名患者(71.6%)的30天mRS4-5分。主要结局指标为1年的mRS,并二分为良好结局(mRS0-3)和不良结局(mRS4-6)。715名幸存者中,417名(58%)为男性,总平均年龄为60.3(11.7)岁。到1年时,129名参与者(18%)死亡,308名参与者(43%)达到了0~3分。未调整模型的组合队列中,以下因素与恢复不良(lackofrecovery)有关:糖尿病、NIHSS、严重脑白质疏松症、松果腺移位、急性缺血性中风,胃造口术以及30天时持续性脑积水。以下因素与良好结局有关:30天时ICH和IVH吸收。在CLEAR-III模型中灌注压低于60mmHg、脓毒症、长时间机械通气,在MISTIE-III模型中需要颅内压监测是预后不良的额外因素。基于30天事件的模型强烈预测了1年的结局(AUC,0.87;95%CI,0.83-0.90),与仅使用基线严重度因子的模型相比,识别能力显著提高(AUC,0.76;95%Cl,0.71-0.80;P<0.001)。最终作者认为,对于最初功能结局不良的重度ICH和IVH患者,1年中超过40%的患者能够恢复到良好状态。医院事件与长期功能恢复密切相关,可能是干预的潜在目标。避免早期悲观预测,应将预测推迟到治疗后,可以提高预测未来康复的能力。文献出处:JAMANeurol.2022Sep1;79(9):856-868.doi:10.1001/jamaneurol.2022.1991.One-YearOutcomeTrajectoriesandFactorsAssociatedwithFunctionalRecoveryAmongSurvivorsofIntracerebralandIntraventricularHemorrhageWithInitialSevereDisability
 杨中华 主任医师 北京天坛医院 神经病学中心937人已读
杨中华 主任医师 北京天坛医院 神经病学中心937人已读 - 脑卒中的康复治疗 Lancet N:卒中后吞咽困难治疗新进展
卒中后大多数患者都有吞咽困难,这可能引起吸入性肺炎、营养不良和功能结局不良。旨在减少这些并发症的保护性干预措施仍然是治疗的基石。饮食调整和口腔卫生有助于降低吸入性肺炎的风险,补充营养,包括管饲,可以防止营养不良。康复干预旨在增强吞咽功能,不同的行为策略在小型研究中显示出前景。一些研究已经探索了药物治疗的作用,如辣椒素和其他可改变咽部感觉的Transient-Rreceptor-Potential-Vanilloid-1(TRPV-1)感觉受体激动剂。神经刺激技术,如经颅直流电刺激、重复经颅磁刺激和咽部电刺激,可能会促进感觉运动吞咽网络内的神经可塑性。进一步了解卒中后和康复期间吞咽困难患者的中枢和外周感觉运动机制,将有助于优化治疗方案。介绍吞咽困难是指将食物、饮品和唾液从口腔送到胃入口过程中存在障碍。由于吞咽需要皮层、皮层下和脑干网络进行中央控制,吞咽困难通常发生在卒中的急性期,卒中病例的患病率高达75%。吞咽困难不仅会影响生活质量,还会导致严重并发症。由于侵入气道,与吸入性肺炎的关联已得到充分证实。除了肺炎,卒中后吞咽困难还会造成口腔摄入困难而导致营养不良。由于这些严重并发症,吞咽困难与住院死亡率和医疗系统的成本增加有关。吞咽困难的并发症通常发生在卒中早期,因此及时处理非常重要。临床筛查方案结合仪器金标准的评估(如软式内视镜评估和视频透视吞咽检查)在分级诊断中具有决定性作用。在之前的综述中,我们详细描述并讨论了卒中后吞咽困难的诊断问题。在这篇综述中,我们重点关注卒中后吞咽困难患者的治疗策略。尽管吞咽困难具有重要临床意义,但多年来一直被忽视,这是因为以前缺乏证据或证据存在异质性。不过,这种情况已经发生了显著变化,因为现在发表了许多研究为卒中后吞咽困难的治疗提供了证据。为了实施这些循证治疗的方案,本文对可用的治疗策略进行了全面总结。我们首先提出一个通用的最低治疗标准,甚至适用于资源有限的情况。然后,深入到先进的附加疗法。最后,本文概述了该领域未来的研究方向。饮食干预改变食物和液体的质地是解决吞咽困难的治疗基石,其原理是不同粘稠度食团的吸入风险是不同的。饮食干预的证据受到不同研究采用的非标准食团的一致性的限制。自2017年以来,国际吞咽困难饮食标准化倡议提供了食团质地标准化定义和术语的框架。该框架定义了从低粘度到高粘度的八个连续性稠度水平。该框架的0–4级为饮品,3–7级为食物。级别3和4表示重叠粘稠度(overlappingconsistencies)。该框架还包括易于掌握的测试程序,以便确定各自的粘稠度级别。质地改良,如饮品增稠和将固体食物制成糊状,是管理吞咽困难的常用方法。在一项针对西班牙120名卒中患者的研究中,通过将饮品增稠,随着吞咽食团粘稠度的增加,误吸的频率逐步下降。在一项纳入了454名日本卒中患者的研究中,采用个性化饮食干预措施,结合改变食物的质地,饮食处方的频率与营养状况的改善、身体功能的改善和住院时间的缩短独立相关。一项关于改变口咽吞咽困难患者食物质地的系统综述得出结论,饮品增稠会降低误吸频率,但改变质地也会导致咽部残留物增加。在一项纳入了443名日本卒中患者的回顾性研究中,发现摄入低质地食物与营养不良和少肌症有关。这可能是由于质地改变降低了患者的食欲,以及降低了患者对这种饮食的可接受性程度。由于长期不良影响,改变质地最适合于吞咽困难急性期的短期早期干预。因此,吞咽功能训练可以在吞咽困难康复的早期开始(例如,即使仍然需要管饲喂养)。饮食干预措施应个体化,最好采用仪器诊断测试。在panel1中概述了国际指南中提出的治疗建议。panel1:自2017年以来发表的关于卒中后吞咽困难治疗的国际指南推荐意见欧洲卒中组织和欧洲吞咽障碍学会卒中后吞咽困难诊断和治疗指南•根据合理的吞咽评估,推荐摄入改变质地的饮食。吞咽困难管理推荐行为吞咽训练,针灸,口服营养补充剂,或者存在营养不良风险这给予肠内营养,同时进行口腔健康干预。推荐在临床试验环境中进行药物和神经刺激治疗。欧洲临床营养与代谢学会神经病学临床营养指南•存在营养不良风险的患者推荐口服营养补充剂。该指南指出,关于质地改良饮食和液体增稠对结局影响的数据不足。因此,只有在吞咽评估后,以及在监测液体平衡和营养摄入时,才推荐使用质地改良饮食和液体增稠。对于预期长期严重吞咽困难的患者,推荐采用早期肠内管饲。当肠内喂养超过28天时,推荐进行经皮内镜下胃造口置管。营养干预营养干预的目标是防止营养不良的负面影响。对于无法吞咽食物、饮品或药物的严重吞咽困难患者,有必要进行管饲,以确保摄入足够的蛋白质和热量。FOOD研究组由三项多中心随机对照试验组成,这些试验探讨了卒中患者的营养干预措施。在FOOD-2试验中,纳入了来自15个国家的859名卒中患者,与入院后超过7天的延迟管饲相比,早期管饲组的死亡减少了5.8%(p=0.09,未达显著性)。在许多患者中,无论是否立即开始进食,给药时通常都需要置入喂养管。然而,管饲并不能降低吸入性肺炎的发病率,因为吸入含口腔病原体的唾液也会造成吸入性肺炎。这种风险也反映在长期接受肠内营养的患者的高死亡率上。哪种热量方案最适合管饲患者尚存在争议。一项纳入了中国315名严重卒中患者的随机对照试验表明,与改良的全肠内方案(在该方案中,充足的热量摄入与促动力剂一起使用)相比,低热量肠内营养与死亡率增加有关。在两项试验(英国和伊朗)中,使用甲氧氯普胺或多潘立酮作为促动力药物降低了卒中后患者的肺炎发病率,尽管甲氧氯普胺的作用在大型欧洲PRECIOUS试验中没有得到证实(欧洲卒中组织会议,2023年5月)。在一项针对中国卒中后危重患者的回顾性观察性研究中,蛋白质摄入(而非热量摄入)与30天和6个月时的死亡率降低有关,这表明充足的蛋白质摄入可能特别重要。根据现有研究,是否以及何时通过鼻胃管或经皮内镜胃造口术(PEG)提供肠内营养,目前尚无最终回答。FOOD-3试验纳入了来自11个国家的321名参与者,发现早期接受PEG治疗的患者的死亡和不良功能结局的绝对风险比接受鼻胃管喂养的患者高7.8%(p=0.05)。不过,值得注意的是,在该研究162名接受PEG治疗的患者中,导管放置时间明显晚于159名接受鼻胃管喂养的患者。相比之下,Cochrane综述得出结论,鼻胃管喂养和PEG喂养与病死率和依赖性的差异无关;事实上,与鼻胃管喂养相比,PEG喂养与更少的治疗失败、更少的胃肠道出血和更高喂养输送有关。考虑到实用性,卒中后不立即进行更具有创性的PEG似乎是合理的,因为大多数患者的经口进食在30天内恢复。因此,如果在卒中的稳定期预计管饲时间超过28天,则应植入PEG,这得到了广泛共识。鉴于卒中后营养不良的危害,以口服补充剂的形式提供额外的能量是一种营养干预措施。FOOD-1试验在15个国家招募的4023名卒中患者,在未经筛选(就营养不良风险而言)的卒中后口服营养的患者中,补充口服营养对死亡率或功能结局没有获益。然而,在一些患者中,口服营养补充剂是有益的。一项针对日本454名卒中患者的前瞻性观察性研究,基于营养评估的个体化方法探讨了质地改变的饮食干预措施,包括口服能量和蛋白质补充。发现,这种方法与肌肉质量的增加、身体功能的改善和住院时间的缩短独立相关。一项在中国进行的173名卒中患者的随机对照试验评估了个体化营养支持,包括基于计算热量需求的个体化营养计划。经过干预后,干预组的身体成分比未接受干预组的身体成分的瘦体重和相位角更高,以及血清蛋白质、白蛋白和血红蛋白浓度水平更高。因此,研究结果表明,个体化的营养支持,包括监测热量摄入,可能会改善一些患者的营养状况。总之,现有数据表明,严重吞咽困难患者应考虑早期管饲并摄入足够的热量。如果管饲需要超过4周,应考虑放置PEG。此外,应密切监测和个体化管理热量摄入。只有在口服摄入足够安全的情况下,才应在一些有营养不良风险的患者中使用口服补充营养。口腔卫生吸入含口腔病原体污染的唾液是急性脑卒中患者发生吸入性肺炎的关键机制。根据这一机制,新西兰的一项研究进行PCR分析表明,脑卒中后口腔细菌(如大肠杆菌、肺炎克雷伯菌和铜绿假单胞菌)的浓度增加,出院时的总细菌水平(用qPCR测量的)与肺炎有关。相反,口腔卫生干预的目的是减少口腔病原体的定植。在一项对中国84名患者进行的随机对照试验中,强化口腔卫生项目包括每天用氯己定刷牙和口腔软组织3次,肺炎的发病率从32%下降到14%(p=0.052)。在一项纳入了2771名日本急性卒中患者的回顾性观察性研究中,与没有系统性口腔护理的时期相比,实施系统性口腔护理与肺炎显著减少有关。在不同的护理时期(不同程度的强化牙科护理),肺炎减少的比值比从0.24到0.49不等。然而,其他较老的试验报告称,要么没有统计学上显著的效果,要么改善了口腔卫生但对呼吸道并发症没有影响。一项纳入了口腔卫生干预研究的荟萃分析,发现降低了肺炎发生率(p=0.06),口腔健康结局也有所改善。因此,对于卒中后吞咽困难的患者,应在现有护理能力范围内尽可能优化口腔卫生。行为疗法行为练习和动作是吞咽困难患者最广泛使用的治疗方法,言语和语言治疗师可以使用几种不同的操作方法。补偿操作是在吞咽过程中改变身体和头部的位置,优化生理吞咽过程和食团流量,以实现即时改善。康复吞咽练习是指通过肌肉训练或优化吞咽机制以达到长期的效果。然而,许多行为操作同时具有短期补偿效果和长期疗效,这取决于练习项目中的管理。一些研究采用个性化方法探讨了行为吞咽困难疗法的疗效。一项针对台湾2994名卒中患者的回顾性研究,研究者采用倾向评分匹配,发现吞咽治疗与降低肺炎发病率和提高长期生存率之间存在关联。在接受吞咽治疗的患者中,持续治疗超过1个月与肺炎发病率下降有关,这表明吞咽治疗存在强度依赖性效应。一项对澳大利亚306名卒中患者进行的较老但高质量的随机对照试验,比较了常规吞咽困难治疗、标准低强度吞咽治疗(吞咽补偿策略和饮食调整)和标准高强度吞咽治疗(高频直接吞咽练习和饮食调整)。在标准吞咽治疗组中,胸部感染、死亡或住院在统计学上显著减少。高强度组也显示,恢复正常饮食或恢复吞咽功能的患者比例更高。在一项Cochrane荟萃分析中,40种不同的行为干预措施与吞咽能力的提高有关,并降低了卒中后吞咽困难患者的比例。一些研究评估了特定动作或练习方案的效果。其中一项技术是改良低头吞咽动作(chin-tuckmanoeuvre)。在最初低头吞咽动作中,低头将下巴抵向胸部。这个动作通过改变姿势进而改善了吞咽机制。这项技术已被修改为对抗阻力的长期效果练习方案。一项纳入了八项随机对照试验的荟萃分析发现,与对照干预措施相比,低头抵抗阻力(chin-tuckagainstresistance)可提高吞咽的安全性(五项研究)和经口摄入量(三项研究)。在一项亚组分析中,低头抵抗阻力干预在提高吞咽安全性方面比Shaker练习(四项研究)更有效,Shaker练习一项抬头训练方法,可以抬高喉部和保持上食道括约肌开放。在一项针对韩国32名卒中患者的随机对照试验中,研究人员发现,与传统吞咽困难治疗组相比,Shaker练习可以改善Penetration-AspirationScale和功能性经口摄食。最后,加强口腔、面部或呼吸肌肉的练习方案。一项针对瑞典19名卒中患者的试验探讨了口腔神经肌肉训练的作用,发现其对吞咽速率和嘴唇力量有积极影响;然而,在视频荧光镜吞咽检查(VideofluoroscopicSwallowingStudy)的分析中没有发现统计学上的显著差异。一项纳入了韩国35名卒中患者的研究利用视频荧光镜吞咽检查比较了舌-腭阻力训练与传统疗法的作用,发现可以改善舌肌力量和口咽参数。另一项针对美国19名卒中患者的试验报告称,设备辅助舌训练可以增加功能口腔摄入。在另一项随机对照试验中,对韩国29名卒中患者进行了阻力张口训练(resistivejawopening),发现干预组的饮料渗透(penetrations)和吸入减少,但干预组和对照组之间没有统计学上的显著差异。吸气和呼气肌肉训练可以改善咳嗽反射和吞咽功能。在一项针对西班牙109名卒中患者的研究中,吸气和呼气肌肉训练能够增强肌肉力量,减少呼吸道并发症。一项针对韩国27名患者的研究表明,呼气肌肉力量训练有助于减少液体的渗透和吸入,并提高经口摄入量。同样,一项纳入了11项随机对照试验的荟萃分析得出结论,呼吸肌训练降低了呼吸并发症的风险,并减少了具有一定粘稠度饮料的渗透和吸入。吞咽障碍的肌电图或视觉生物反馈可视化治疗仪可优化吞咽机制或增加吞咽肌肉的肌电振幅。此外,各种荟萃分析表明针灸具有积极的治疗效果。然而,尽管进行了几项大型研究,但由于方法学的异质性,缺乏高质量的方法学,以及针灸治疗的机制尚不清楚,所以针灸治疗的证据水平质量较低。总之,有几种方案可用于行为吞咽困难的治疗。简单易行的练习方案可以改善卒中后的吞咽困难,包括低头阻抗(chin-tuckagainstresistance)、shaker练习和呼气肌肉力量训练(图1)。行为治疗应基于个体化的吞咽困难模式,并在治疗过程中根据具体情况评估其有效性。图1:卒中后吞咽困难的行为吞咽练习。(A)shaker练习,患者平躺在地板上,使用舌骨上和舌骨下肌群抬头1分钟。Thisexerciseisrepeated3timesfor1min,following30headlifts,3timesadayfor6weeks。(B)低头阻抗练习(Chin-tuckagainstresistance),即低头对抗阻力(即放置在下巴下方的物体),涉及到舌骨上肌群和舌骨下肌群。每节课必须重复此练习几次。(C)呼气肌力量训练(Expiratory-Muscle-Strength-Training,EMST),需要咽肌群参与,将空气吹入具有阻抗的设备。每节课必须重复多次此练习:药物治疗尽管发现了有希望的结果,但由于荟萃分析缺乏明确证据,药物治疗仅能在研究环境中使用。药物治疗包括在外周感觉水平或中枢神经系统水平对吞咽具有神经调节作用的药物。辣椒素是一种作用于外周的吞咽困难治疗药物,是一种药物感觉刺激的方法。辣椒素是TRPV-1受体的激动剂,并介导神经肽物质P从感觉神经末梢的释放。在自然界中,辣椒素存在于辣椒中,产生辛辣的味道。在一项针对中国92名卒中患者的随机对照试验中,对辣椒素联合冰块与单独冰块刺激进行了比较。冰刺激包括使用冰刷刺激特定区域,包括软腭、腭弓、咽后壁和舌头后部。每天两次,在午餐和晚餐前进行。通过咽水试验和临床吞咽评估,发现干预组的吞咽困难有了更大的改善。此外,与对照组相比,干预组的血清物质-P浓度更高。另一项针对60名患者的随机对照试验也在中国进行,研究了辣椒素联合触觉热刺激的作用。触觉热刺激是指使用棉签将4°C溶液涂抹在口咽粘膜上。在这项研究中,通过问卷调查和咽水试验发现,干预组的吞咽功能比对照组改善更明显。另一项纳入了中国53名出血性卒中患者的随机对照试验发现,使用辣椒素溶液雾化方案可以改善咳嗽功能和减少咽部残留。相比之下,在纳入了36名西班牙卒中后吞咽困难患者的研究中,给予辣椒素后立即使用视频荧光透视吞咽检查评估吞咽情况,未检测到其对吞咽生理功能的影响,但研究人员发现增强了运动皮层的兴奋性。除了辣椒素外,胡椒碱和薄荷醇也能刺激TRPV-1受体或功能相似的受体,能够改善不同病因吞咽困难患者的吞咽功能。其他种类的药物也正在研究中,结果不具结论性,包括血管紧张素转换酶(ACE)抑制剂,它可以抑制P物质的降解并使咳嗽反射敏感(ACE抑制剂的已知副作用),还有多巴胺能药物,它可以缩短吞咽反应的潜伏期。神经刺激为了诱导吞咽网络神经可塑性的变化,已经开发了不同的外周和中枢神经刺激方法(procedures)。这些变化可能会改善卒中后的吞咽功能(Panel2)。Panel2.神经刺激的方法:无创脑刺激•经颅直流电刺激(Transcranialdirectcurrentstimulation,tDCS)和重复经颅磁刺激(repetitivetranscranialmagneticstimulation,rTMS)是无创的脑刺激方法。•tDCS,通过电极,电流施加在颅骨上,可逆地影响皮层的兴奋性。具体效果取决于电极放置的极性。阳极刺激增加皮层兴奋性,阴极刺激降低皮层兴奋性。•rTMS,放置在头皮上的线圈产生磁场。不同频率的磁场具有促进或降低皮层兴奋性的作用。高频rTMS(如>5Hz)通常会增强皮层活动,而低频rTMS则会降低皮层活动。•除了用于吞咽困难康复外,这些方法还用于调节各种神经和精神疾病中的大脑活动。口咽外周刺激方法•咽部电刺激(Pharyngealelectricalstimulation,PES)和神经肌肉电刺激(neuromuscularelectricalstimulation,NMES)是对咽部和吞咽肌肉的外周刺激。•PES,通过导管,电流施加到咽下部的粘膜,进行感觉刺激。•NMES应用于颈部区域,通过经皮刺激轴突运动或感觉神经末梢和肌肉纤维来激活参与吞咽功能的神经或肌肉。•尽管外周神经刺激方法的确切机制尚未完全阐明,但据信这些技术可能对整个吞咽网络产生次级(secondary)调节作用。鉴于需要进一步的临床验证和新证据的出现,建议在临床试验环境中优先使用这些神经刺激方法。经颅直流电刺激各种荟萃分析探讨过经颅直流电刺激(Transcranialdirectcurrentstimulation,tDCS)对脑卒中吞咽康复的疗效,这些分析表明tDCS对吞咽功能有积极作用。在亚组分析中,发现不同刺激部位的疗效存在差异。在一项荟萃分析中,发现同侧、对侧或双侧阳极(兴奋性)刺激有积极作用,只是对侧受到刺激时的效果比同侧受到刺激更大。在另一项荟萃分析中,发现只有对侧兴奋性刺激才能改善吞咽困难。相比之下,一项荟萃分析得出结论,同侧刺激比对侧刺激的效果更明显。还有荟萃分析没有发现差异。个别研究表明,tDCS对脑干卒中患者的吞咽困难也有积极影响。这些患者吞咽功能的改善可能是通过促进皮层神经可塑性介导的。重复经颅磁刺激各种荟萃分析得出结论,重复性经颅磁刺激(repetitivetranscranialmagneticstimulation,rTMS)可以改善吞咽功能。在亚组分析中,报告了刺激特定位置或卒中所在半球的疗效没有差异,或与对侧刺激相比同侧高频刺激的疗效更大。此外,随机对照试验的结果表明,小脑刺激也可以改善吞咽困难,rTMS的治疗效果可能受到皮质球束结构完整性的调节。神经肌肉电刺激一些荟萃分析表明,神经肌肉电刺激对吞咽功能有治疗作用。一项针对韩国31名卒中患者的研究调查了不同的电极放置方案。结果表明,与垂直放置电极相比,水平放置在舌骨上和舌骨下肌肉上的电极获得了最佳的治疗效果。在一项针对26名韩国患者的研究中,与舌骨下电极放置相比,舌骨上患者的渗透和吸入更少。在另一项纳入了40名患者的韩国试验中,通过视频荧光镜吞咽检查进行评估,接受咬肌和舌骨上肌肉刺激的组与单独接受舌骨上肌刺激的组之间的总体吞咽困难严重程度没有差异。咽部电刺激一项纳入了六项随机对照试验的荟萃分析显示,咽部电刺激可改善吞咽功能,并可增加拔除鼻饲管的比例。另一项荟萃分析纳入了五项研究,发现咽部电刺激对吞咽功能产生了积极影响,只是差一点才能达到统计学显著性阈值。尽管如此,来自两项研究针对气管切开患者的数据显示,咽部电刺激有利于拔除气管切开套管。另外两项荟萃分析(每项分析都有两项研究中的数据)没有确定咽部电刺激的治疗效果(未考虑拔除气管套管)。相反,纳入了八项评估气管切开和非气管切开患者的研究的荟萃分析,报告了咽部电刺激对吞咽困难的统计学显著改善,而拔管成功被认为是一种治疗效果。因此,在评估咽部电刺激的治疗效果时,区分危重气管切开患者和病情较轻的非气管切开患者至关重要。根据这一发现,一项纳入了卒中后气管切开的欧洲多中心随机对照试验显示干预组的拔管率(达到49%)高于对照组(9%),具有统计学意义。在另一项德国试验中,纳入了60名卒中患者,这些患者在拔管后4小时内接受刺激治疗,与假刺激相比,咽部电刺激与拔管后吞咽困难的改善、肺炎发病率的降低、出院时管饲需求的减少以及住院时间的缩短有关。总之,许多随机对照试验研究了神经刺激的方法,表明其对吞咽功能有积极影响。对其他重要结局参数的影响,如吸入性肺炎、管饲或死亡率,很少报道。此外,哪种方法最适合哪些患者群体,仍然是一个问题。两项比较不同神经刺激方法效果的荟萃分析得出结论,rTMS对吞咽功能的影响最大,排在神经肌肉电刺激和tDCS前面,而对咽部电刺激没有显示出统计学上的显著影响。与这一发现一致,另一项侧重于tDCS和rTMS的荟萃分析显示rTMS治疗效果最好。一项荟萃分析还显示rTMS的效果最好,其次是咽部电刺激和tDCS,而没有分析神经肌肉电刺激。咽部电刺激疗效差异的一个原因是,除了关注吞咽评分外,后一项meta分析还将拔除气切套管作为结局参数。在同一荟萃分析中,根据刺激定位调查了无创脑刺激的效果。双侧刺激效果最大。对于单侧刺激,tDCS和rTMS的结果是不同的,rTMS对同侧的影响更大,而tDCS仅对对侧的影响具有统计学意义。一项针对土耳其40名卒中患者的试验表明,rTMS联合神经肌肉电刺激可以产生额外的积极治疗反应。产生部分矛盾结果的原因可能是由于研究方案的刺激频率、部位、刺激目标、持续时间和重复次数的差异,以及研究队列的不同造成的。此外,作为吞咽困难的恢复机制,补偿性神经可塑性存在不同的理论模型甚至部分矛盾的理论模型,所以才发展了不同的刺激方案(图2)。由于部分数据相互矛盾,需要进一步研究。图2:单侧卒中后吞咽困难恢复的假设模型及其相应的无创脑刺激方案。在健康的大脑中,吞咽的大脑活动位于感觉运动皮层和小脑的两侧(从绿色到黄色的彩色区域,活性逐渐增加)。在对侧代偿模型中,单侧卒中后吞咽网络被破坏(红色同心圆)。根据该模型,吞咽功能的恢复基本上是由对侧半球的神经可塑性驱动的。因此,兴奋性对侧刺激可促进吞咽困难的康复。在半球间抑制模型中,对侧半球对同侧半球施加抑制。因此,根据该模型,对侧半球的抑制性刺激或同侧半球的兴奋性刺激可以促进吞咽困难的恢复。在神经机能联系不能模型中,随着整个网络的崩溃,卒中病变会导致吞咽网络的广泛崩溃。根据该模型,在这些情况下,双侧兴奋性刺激或小脑的兴奋性刺激可以促进吞咽网络的恢复:从实用的角度来看,并考虑到各种方法在方法学上的优缺点,可以进一步得出其适用于某些患者的结论:咽部电刺激特别适用于卒中、咽感觉减退和吞咽反射延迟的气管切开患者。TDCS和神经肌肉电刺激可以作为行为干预的辅助治疗方法。相比之下,rTMS作为行为干预的辅助手段,在技术上要求很高,通常需要转运到专门的设施中。因此,它可以考虑用于病情严重但稳定的患者。结论和展望吞咽困难在卒中患者中非常普遍,并可能与严重并发症有关。卒中后吞咽困难的早期治疗对于降低死亡率和提高患者的生活质量至关重要。有各种基本疗法可供选择,应大规模应用(在所有环境中)。此外,还有一些疗效证据越来越多的附加疗法需要进一步探索,特别是在临床试验环境中。在治疗上,既定的基本干预措施主要旨在避免吞咽困难的并发症,而不是针对吞咽功能本身。其中一些干预措施旨在改善口腔健康,减少口腔中呼吸道病原体的负荷。调整食团稠度的饮食干预以吞咽安全为目标,旨在防止误吸,并用于早期吞咽训练。监测营养状况和补充剂或经口或肠内营养可以预防营养不良。此外,有几种行为治疗练习方法具有补偿机制,或旨在长期改善吞咽功能。已经开发了触发和促进神经可塑性的不同刺激方法。这些方法包括直接脑刺激,如tDCS或rTMS,也包括外周刺激干预,如神经肌肉或咽部电刺激。几项研究显示了有希望的结果,有证据表明这些方法可以改善吞咽功能。然而,探索这些方法对其他临床结局(如肺炎、功能性结果或死亡率)的高质量研究很少。除了神经刺激外,药物(尤其是辣椒素)也显示出了有希望的结果,表明药理学感觉刺激促进了吞咽功能或咳嗽的改善。图3显示了根据卒中入院时间量身定制的吞咽困难治疗的关键管理选项。图3.吞咽困难的全面管理。由于疾病早期并发症率很高,在吞咽困难的急性期以预防并发症为主的保护措施占主导地位。由于患者可能会从吞咽困难中恢复,因此应通过鼻胃管提供肠道营养。在急性期后和慢性期,应使用所有吞咽困难疗法,包括改善吞咽功能恢复的措施。慢性吞咽困难患者的肠道营养可以通过PEG提供。在慢性期应谨慎使用饮食措施,因为长期使用有副作用的风险。PEG=经皮内镜胃造口术:对于吞咽困难康复,吞咽网络的部位、方向性和半球协调性尚不完全清楚。知识的缺乏限制了神经调控程序的优化,产生了各种刺激方案,所以引起研究结果的不一致。此外,谁可以或应该进行这些干预也缺乏数据,担心风险,比如tDCS和rTMS诱导癫痫发作,监管障碍和制药行业缺乏兴趣,这些因素阻碍了进一步的发展。然而,从机制的角度来看,考虑到吞咽的双中心特征,神经可塑性介导的康复潜力特别高。更详细地了解吞咽困难康复中的中枢控制和神经可塑性将推动神经刺激的进一步改进。为此,临床联合神经影像学研究将是至关重要的。此外,基于证据的疗法进入到临床实践中,是至关重要的。在这种情况下,越来越多的仪器诊断使临床医生能够描述吞咽困难患者的表现,从而深入了解吞咽障碍的机制模式。值得注意的是,与幕上梗死患者相比,在延髓卒中患者中观察到的吞咽困难通常表现为梨状窦中聚集性残留物。这种独特的特征可能归因于食道上括约肌的过度收缩所致。对于具有这种特殊病因的患者,采取针对性的干预措施(例如手术干预措施),比如减轻食道上括约肌的高收缩性可以带来临床益处。除了描述吞咽困难的表现外,未来可能会对吞咽困难的个体原因进行更详细的探索。这种细致入微的探索将对制定适当的治疗干预措施发挥关键作用。因此,年龄相关的吞咽功能变化可能发生在吞咽困难之前。因此,肌肉减少和吞咽肌量减少已被确定为卒中后吞咽困难的关键机制。具体而言,对于卒中后7天以上发生的延迟吞咽困难,肌肉减少可能是主要的吞咽困难机制。对于因肌肉减少所致吞咽困难,全身肌肉计划可能对吞咽困难康复有效,正如日本一项对148名患者的回顾性研究所表明的那样,该研究发现改善食物摄入水平与椅子站立练习的频率之间存在关联。因此,未来的研究应该考虑到吞咽困难的原因和机制,促进个性化治疗。加强吞咽困难治疗,减少并发症,降低死亡率,提高大多数患者的生活质量。文献出处:LancetNeurol.2024Apr;23(4):418-428.doi:10.1016/S1474-4422(24)00053-X.Dysphagiaafterstroke:researchadvancesintreatmentinterventions
 杨中华 主任医师 北京天坛医院 神经病学中心421人已读
杨中华 主任医师 北京天坛医院 神经病学中心421人已读 - 脑梗塞 闭锁综合征的预后
经典的闭锁综合征(locked-insyndrome,LIS)通常是由脑桥腹侧卒中引起的,表现为四肢瘫痪、缄默症、意识完整,仅能依靠眼球垂直凝视和/或眨眼进行沟通。LIS的临床表现和定义各不相同,尤其是对于不完全LIS。2023年9月来自瑞典的FrankBecker等在Neurology上公布了他们的研究结果,探讨了LIS的功能多样性、预后及其过程的复杂性,以及病变位置的差异及其对预后的价值。根据LIS的功能定义,对一组持续>=6周LIS状态的血管性LIS患者进行了研究。研究数据来自于挪威国家闭锁综合征康复中心的质量登记,收集2012年至2022年间人口统计学数据、药物和随访数据。样本包括了51名患者(中位年龄:55.7岁,36名男性),其中43人有随访数据。缺血性卒中是最常见的病因(n=35)。23名患者从LIS状态恢复过来(非-LIS定义为不再满足LIS标准[挪威国家闭锁综合征康复中心的定义]的>=一条:1.交流的主要形式为语言交流,和/或2.无辅助步行的下肢运动功能,和/或3.ADL时部分独立的上肢运动功能,和/或没有时间、地点和环境的定向力障碍),大多发生在发病2年内。除1名患者外,所有患者的运动都有所改善,而只有3名患者的运动完全恢复,88%的患者长期高度依赖。3年生存率为87%。5名患者为孤立性脑桥病变,而80%的患者在脑干外有各种病变。在从LIS状态恢复过来的患者中,脑干外病变的发生率明显低于仍处于LIS状态的患者。最终作者认为,对未经筛选的血管性LIS患者的人群样本进行调查,为了解LIS的功能多样性提供了重要的见解。尽管大多数患者仍然严重残疾,但即使是功能的小幅改善也可以大大增加活动和参与的潜力。脑干外的其他病变在长期LIS中很常见,这可能是遗留LIS状态的预后因素。文献出处:Neurology.2023Sep5;101(10):e1025-e1035.doi:10.1212/WNL.0000000000207577.Epub2023Jul13.Demographic,Medical,andClinicalCharacteristicsofaPopulation-BasedSampleofPatientsWithLong-lastingLocked-InSyndrome
杨中华 主任医师 北京天坛医院 神经病学中心189人已读 - 颅内动脉瘤 伴未破裂动脉瘤的高血压,首先钙离子拮抗剂?
高达45%-60%的颅内动脉瘤患者患有高血压。高血压是未破裂颅内动脉瘤(UIAs)生长或破裂的危险因素。高血压患者,尤其是那些未控制的高血压患者,UIA生长或破裂的风险更高。抗高血压治疗可以防止UIA生长和破裂。钙通道阻滞剂(CCBs)是临床上常用的降压药;它们可以降低血压和血压变异性。此外,CCBs还通过调节平滑肌和内皮功能具有血管保护作用,例如,抑制血管壁炎症,上调内皮一氧化氮合酶和其他血管保护因子的表达,以及预防内皮功能障碍和血管重塑过程,正如一些体外和体内研究所揭示的那样。尽管先前有报道CCBs具有防止UIA生长或破裂的作用,但很少的临床研究数据用于验证其疗效。2023年9月来自南京医科大学的ShuoWang等在JNS上公布了他们的研究结果,目的在于探讨CCB是否与高血压患者未破裂颅内动脉瘤(UIA)不稳定(生长和破裂)的发生率较低有关。本研究对象为两项前瞻性多中心队列研究(IARP-CP和100-Projectcohorts)中的UIA患者。所有患者均接受保守治疗,每6个月定期进行CT血管造影术随访2年。每周至少服用5天CCB的患者被认定为CCB使用者;否则,为非CCB使用者。主要终点是UIA不稳定(破裂、生长>20%和/或1mm,或在影像学随访中发现新的穹顶不规则)。共纳入392名UIA高血压患者(191名男性,201名女性;中位年龄57岁),平均随访时间为21.7±5.2个月。在随访过程中,81名患者(20.7%)达到了主要终点,其中68名患者发现动脉瘤生长,13名患者动脉瘤破裂。CCB使用者的UIA不稳定性发生率低于非CCB使用者(27/237[11.4%]vs54/155[34.8%],p<0.001)。多变量Cox分析表明,使用CCB与UIA不稳定的风险较低有关(HR0.37,95%CI0.22-0.61;p<0.001)。在服用单一降压药的患者(HR0.22,95%CI0.12–0.40;p<0.001)和服用>1种降压药的患者(HR0.42,95%CI0.20–0.87;p=0.021)中,CCB的保护作用是一致的。对于高血压被控制的患者,CCB仍然与UIA不稳定的风险较低有关(HR0.22,95%CI0.09–0.52;p=0.001)。最终作者认为,在患有高血压的UIA患者中,使用CCB可降低动脉瘤不稳定的发生率。文献出处:JNeurosurg.2023Jan27;139(3):651-660.doi:10.3171/2022.12.JNS222428.Print2023Sep1.Associationofcalciumchannelblockerswithlowerincidenceofintracranialaneurysmruptureandgrowthinhypertensivepatients
杨中华 主任医师 北京天坛医院 神经病学中心50人已读 - 脑出血 脑出血患者应该就近救治!
脑出血(ICH)约占所有卒中的15%,是死亡率、发病率和经济影响最高的卒中亚型。不幸的是,没有任何特定的治疗方法被证明是绝对有效的。在ICH毁灭性的临床病程中,早期神经系统恶化起着重要作用,主要是由于血肿扩大,受累患者达到30%,大多数发生在最初的3小时内。血压高度变异性、体温、心率和血糖与更差的ICH结局、高死亡率有关,同样还有呕吐、感染性并发症和癫痫。研究发现,逆转抗凝、积极降压和入住重症监护可降低30天的死亡率。考虑到脑出血的快速和毁灭性过程,院前转院方案可能在脑出血患者的功能结局和死亡率中发挥重要作用。2023年10月来自西班牙的YolandaSilva等在JAMANeurology上公布了RACECAT随机对照试验的二次分析结果,目的在于比较脑出血患者直接送至血管内治疗(EVT)卒中中心与送至最近的当地卒中中心的效果。这是对RACECAT试验预先指定的二次分析,RACECAT试验是一项多中心、基于人群的簇随机临床试验,于2017年3月至2020年6月在西班牙加泰罗尼亚进行。患者盲法评价终点。随机分为直接转运到具有EVT能力的卒中中心或最近的当地卒中中心。所有被怀疑大血管闭塞性卒中(RACE评分>4)并最终诊断为脑出血的连续患者均被纳入。共有1401名患者因怀疑大血管闭塞性卒中被纳入RACECAT试验。目前的分析是在2022年10月进行的。主要结果使用累积顺序逻辑回归进行测试,以估计90天时残(mRS)shift分析的共同优势比(OR)和95%CI。次要结局,包括90天死亡率、死亡或严重功能依赖性、早期神经系统恶化、早期死亡率、脑出血量和扩大、神经外科治疗率、初次转运期间的临床并发症率以及直到第5天的不良事件率。在1401名入选患者中,1099名被排除在该分析之外(32名拒绝知情同意,920名患有缺血性卒中,29名患有短暂性脑缺血发作,12名患有蛛网膜下腔出血,106名患有卒中mimic)。因此,共纳入了302名患者(204名[67.5%]男性;平均[SD]年龄71.7[12.8]岁;中位[IQR]RACE评分7[6-8])。对于主要结局指标,与转运到最近的局部卒中中心相比,直接转运到具有EVT功能的卒中中心的90天功能结局更差(调整后的cOR,0.63;95%CI,0.41-0.96)。与转运到最近的当地卒中中心相比,直接转运到具有EVT能力卒中中心的90天死亡率更高(48.9%vs37.6%;调整后的危险比为1.40;95%置信区间为0.99-1.99)。对于直接转运到具有EVT能力卒中中心的患者,最初转运期间的内科并发症发生率(22.6%vs5.6%;调整的OR为5.29;95%置信度为2.38-11.73)和院内肺炎发生率(35.8%vs17.6%;OR为2.61;95%可信区间为1.53-4.44)更高。最终作者认为,在RACECAT随机临床试验的二次分析中,绕过最近的卒中中心而直接转运到具有EVT能力的卒中中心,降低最终诊断为脑出血患者的90天时功能独立的机会。文献出处:JAMANeurol.2023Oct1;80(10):1028-1036.doi:10.1001/jamaneurol.2023.2754.EffectofBypassingtheClosestStrokeCenterinPatientswithIntracerebralHemorrhage:ASecondaryAnalysisoftheRACECATRandomizedClinicalTrial
杨中华 主任医师 北京天坛医院 神经病学中心212人已读 - 学术前沿 搏动性耳鸣的病因是什么?治疗效果如何?
搏动性耳鸣(Pulsatiletinnitus,PT)是指在没有体外原因的情况下,主管感觉到与脉搏同步的声音,从轻微不适的间断感觉到让人倦怠的持续感觉。PT也可能提示存在危及生命的疾病,如硬脑膜动静脉瘘(dAVFs)或严重的动脉狭窄。不同研究报告的PT病因比例差异很大,最常见的原因包括动脉狭窄、正常解剖变异,或高度血管化的肿瘤。这些差异可能是由于不同的转诊模式和评估方法造成的。因此,PT病因的频率仍然是一个悬而未决的问题。为此,2023年10月来自美国的MatthewRAmans等在JNIS上公布了他们的数据。本研究的数据来自于一个学术中心多学科PT诊所的连续患者。根据临床和/或无创影像,通过血管内技术(动脉造影、静脉造影、测压和/或球囊试验闭塞)评估的疑似脑血管病因的PT患者进行分析。比较PT的基线临床特征和最终病因的治疗结果。在552名接受PT评估的患者中,纳入了164名(29.7%)接受了PT血管内评估的患者。首次临床评估时的平均(±SD)年龄为54.3±14.1岁(范围为25-89岁);111例(67.7%)为女性。PT的病因为血管性占75.6%,非血管性占24.4%。动静脉分流病变占20.7%,静脉病因占48.2%,动脉病因占6.7%。在接受血管内栓塞治疗的分流病变患者中,96.9%的患者PT持续显著改善或消退。在血管内支架治疗的静脉窦狭窄的患者中,84.6%的患者PT持续改善或消退。动脉和非血管PT的血管内治疗患者较少,PT症状改善不明显。最终作者认为疑似血管原因的PT通常是因为静脉的原因引起的。对于动静脉分流或静脉窦狭窄引起的PT,血管内治疗是有效的。文献出处:JNeurointervSurg.2023Oct;15(10):1014-1020.doi:10.1136/jnis-2022-019259.Epub2022Sep8.Cerebrovascularpulsatiletinnitus:causes,treatments,andoutcomesin164patientswithneuroangiographiccorrelation
杨中华 主任医师 北京天坛医院 神经病学中心208人已读 - 蛛网膜下腔出血 不良分级动脉瘤蛛网膜下腔出血患者的预后并不太差,要有信心!
关于不良分级动脉瘤性蛛网膜下腔出血(aSAH)幸存者的生活质量(qualityoflife,QoL)的数据很少。尽管与高死亡率和不良结局相关,但近年来,不良分级aSAH幸存者的比例有所增加。除了医生报告的结局外,患者报告的生活质量也越来越重要,因为它反映了患者对个人健康的主观看法。这在不良分级aSAH患者尤为重要,因为幸存者必须应对神经系统缺损带来的危害。不良分级aSAH与良好分级aSAH患者往往被混合在一起进行分析,引起不良分级患者的生活质量的研究存在代表性不足的问题。2023年5月来自瑞士的JohannesGoldberg等在Neurosurgery公布了不良分级aSAH幸存者的前瞻性生活质量数据,以帮助制订临床决策和向家属交代病情。WFNS脑疝量表研究是一项前瞻性多中心观察性研究,研究对象为不良分级aSAH(WFNS4级和5级)的患者。通过电话随访发病6个月和12个月的数据。使用EuroQoL-5维度-3水平(EuroQoL-5Dimensions-3Levels,EQ-5D-3L)问卷调查患者的生活质量,0代表相当于死亡的健康状态,1表示完全健康。采用mRS评分评价良好和不良结局。共纳入了250名患者,其中237名患者在6个月后纳入分析,223名患者在12个月后纳入分析。6个月后,118名(49.8%)患者存活,12个月后104名(46.6%)患者存活。其中,95例(80.5%)和89例(85.6%)患者预后良好,平均EQ-5D-3L指数分别为0.85(±0.18)和0.86(±0.18)。6个月和12个月后,23例(19.5%)和15例(14.4%)患者预后不良,平均EQ-54D-3L指数分别为0.27(±0.25)和0.19(±0.14)。最终作者认为,尽管最初死亡率很高,但生活质量良好的不良分级aSAH幸存者占比相当大。只有少数幸存者报告生活质量差,需要长期照顾。文献出处:Neurosurgery.2023May1;92(5):1052-1057.doi:10.1227/neu.0000000000002332.Epub2023Jan4.QualityofLifeAfterPoor-GradeAneurysmalSubarachnoidHemorrhage
杨中华 主任医师 北京天坛医院 神经病学中心59人已读 - 颅内动脉瘤 蛛网膜下腔出血家族史的个体,筛查颅内动脉瘤的意义
个体的一级亲属中>=2人发生过动脉瘤性蛛网膜下腔出血(aSAH),该个体发生aSAH的风险增加,终生风险高达25%。模型研究表明,对于20岁至70岁至80岁之间的这些个体,每5至7年进行一次预防性颅内动脉瘤筛查具有成本效益。初次筛查时发现颅内动脉瘤的绝对风险约为11%,以后筛查发现新颅内动脉瘤的几率约为7%。因此,大多数接受筛查的个体都没有动脉瘤。后续筛查中检测到新动脉瘤的危险因素可能有助于确定新动脉瘤发生几率较小或较高的亚组。从而可以提高筛查的功效。2023年4月来自荷兰的YnteM.Ruigrok等在Stroke上公布了他们的研究结果,目的是开发一个模型,用于预测具有严重急性蛛网膜下腔出血阳性家族史的个体在初次筛查后检测出新颅内动脉瘤的概率。从一项前瞻性研究中,获得了499名受试者的动脉瘤随访筛查数据,这些受试者具有aSAH阳性家族史,定义为≥2名一级亲属患有aSAH或一个一级亲属患有aSAH,>=1个一级亲属患有未破裂动脉瘤。由荷兰乌得勒支大学医学中心和法国南特大学医院进行筛查。在5050人-年的随访中,52名受试者发现了颅内动脉瘤。随访5年时发生动脉瘤的风险为2%至12%,10年时为4%至28%,15年时为7%至40%。预测因素为女性、颅内动脉瘤/aSAH病史以及年龄较大。5年时评分(包括性别、既往颅内动脉瘤/aSAH病史、年龄较大)的Cstatistic值为0.70(95%CI,0.61–0.78),10年时为0.71(95%CI,0.64–0.78),15年为0.70(95%CI,0.63–0.76)。最终作者认为该评分(性别、既往颅内动脉瘤/aSAH病史、年龄较大)提供了初次筛查5年、10年和15年后检测到新颅内动脉瘤的估计风险;对于有aSAH阳性家族史的个体,这个数据有助于制订个体化的筛查策略。文献出处:Stroke.2023Apr;54(4):1015-1020.doi:10.1161/STROKEAHA.122.041393.Epub2023Feb27.RiskPredictionofNewIntracranialAneurysmsatFollow-UpScreeninginPeopleWithaPositiveFamilyHistor
杨中华 主任医师 北京天坛医院 神经病学中心55人已读 - 脑血管畸形 脑海绵状血管畸形女性避免服用女性激素
脑海绵状血管畸形(CCM)可以引起痫性发作和卒中(颅内出血或非出血性局灶性神经缺损)。CCM引起的出血性卒中的原因,可能是缓慢的CCM血流造成扩张的窦状血管内血栓形成所致。颅内出血5年的估计风险各不相同,未经治疗者的发生率为4%-31%。脑干CCM和既往颅内出血的患者风险最高。女性激素治疗包括育龄女性口服避孕和绝经后更年期激素替代治疗。女性激素治疗已被证明会增加卒中和静脉血栓形成的风险。然而,很少有数据表明女性激素治疗对CCM患者颅内出血风险的影响,因此指南无法提出建议。一个病例报道提示女性激素治疗会增加CCM颅内出血的风险,一项观察性研究发现雌激素治疗增加CCM女性脑出血的可能性。但是,目前尚缺乏前瞻性,大型队列研究的数据。2023年4月来自美国和德国的专家在Neurology上公布了他们的研究结果,他们利用两项大型前瞻性、多中心、观察性队列研究的数据,调查了女性激素治疗与女性CCM颅内出血之间的关系。纳入了连续的CCM患者。在多变量Cox比例风险回归中,比较了长达5年的前瞻性随访中使用女性激素治疗与CCM发生颅内出血之间的相关性。并进行了系统性综述。共722名女性患者,诊断CCM时的年龄在10岁或以上,在随访期间的任何时候137例使用了女性激素治疗。未使用女性激素治疗的平均年龄为44岁,使用女性激素治疗的平均年龄为33.5岁。女性激素治疗(根据年龄、症状[modeofpresentation]和CCM位置进行调整)与随后颅内出血的风险增加有关(46/137[33.6%]vs91/585[15.6%],调整后的危险比为1.56,95%CI为1.09-2.24;p=0.015)。经调整相同的因素后,10-44岁女性患者使用口服避孕药与随后较高的颅内出血风险有关(调整后的危险比2.00,95%CI1.26-3.17;p=0.003)。系统文献检索显示,没有研究报告女性激素治疗对随访期间颅内出血风险的影响。最终作者认为,使用女性激素治疗与CCMs较高的颅内出血风险有关。这些发现对临床实践中CCM患者给予女性激素治疗的安全性提出了质疑。进一步评估增加血栓形成风险临床因素的研究可能有助于确定哪些患者最容易发生颅内出血。文献出处:Neurology.2023Apr18;100(16):e1673-e1679.doi:10.1212/WNL.0000000000206888.Epub2023Feb8.FemaleHormoneTherapyandRiskofIntracranialHemorrhageFromCerebralCavernousMalformations:AMulticenterObservationalCohortStudy
杨中华 主任医师 北京天坛医院 神经病学中心67人已读 - 脑血管病危险因素 补充维生素D是预防缺血性卒中的新方法?
越来越多的证据表明,常见的基因变异在很大程度上是导致缺血性卒中(Ischemicstroke,IS)的原因。这种基因不仅影响卒中的风险,还影响卒中的严重程度、结局和复发。迄今为止,已发表的最大规模的IS全基因组关联研究(genome-wideassociationstudy,GWAS)确定了32个易感风险基因座(loci),这些基因座改变了所有卒中亚型,包括心源性栓塞、小血管和大动脉卒中。此外,后续研究显示IS的遗传率约为38%。然而,由于缺乏测序数据的大型研究,迄今为止,大多数研究都聚焦在常见和低频遗传变异上,只有少数研究涉及了罕见变异的贡献。2023年3月来自美国的GuidoJ.Falcone等在Stroke上公布了他们的研究结果,他们利用英国生物库200632名参与者的全外显子组测序(whole-exomesequencing,WES)数据,旨在确定IS的罕见遗传危险因素。在这项研究中,研究者发现CYP2R1的罕见基因变异是缺血性卒中的危险因素。CYP2R1在维生素D代谢中扮演着重要作用,以前的观察性证据也显示维生素D和脑血管病有关。译者注:缺血性卒中的病因复杂,单纯一个基因变异影响到所有卒中病因似乎说不过去,以后应该探索这个基因变异对不同卒中病因的作用。文献出处:troke.2023Mar;54(3):800-809.doi:10.1161/STROKEAHA.122.040883.Epub2023Feb10.Whole-ExomeSequencingAnalysesSupportaRoleofVitaminDMetabolisminIschemicStroke
杨中华 主任医师 北京天坛医院 神经病学中心110人已读





