重庆大坪医院关节四肢外科科普号
- 精选 股骨头骨坏死塌陷机制研究进展
股骨头骨坏死是骨科临床常见的难治性疾病,多种原因可以引起该疾病,然而目前其病理机制还不是很明确。股骨头骨坏死后发生股骨头塌陷,是该病进展过程中的一个重要节点,特别是对于活动量大的年轻患者。我们回顾文献发现骨坏死修复过程中成骨和破骨活动的不平衡会导致股骨头内骨小梁力学性能及结构的改变,从而在正常力学载荷的情况下导致股骨头发生塌陷。所以我们认为防治股骨头骨坏死塌陷不但要为股骨头提供有效的力学支撑,更重要的是要调节股骨头局部的成骨和破骨活动。 股骨头骨坏死(osteonecrosis of the femoral head, ONFH),又名股骨头缺血性坏死(avascular necrosis, AVN),是由于多种原因造成股骨头血供受损,骨细胞死亡,晚期导致股骨头塌陷和髋关节骨关节炎[1]。目前尚没有该病准确发病率的报道。在美国每年大约有15000例新发病例,且呈逐年增长的趋势,另外每年约有5%-18%的髋关节置换是因为股骨头骨坏死造成的[2]。在日本2004年大约有11400例患者因该病就诊[3]。据统计在我国台湾,46.3%髋关节置换的病因是股骨头骨坏死[4]。该病主要影响30-40岁人群[5],男性患病率是女性的3倍,75%的患者累及双侧髋关节。ONFH往往会导致股骨头塌陷,继而发生髋关节骨性关节炎[6]。尽管人工髋关节置换对晚期ONFH的治疗令人满意,但是对于早期ONFH的治疗,防止股骨头塌陷仍很重要的,特别是对于年轻、活动量大的患者。目前有多种方法被报道用于防治ONFH早期股骨头塌陷,但是临床效果都不是很满意,所以正确的理解股骨头骨坏死塌陷的机制是获得满意临床疗效的关键。因此我们回顾文献,总结了导致ONFH股骨头塌陷的可能机制,为该疾病的有效早期治疗提供依据。1.病因和病理机制ONFH的病理机制目前还不是很明确,部分病例具有明显的诱因,如创伤,辐射或者减压病[7]。目前公认的病因包括:长期使用激素、酗酒、吸烟、髋部创伤和髋部手术。其他可能的病因包括:青少年骺滑移、深海潜水或高气压疾病、系统性红斑狼疮和其他结缔组织疾病、自身免疫性疾病导致的血管炎、镰状细胞贫血、凝血病(易栓症和弥散性血管内凝血)、HIV感染、高脂血症、脂肪栓塞综合征、化疗和放疗、器官移植、慢性肝病、高雪氏症、痛风和代谢性骨病等。ONFH常见的病因是使用皮质激素(51%)和酗酒(31%)[3]。其中皮质激素的使用是发生ONFH的最常见原因。连续使用皮质激素超过1个月的患者中,大约5%-25%的患者会发生ONFH[8],并且其发生风险随着激素的使用量和使用时间而增加。ONFH患者中大约有15%的患者没有明显诱因,被称作是特发性股骨头骨坏死。许多特发性股骨头骨坏死患者与基因变异有关。台湾学者曾发现一个家族性ONFH,其家族成员的COL IIA1基因发生突变[9]。虽然目前研究发现多种因素都能导致骨坏死,但是其发病机制却不明确。一些学者认为骨坏死是由于股骨头骨及周围软组织的损伤导致的。股骨头血供受损被认为股骨头骨坏死的始动因素[10],特别是对于创伤性骨坏死。血管造影检查发现,在ONFH早期旋骨内侧和旋骨外侧动脉往往显影缺失,这可能是ONFH的重要发病机制。一旦股骨头血供受损,细胞发生死亡,骨髓水肿导致髓腔内压力升高,进一步减低了股骨头的血液供应。在动物实验研究中发现,激素可以使骨髓中的脂肪细胞肿大,加之股骨头的封闭皮质骨腔,骨髓腔压力显著升高会进一步加重缺血。另外,升高的髓内压也会阻断股骨头血供,这点解释了为什么高压环境工作者的ONFH发病率较高(减压病)。但是也有学者认为髓内压的增高与骨坏死的进展无关。相比创伤性骨坏死而言,非创伤性骨坏死的病理机制更加复杂[11]。皮质激素能够作用于多种代谢通路,影响成骨细胞分化、成破骨细胞凋亡、脂代谢、凝血和钙的代谢, 因此激素相关的骨坏死的病理机制就更加复杂[12]。目前在软骨细胞、成骨细胞、破骨细胞和骨细胞中均发现了皮质激素的受体[13, 14]。皮质激素的对免疫系统的作用机制十分复杂,它可以同时在抑制性通路和兴奋性通路影响多种基因的转录[15],由于很多调节因子都同时存在于免疫系统和骨代谢系统中,所以皮质激素对二者的影响十分复杂和深奥。体内研究证实,长时间给予皮质激素会导致成骨和破骨细胞发生凋亡[16]。皮质激素可以直接阻止骨髓细胞向成骨细胞分化,转而向脂肪细胞分化[17]。皮质激素对骨的作用十分复杂,它可以抑制成骨细胞和破骨细胞的生成,增加细胞凋亡,延长破骨细胞生存周期[12]。在ONFH中骨组织正常的修复机制被破坏。正常修复时,新生血管长入坏死区,死骨被吸收伴随着新骨的生成。爬行替代的过程主要包括:破骨细胞吸收坏死骨组织,成骨细胞沿着失细胞小梁骨生成新骨[18]。新骨的形成和新生血管的形成与骨修复密切相关。在ONFH中,虽然破骨细胞诱导的骨吸收会导致股骨头塌陷,但是其准确的修复机制却不是很清楚。有研究发现,在ONFH早期破骨细胞主要集中在圆韧带和支持带周围,在晚期主要集中在修复反应界面。并且在早期坏死区可以检测到低氧诱导因子、血管内皮生长因子和成纤维细胞生长因子的表达,但是没有诱导新生血管形成[19]。2.ONFH股骨头塌陷机制ONFH会导致患者髋关节疼痛并跛行,该病的进展与股骨头的塌陷密切相关。有研究报道ONFH股骨头塌陷的发生率在44%-79%之间,平均塌陷发生率约为50%,并且塌陷往往发生在明确诊断后的两年之内[20, 21]。有研究对100例明确诊断双侧ONFH,一侧已行髋关节置换的患者进行随访研究发现,未置换的髋关节往往在两年之内就发生塌陷。并且年轻(小于50岁)、活动量大和血清高甘油三脂的患者股骨头塌陷的风险更高[22]。但是有些学者认为,股骨头塌陷并不是ONFH病程的关键因素。Nishii等研究发现如果塌陷程度小于2mm并且坏死区累及范围小于负重区的内侧2/3,那么即使在没有外科干预的情况下,塌陷过程也会静止,并且患者症状也会减轻[21]。他们认为股骨头塌陷不一定是ONFH不良预后的征兆。还有研究发现,即使坏死范围很大或已有晚期影像学表现,股骨头关节软骨的外观和力学性能仍可以保持正常[23]。相反,多数学者认为,股骨头塌陷是ONFH不良预后的标志,因为塌陷的发生表明股骨头的正常结构遭到了严重破坏[21]。当出现股骨头塌陷或者塌陷大于2mm时会导致患者髋关节疼痛并且继发髋臼侧发生退变,从而导致骨性关节炎形成。很多研究发现,一旦骨坏死出现,大约80%的股骨头会发生塌陷并且大多数患者需要进行髋关节置换手术。虽然髋关节置换手术可以有效恢复晚期患者的髋关节功能,但是对于20-50岁的年轻患者而言则可能在一生中需要经受多次的翻修手术[24, 25]。因此防止股骨头塌陷应该被得到重视,因为股骨头塌陷是ONFH病程中的重要转折点[23]。目前ONFH股骨头塌陷机制还不是很明确。对于小范围的骨坏死,坏死的骨组织可以通过“爬行替代”被正常新生骨组织所取代。 然而对于大范围的坏死,新生血管只能长入到坏死区的周围,大量新生骨组织出现在坏死区周围并形成硬化带,这进一步阻止了血管向坏死区中心的长入。从而坏死区中心不能得到有效修复,导致坏死区小梁骨组织力学性能降低,最终发生骨折而导致股骨头塌陷[18]。股骨头塌陷常发生在股骨头的前上方,因为该区域是股骨头负重最集中的区域。 Christian等对7例髋关节炎和3例股骨颈骨折的股骨头进行病理学研究发现,股骨颈骨折组股骨头的整体骨质和骨量都显著降低,在每一个股骨头中骨量的分布比较一致,但是在前侧区域骨质的降低比较显著。所以作者认为股骨头前侧区域更易于受到载荷损伤,并建议对于ONFH的力学支撑应集中于前侧区域[26]。Brown等认为紧邻软骨下骨板的骨小梁力学性能减低是股骨头塌陷的始动因素。他们将ONFH股骨头标本切割成小立方体并分别进行单轴压缩实验,坏死区屈服强度下降52%,弹性模量下降72%,最大牵拉负荷增加29%。他们还采用了3D有限元分析了不同坏死范围下,股骨头不同区域的应力分布情况,发现ONFH股骨头应力分布十分复杂。另外,即使是完全正常的软骨下骨板也只能够为坏死区的骨小梁提供一定的力学保护,坏死区的骨小梁仍要承受较大的应力载荷。在应力过载或者正常应力合并骨损伤的情况下,骨小梁会因为微创伤导致发生微骨折,这是ONFH的亚临床病理改变。股骨头皮质骨壳的形变被认为是股骨头塌陷的驱动力,从而导致整个股骨头发生塌陷。Volokh等研究发现正常的骨小梁能够对股骨头皮质骨壳提供有效的力学支撑,从而防止其变形[27]。然而,在发生骨坏死时,松质骨骨小梁杨氏模量降低,导致其最大应力载荷下降,不能够有效防止股骨头皮质骨壳发生形变。因此有学者建议,对股骨头的力学支撑应该尽可能的接近其皮质骨壳。此外,一些研究发现骨的修复能力在ONFH进展中发挥了重要的作用[28]。骨坏死修复往往起始于其反应界面,该界面形成于正常骨组织与坏死骨组织之间,主要由纤维组织构成。新生血管从坏死区边缘侵入,破骨细胞将坏死骨组织吸收并由成骨细胞介导新骨形成。然而由于血管化程度有限,骨修复往往出现在坏死区边缘。由于破骨细胞过度活跃,负重区的骨组织容易出现塌陷[28]。对51例ONFH股骨头标本研究发现,在影像学早期,破骨细胞主要出现在股骨头圆韧带和支持带附着的位置,随着疾病的进展修复界面附近的破骨细胞数量显著增加[19]。股骨头坏死塌陷的进程主要受到骨修复进程的影响,特别是破骨细胞介导的骨吸收作用。在修复反应界面,破骨细胞的过度活跃降低了骨小梁的骨质和力学特性,在正常应力负荷下会导致受损的骨小梁发生微骨折,从而导致股骨头塌陷。总之,破骨细胞介导的骨吸收和成骨细胞介导的骨形成之间的失衡,加之坏死区骨小梁的应力集中可能是导致股骨头发生塌陷的主要机制。3.预测ONFH股骨头塌陷方法骨矿密度、关节面与坏死范围的比率、闪烁显像技术以及基于MRI的Kerboul法和改良Kerboul法已经被用于预测股骨头塌陷的可能性[27, 29-31]。研究证明坏死区的位置和范围与股骨头坏死塌陷具有密切关系[32]。坏死范围与股骨头塌陷关系密切,而在坏死范围较小的情况下,坏死区的位置被认为是预测塌陷的重要指标[31]。坏死累及的关节面范围及其与整个关节面的比率也可以被用来预测股骨头塌陷[30]。骨闪烁显像技术可以评价交界面的修复活动情况,在ONFH早期,修复界面对示踪剂的高摄取表明股骨头容易发生塌陷[29]。依据对塌陷机制的研究,我们建议采用基于MRI的改良Kerboul法,并联合使用评价修复活动强度的方法,以此来评价股骨头塌陷的风险。总之,由于股骨头血供受损,股骨头内环境发生紊乱,导致细胞发生死亡,形成空骨陷窝。与此同时,骨细胞的死亡导致骨髓发生水肿,增加了髓腔内压力,再血管化和成破骨活动的失衡导致修复区骨小梁的力学性能降低,在正常载荷的情况下,受损的骨小梁发生微骨折,从而导致股骨头发生塌陷。如果想防止股骨头发生塌陷,那么治疗的时间窗口应该被限定在股骨头骨坏死早期,即未发生明显塌陷之前。回顾文献,我们建议首先应减轻患者对髋关节的负重,然后给予有效力学支撑并局部调节骨修复进程。
苟文隆 副主任医师 陆军特色医学中心(大坪医院) 关节四肢外科1846人已读 - 精选 骨性关节炎诊治指南
骨性关节炎(osteoarthritis,OA)是一种以关节软骨的变性、破坏及骨质增生为特征的慢性关节病。本病在中年以后多发。国内的初步调查显示,骨性关节炎的总患病率约为15%,40岁人群的患病率为10%-17%, 60岁以上则达50%。而在75岁以上人群中,80%患有骨性关节炎。该病的最终致残率为53%。临床上以关节肿痛、骨质增生及活动受限最为常见。骨性关节炎的发病无地域及种族差异。年龄、肥胖、炎症、创伤及遗传因素可能与本病的发生有关。[临床表现] 1、症状和体征骨性关节炎主要表现为受累关节的疼痛、肿胀、晨僵、关节积液及骨性肥大,可伴有活动时的骨擦音、功能障碍或畸形。(1)关节疼痛及压痛 本病最常见的表现是关节局部的疼痛和压痛。负重关节及双手最易受累。一般早期为轻度或中度间断性隐痛,休息时好转,活动后加重,随病情进展可出现持续性疼痛,或导致活动受限。关节局部可有压痛,在伴有关节肿胀时尤为明显。(2)关节肿胀 早期为关节周围的局限性肿胀,但随病情进展可有关节弥漫性肿胀、滑囊增厚或伴关节积液。后期可在关节周围触及骨赘。(3)晨僵 患者可出现晨起时关节僵硬及黏着感,经活动后可缓解。本病的晨僵时间较短、一般数分钟至十几分钟,很少超过半小时。(4)关节摩擦音 主要见于膝关节的骨关节炎。由于软骨破坏,关节表面粗糙,出现关节活动时骨摩擦音(感)、捻发感,或伴有关节局部疼痛。2、不同部位的骨性关节炎(1)手 以远端指间关节受累最为常见,表现为关节伸侧面的两侧骨性膨大,称赫伯登(Heberden)结节。而近端指间关节伸侧出现者则称为布夏尔(Bouchard)结节。可伴有结节局部的轻度红肿、疼痛和压痛。第一腕掌关节受累后,其基底部的骨质增生可出现方形手畸形,而手指关节增生及侧向半脱位可致蛇样畸形。(2)膝关节 膝关节受累在临床上最为常见。危险因素有肥胖、膝外伤和半月板切除。主要表现为膝关节疼痛,活动后加重,休息后缓解。严重病例可出现膝内翻或膝外翻畸形。(3)髋关节 髋关节受累多表现为局部间断性钝痛,随病情发展可成持续性疼痛。部分患者的疼痛可以放射到腹股沟、大腿内侧及臀部。髋关节运动障碍多在内旋和外展位,随后可出现内收、外旋和伸展受限。(4)脊柱 颈椎受累比较常见。可有椎体、椎间盘以及后突关节的增生和骨赘,引起局部的疼痛和僵硬感,压迫局部血管和神经时可出现相应的放射痛和神经症状。颈椎受累压迫椎-基底动脉,引起脑供血不足的症状。腰椎骨质增生导致椎管狭窄时可出现间歇性跛行以及马尾综合征。(5)足 跖趾关节常有受累,除了出现局部的疼痛、压痛和骨性肥大外,还可以出现拇外翻等畸形。3、特殊类型的骨性关节炎(1)原发性全身性骨关节炎 以远端指间关节、近端指间关节和第一腕掌关节为好发部位。膝、髋、跖趾关节和脊柱也可受累。症状呈发作性,可有受累关节积液、发热等表现。可根据临床和流行病学将其分为两类:①结节型以远端指间关节受累为主,女性多见,有家族聚集现象。②非结节型以近端指间关节受累为主,性别和家族聚集特点不明显,但常反复出现外周关节炎。重症患者可有血沉增快及C反应蛋白增高等。(2)侵蚀性炎症性骨关节炎 常见于绝经后的女性,主要累及远端及近端指间关节和腕掌关节。有家族倾向性及反复急性发作的特点。受累的关节出现疼痛和触痛,最终导致关节的畸形和强直。患者的滑膜检查可见明显的增生性滑膜炎,并可见免疫复合物的沉积和血管翳的生成。X线可见明显的骨赘生成和软骨下骨硬化,晚期可见明显的骨侵蚀和关节骨性强直。(3)弥漫性特发性骨质增生症(diffuse idiopathic skeletal hyperostosis, DISH) 好发于中老年男性。病变累及整个脊柱,呈弥漫性骨质增生,脊柱韧带广泛增生骨化及其邻近的骨皮质增生。但是,椎小关节和椎间盘保持完整。一般无明显症状,少数患者可有肩背痛、发僵、手指麻木或腰痛等症状,病变严重时会出现椎管狭窄的相应表现。X线片可见特征性椎体前纵及后纵韧带的钙化,以下胸段为著,一般连续4个或4个椎体以上,可伴广泛骨质增生。4、实验室检查血常规、蛋白电泳、免疫复合物及血清补体等指标一般在正常范围。伴有滑膜炎的患者可出现C-反应蛋白和血沉轻度升高。类风湿因子及抗核抗体阴性。继发性骨关节炎的患者可出现原发病的实验室检查异常。出现滑膜炎者可有关节积液,但是,一般关节液透明,淡黄色,黏稠度正常或略降低,但黏蛋白凝固良好。5、X线检查骨性关节炎的X线特点为:非对称性关节间隙变窄;软骨下骨硬化和囊性变;关节边缘的骨质增生和骨赘形成;关节内游离体;关节变形及半脱位。这些变化是骨关节炎诊断的重要依据。[诊断要点]根据患者的临床表现、体征和影像学等辅助检查,骨性关节炎的诊断并不困难。目前,国内多采用美国风湿病学会1995年的诊断标准(表1-3)。表1 手骨性关节炎的分类标准(临床标准)1. 近1个月大多数时间有手痛,发酸,发僵2. 10个指间关节中,骨性膨大关节≥2个3. 掌指关节肿胀≤2个4. 远端指间关节骨性膨大>2个5. 10个指间关节中,畸形关节≥1个满足1+2+3+4条或1+2+3+5条可诊断手骨性关节炎注:10个指间关节为双侧第二、三远端及近端指间关节,双侧第一腕掌关节。表2 膝骨性关节炎分类标准 临床标准 1. 近1个月大多数时间有膝痛2. 有骨摩擦音3. 晨僵≤30min4. 年龄≥38岁5. 有骨性膨大满足1+2+3+4条,或1+2+5条或1+4+5条者可诊断膝骨性关节炎临床+放射学标准 1. 近1个月大多数时间有膝痛2. X线片示骨赘形成3. 关节液检查符合骨性关节炎4. 年龄≥40岁5. 晨僵≤30min6. 有骨摩擦音满足1+2条或1+3+5+6条,或1+4+5+6条者可诊断膝骨性关节炎表3 髋骨性关节炎分类标准临床+放射学标准 1. 近1个月大多数时间髋痛2. 血沉≤20mm/h3. X线片有骨赘形成4. X线片髋关节间隙狭窄满足1+2+3条或1+2+4条或1+3+4条者可诊断髋骨性关节炎[治疗]治疗的目的在于缓解疼痛、阻止和延缓疾病的发展及保护关节功能。治疗方案应依据每个患者的病情而定。1、一般治疗(1)患者教育 使患者了解本病的治疗原则、锻炼方法,以及药物的用法和不良反应等。(2)物理治疗 包括热疗、水疗、经皮神经电刺激疗法、针灸、按摩和推拿、牵引等,均有助于减轻疼痛和缓解关节僵直。(3)减轻关节负荷,保护关节功能 受累关节应避免过度负荷,膝或髋关节受累患者应避免长久站立、跪位和蹲位。可利用手杖、步行器等协助活动,肥胖患者应减轻体重。肌肉的协调运动和肌力的增强可减轻关节的疼痛症状。因此患者应注意加强关节周围肌肉的力量性锻炼,并设计锻炼项目以维持关节活动范围。2、药物治疗主要可分为控制症状的药物、改善病情的药物及软骨保护剂(表4-5)。(1)控制症状的药物①非甾体抗炎药(NSAIDs) NSAIDs是最常用的一类骨关节炎治疗药物(表4),其作用在于减轻疼痛及肿胀,改善关节的活动。主要的药物包括双氯酚酸等,如果患者发生NSAID相关胃肠道疾病的危险性较高,则罗非昔布、塞来昔布及美洛昔康等选择性环氧化酶-2抑制剂更为适用。药物剂量应个体化,同时注意对老年患者合并的其它疾病影响。表4 治疗骨性关节炎的常用NASIDs 丙酸衍生物 布洛芬 酮洛芬 洛索洛芬苯酰酸衍生物 双氯芬酸 吲哚酰酸类 舒林酸 阿西美辛吡喃羧酸类 依托度酸非酸性类 萘丁美酮昔康类 美洛昔康磺酰苯胺类 尼美舒利昔布类 塞来昔布 罗非昔布 表5 骨性关节炎患者的药物治疗口服 对乙酰氨基酚关节软骨保护剂 硫酸氨基葡萄糖选择性COX-2抑制剂 非选择性NSAIDs+米索前列醇或质子泵抑制剂其它止痛剂 盐酸曲马多关节内注射 糖皮质激素 透明质酸钠局部外用药治疗 双氯酚酸钠乳胶剂 依托芬那酯霜②其它止痛剂 对乙酰氨基酚对骨关节炎有良好的止痛作用,费用低,在国外仍广泛使用,而国内的应用相对较少。每日剂量最多不超过4000mg。若上述方法仍不能有效缓解症状,可予以曲马多治疗。该药为一种弱阿片类药物,耐受性较好而成瘾性小,平均剂量每日200-300mg,但应注意不良反应。③局部治疗 包括局部外用NSAIDs药物及关节腔内注射治疗。糖皮质激素可缓解疼痛、减少渗出,效果可持续数周至数月,但仅适用于关节腔注射治疗,在同一关节不应反复注射,一年内注射次数应少于4次。关节腔内注射透明质酸类制剂(欣维可、其胜及施沛特等)对减轻关节疼痛、增加关节活动度、保护软骨有效,治疗效果可持续数月,适用于对常规治疗效果不佳或不能耐受者。(2)改善病情药物及软骨保护剂此类药物具有降低基质金属蛋白酶、胶原酶等的活性作用,既可抗炎、止痛,又可保护关节软骨,有延缓骨性关节炎发展的作用。一般起效较慢。主要的药物包括硫酸氨基葡萄糖、葡糖胺聚糖、S-腺苷蛋氨酸及多西环素等。双醋瑞因也可明显改善患者症状,保护软骨,改善病程。骨性关节炎的软骨损伤可能与氧自由基的作用有关,近几年来的研究发现,维生素C、D、E可能主要通过其抗氧化机制而有益于骨性关节炎的治疗。3、外科治疗对于经内科治疗无明显疗效,病变严重及关节功能明显障碍的患者可以考虑外科治疗。(1)关节镜手术 对有明显关节疼痛,并对止痛剂、关节内糖皮质激素注射治疗效果不理想的患者,可关节内予以大量灌洗来清除纤维素、软骨残渣及其它杂质,可减轻患者的症状。还可通过关节镜去除软骨碎片。(2)整形外科手术 截骨术可改善关节力线平衡,有效缓解患者的髋或膝关节疼痛。对60岁以上、正规药物治疗反应不佳的进展性骨性关节炎患者可予以关节置换,由此可显著减轻疼痛症状,改善关节功能。此外,新的治疗方法如软骨移植及自体软骨细胞移植等有可能用于骨性关节炎的治疗,但尚需进一步临床研究。
熊雁 副主任医师 陆军特色医学中心(大坪医院) 关节四肢外科4092人已读 - 引用 股骨头坏死诊治指南
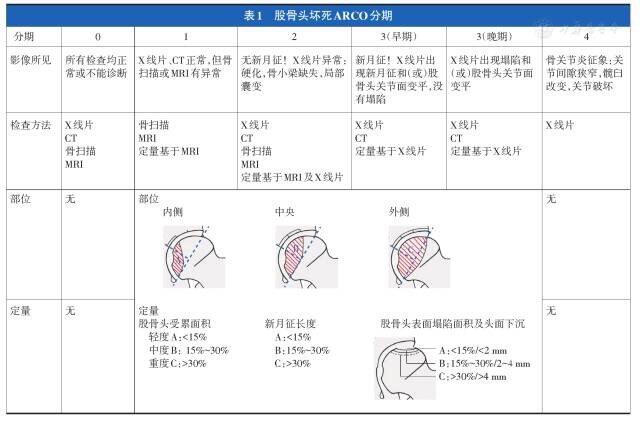
股骨头坏死曾被称为股骨头缺血性坏死和股骨头无菌性坏死,是骨科常见的难治性疾病。对任何年龄段、任何病理分期的患者,规范的诊疗方案都非常重要。"《股骨头坏死诊疗专家意见(2007)》"、"《成人股骨头坏死诊疗专家共识(2012)》"的制定为国内股骨头坏死诊疗的规范化起到了巨大的推动作用,但在分期规范化与治疗方式的选择方面仍存在不足之处。 为了更加规范而有效地诊治股骨头坏死,中国医师协会骨科医师分会显微修复工作委员会、中国修复重建外科专业委员会骨缺损及骨坏死学组和中华医学会骨科分会显微修复学组共同组织国内股骨头坏死研究领域的专家,于2015年3月21日经过对既往专家共识的讨论、修改,结合近几年的研究进展,制定了成人股骨头坏死临床诊疗指南。 一、概述 1 定义:股骨头坏死是股骨头静脉淤滞、动脉血供受损或中断使骨细胞及骨髓成分部分死亡及发生随后的修复,继而引起骨组织坏死,导致股骨头结构改变及塌陷,引起髋关节疼痛及功能障碍的疾病。 2 流行病学:我国股骨头坏死的患病率为平原农民11.76/万,城市居民9.57/万,工人7.92/万,山区农民6.29/万,沿海渔民5.53/万。 3 病因及高危人群:股骨头坏死可分为创伤性和非创伤性两大类。创伤性股骨头坏死的主要致病因素包括股骨头颈骨折、髋臼骨折、髋关节脱位、髋部严重扭伤或挫伤(无骨折,有关节内血肿);非创伤性股骨头坏死在我国的主要病因为皮质类固醇类药物应用、长期饮酒过量、减压病、血红蛋白病(镰状细胞贫血、镰状细胞血红蛋白C病、地中海贫血、镰状细胞特质等)、自身免疫病和特发性等。吸烟、肥胖等增加了发生股骨头坏死的风险,被认为与股骨头坏死相关。 二、诊断标准 1 临床特点:多以髋部、臀部或腹股沟区的疼痛为主,偶尔伴有膝关节疼痛,髋关节内旋活动受限。常有髋部外伤史、皮质类固醇类药物应用史、酗酒史及潜水员等职业史。 2 MRI影像:MR检查对股骨头坏死具有较高的敏感性。表现为T1WI局限性软骨下线样低信号或T2WI "双线征" 。 3 X线影像:正位和蛙式位是诊断股骨头坏死的X线基本体位,通常表现为硬化、囊变及"新月征"等。 4 CT扫描征象:通常出现骨硬化带包绕坏死骨、修复骨,或表现为软骨下骨断裂。 5 放射性核素检查:股骨头急性期骨扫描(99Tcm-MDP、99Tcm-DPD等)可见冷区;坏死修复期表现为热区中有冷区,即"面包圈样"改变。单光子发射计算机断层显像(SPECT)或许可能提高放射性核素检查对股骨头坏死诊断的灵敏度。正电子发射断层扫描(PET)可能比MRI和SPECT更早发现股骨头坏死征象,并可以预测股骨头坏死的进展。 6 骨组织活检:骨小梁的骨细胞空陷窝多于50%,且累及邻近多根骨小梁,骨髓坏死。 7 数字减影血管造影:表现为股骨头血供受损、中断或淤滞。不建议在诊断时常规应用。 除1外,2至7另外符合任意一条即可确诊。 三、鉴别诊断 对具有股骨头坏死类似临床症状、X线或MRI影像学表现的患者,应注意鉴别。 1 中、晚期髋关节骨关节炎:当关节间隙变窄并出现软骨下囊性变时与股骨头坏死不易鉴别。但股骨头坏死的CT表现为硬化并有囊性变,MRI改变以低信号为主,可据此鉴别。 2 髋臼发育不良继发骨关节炎:X线表现为股骨头包裹不全,关节间隙变窄、消失,骨硬化及囊变,髋臼对应区出现类似改变,容易鉴别。 3 强直性脊柱炎累及髋关节:常见于青少年男性,多为双侧骶髂关节受累,血清检测HLA-B27阳性,X线表现为股骨头保持圆形而关节间隙变窄、消失甚至融合,容易鉴别。部分患者长期应用皮质类固醇类药物可并发股骨头坏死,股骨头可出现塌陷但往往不严重。 4 暂时性骨质疏松症:中青年发病,属暂时性疼痛性骨髓水肿。X线片表现为股骨头颈甚至转子部骨量减少;MRI表现为T1WI均匀低信号、T2WI高信号,范围可至股骨颈及转子部,无带状低信号;病灶可在3~12个月内消散。 5 股骨头内软骨母细胞瘤:MRI表现为T2WI片状高信号,CT扫描呈不规则的溶骨破坏。 6 软骨下不全骨折:多见于60岁以上患者,无明显外伤史,表现为突然发作的髋部疼痛,不能行走,关节活动受限。X线片示股骨头外上部稍变扁;MRI表现为T1WI及T2WI软骨下低信号线及周围骨髓水肿,T2抑脂像出现片状高信号。 7 色素沉着绒毛结节性滑膜炎:多发于膝关节,髋关节受累少见。累及髋关节者以青少年发病、髋部轻中度疼痛伴跛行、早中期关节活动轻度受限为特征。CT及X线片表现为股骨头颈或髋臼皮质骨侵蚀,关节间隙轻中度变窄;MRI表现为广泛滑膜肥厚,低或中度信号均匀分布。 8 滑膜疝:滑膜组织增生侵入股骨颈皮质的良性病变,通常无临床症状。MRI表现为股骨颈上部皮质T1WI低信号、T2WI高信号的小圆形病灶。 9 骨梗死:发生在干骺端或长骨骨干的骨坏死,不同时期MRI影像表现不同。①急性期:病变中心T1WI呈与正常骨髓等或略高信号,T2WI呈高信号,边缘呈长T1、T2信号;②亚急性期:病变中心T1WI呈与正常骨髓等或略低信号,T2WI呈与正常骨髓等或略高信号,边缘呈长T1、长T2信号;③慢性期:T1WI和T2WI均呈低信号。 四、分期 建议采用国际骨微循环研究协会(ARCO)分期系统(表1)。ARCO分期是1991年ARCO委员会在综合Ficat分期、Steinberg分期和日本骨坏死研究会分期后制定的分期系统,较之前的任何一种分期方法都更系统、更全面、更实用,在确定诊断、评估治疗效果和预后方面具有很高的价值。我国于2015年制订了股骨头坏死中国分期(表2),推荐临床工作中与ARCO分期同时应用。 五、股骨头坏死的治疗 治疗方法包括非手术治疗和手术治疗。 1 非手术治疗 保护性负重:避免撞击性和对抗性运动。使用双拐可有效减轻疼痛,不主张使用轮椅。 药物治疗:建议选用抗凝、增加纤溶、扩张血管与降脂药物联合应用,如低分子肝素、前列地尔、华法林与降脂药物的联合应用等。也可联合应用抑制破骨和增加成骨的药物,如磷酸盐制剂、美多巴等。药物治疗可单独应用,也可配合保髋手术应用。 中医药治疗:以中医整体观为指导,遵循"动静结合、筋骨并重、内外兼治、医患合作"的基本原则,强调早期诊断、病证结合、早期规范治疗。对高危人群及早期无痛患者以活血化瘀为主、辅以祛痰化湿、补肾健骨等中药,具有促进坏死修复、预防塌陷的作用;对早期出现疼痛等症状的股骨头坏死,在保护性负重的基础上应用活血化瘀、利水化湿的中药,能缓解疼痛、改善关节功能;对中晚期股骨头坏死,应用活血化瘀、利水化湿中药配合外科修复手术,能提高保髋手术效果。 物理治疗:包括体外冲击波、电磁场、高压氧等。 制动与牵引:适用于股骨头坏死早中期病例。 2 手术治疗 股骨头坏死进展较快,非手术治疗效果不佳,多数患者需要手术治疗。手术方式包括保留患者自身股骨头为主的修复重建术和人工髋关节置换术两大类。保留股骨头的手术包括髓芯减压术、截骨术、带或不带血运的骨移植术等,适用于股骨头坏死早期(ARCO 0~1期)或中期(ARCO 2~3B期),且坏死体积在15%以上的股骨头坏死患者。如果方法有效,可避免或推迟人工关节置换术。 髓芯减压术:手术开展时间长,疗效肯定。目前可分为细针钻孔减压术和粗通道髓芯减压术。其区别主要在于减压通道的直径,细针钻孔减压术的孔道直径为3、3.5或4 mm,粗通道髓芯减压术为6 mm以上。目前髓芯减压联合干细胞移植(或浓集自体骨髓单个核细胞移植)在国内医疗机构的临床应用效果较好,因此在获得国家资质的前提下可以使用。 不带血运骨移植术:应用较多的术式有经股骨转子减压植骨术、经股骨头颈灯泡状减压植骨术等。植骨方法包括压紧植骨、支撑植骨等,植骨材料包括自体皮质骨和松质骨、异体骨、骨替代材料。 截骨术:目的是将坏死区移出股骨头负重区。截骨术包括内翻或外翻截骨、经股骨转子旋转截骨等,以不改建股骨髓腔为原则选择术式。 带血运自体骨移植术:自体骨移植分为髋周骨瓣移植及腓骨移植。髋周带血管蒂骨瓣移植包括:①带旋股外侧血管升支髂骨(膜)瓣转移术;②旋股外侧血管升支臀中肌支大转子骨瓣转移术;③带旋股外侧血管横支的大转子骨瓣转移术;④带旋髂深血管蒂的髂骨(膜)瓣转移术;⑤对整个股骨头甚至部分股骨颈受到累及者采用的横支大转子骨瓣联合升支髂骨(膜)瓣再造股骨头(颈);⑥髋关节后方入路股内侧血管深支大转子骨瓣、臀上血管深上支髂骨瓣等。髋周带血管蒂骨瓣手术创伤小、疗效确切、手术方法容易掌握,推荐使用。为增加股骨头内的强力支撑,在应用髋周带血管蒂骨瓣时可联合支撑材料植入,能够避免术后股骨头塌陷,其中短期疗效好,长期疗效有待确定。吻合血管腓骨移植的手术效果目前也较为肯定,推荐使用。带血运自体骨移植术式的选择可根据其各自优缺点、术者的熟练程度等因素综合考虑。 人工关节置换术:股骨头塌陷较重(ARCO 3C期、4期)、出现关节功能严重丧失或中度以上疼痛,应选择人工关节置换术。一般认为,非骨水泥型或混合型假体的中长期疗效优于骨水泥型假体。股骨头坏死的人工关节置换术要特别注意:①患者长期应用皮质类固醇类药物或有其他基础病需持续治疗,使感染的风险升高;②患者长期不负重、骨质疏松等原因导致假体容易穿入髋臼;③既往保留股骨头手术会给关节置换造成技术困难;④激素性、酒精性股骨头坏死不仅仅是股骨头的病变,其周围及全身骨质均已受损,因此关节置换术的远期疗效可能不及骨关节炎或创伤性股骨头坏死。 3 治疗方案的选择原则 股骨头坏死治疗方案的选择应综合考虑分期、分型、坏死体积、关节功能及患者年龄、职业及对保存关节治疗的依从性等因素(图1)。 图1 成人股骨头坏死临床诊断流程图 4 疗效评价与康复练习 疗效评价:对股骨头坏死的疗效评价可分为临床评价和影像学评价两部分。临床评价采用髋关节功能评分(如Harris评分、WOMAC评分、中华医学会骨科学分会百分法),应根据相同分期、相似坏死面积、相同治疗方法分类逐例评价。同时建议行步态分析。 影像学评价应用X线片,采用同心圆模板观察股骨头外形、关节间隙及髋臼变化。股骨头坏死中国分期Ⅱ期以内的病变评估应有MRI资料。对带血运骨移植患者应行数字减影血管造影检查,用来评价血运恢复情况。建立患者病例档案,评价不同病因、坏死时期、年龄、治疗方法的疗效,有助于规范股骨头坏死的治疗。 康复锻炼:可防止股骨头坏死患者废用性肌肉萎缩,是促使其早日恢复功能的有效手段。功能锻炼应以主动活动为主,被动活动为辅,由小到大,由少到多,逐渐增加;并根据股骨头坏死的分期、治疗方式、髋关节功能评分及步态分析结果选择适宜的锻炼方法。 ①卧位抬腿法:平仰卧,抬高患肢,屈髋屈膝90°,再放平患肢,动作反复。每日200次,分3~4次完成。应用于股骨头坏死保守治疗及外科治疗术后卧床期。 ②坐位分合法:坐在椅子上,双手扶膝,双脚与肩等宽,双腿同时充分外展、内收。每日300次,分3~4次完成。应用于股骨头坏死保守治疗及外科治疗术后可部分负重期。 ③立位抬腿法:手扶固定物,身体保持竖直,抬高患肢,屈髋屈膝90°,使身体与大腿成直角,再放下患肢,动作反复。每日300次,分3~4次完成。应用于股骨头坏死保守治疗及外科治疗术后可部分负重期。 ④扶物下蹲法:手扶固定物,身体直立,双脚与肩等宽,下蹲后再起立,动作反复。每日300次,分3~4次完成。应用于股骨头坏死保守治疗及外科治疗术后可完全负重期。 ⑤内旋外展法:手扶固定物,双腿分别做充分的内旋、外展、划圈动作。每日300次,分3~4完成。应用于股骨头坏死保守治疗及外科治疗术后可完全负重期。 ⑥扶拐步行训练或骑自行车锻炼:应用于股骨头坏死保守治疗及外科治疗术后可完全负重期。
 熊雁 副主任医师 陆军特色医学中心(大坪医院) 关节四肢外科1876人已读
熊雁 副主任医师 陆军特色医学中心(大坪医院) 关节四肢外科1876人已读 - 引用 七旬老太跛行十年几近瘫痪 大坪医院施术还她直立人生
对合川的古婆婆而言,能像正常人一样直立行走,是件天大的喜事。日前,第三军医大学大坪医院关节四肢外科为古婆婆实施了双膝关节置换术,成功为她解决了膝关节疼痛及内翻畸形问题,圆了这个梦想。 古婆婆今年71岁,患有骨性关节炎已有10年,起初,她认为“忍一忍就过去了”,当时也没太在意,谁知道双膝关节反复疼痛,行动很不方便。其间,古婆婆曾在当地医院求医,医院给予她消炎、止痛等保守治疗,但效果均不理想,只能屈膝,忍痛跛行。 雪上加霜的是,2年前,古婆婆因意外造成左腿骨折,从此病情急剧恶化,近半年来只能待在家里。“膝盖像被刀割一样,痛得我眼泪直掉,有时真想用斧头把这废腿砍掉。”古婆婆绝望了,认为自己的病再也医不好了,注定会成为一个拖累儿女的残废。 经亲戚推荐,2月21日,古婆婆坐着轮椅来到大坪医院关节四肢外科找熊雁副教授就诊。“通常内翻20°就属重度,而古婆婆的内翻已达45°,病情十分严重。”古婆婆听熊教授介绍,由于古婆婆发病较早,且没及时治疗,已经发展成重度骨关节炎和重度内翻畸形骨缺损。为了能彻底解决古婆婆的顽疾,关节四肢外科王爱民主任召集科室骨干力量,就古婆婆的病情进行反复讨论,最终选择实施双膝关节置换术。 然而,正如熊教授预料的那样,当他把古婆婆相关参数输入“大坪医院关节四肢外科术前评分系统”后,结果显示,像古婆婆这种情况,如果双膝同时做手术,那么出现术后并发症的几率将超过30%。鉴于此,熊教授决定分期主刀完成手术,术中采用金属垫块和延长杆来重建膝关节。完善相关准备后,2月28日,左膝关节置换术顺利完成;3月8日,右膝关节置换术非常成功。 3月16日,在关节四肢外科8号病床里的古婆婆,已经可以扶着助行器逐步直立行走。古婆婆心情大好,对王主任和熊教授赞不绝口,“我终于不必一直窝在家里了,可以直立行走了,我迫不及待想走出家门,去看看老姐妹,去赶场。”
 熊雁 副主任医师 陆军特色医学中心(大坪医院) 关节四肢外科1935人已读
熊雁 副主任医师 陆军特色医学中心(大坪医院) 关节四肢外科1935人已读 - 引用 中国骨质疏松性骨折诊疗指南(骨质疏松性骨折诊断及治疗原则
中国骨质疏松性骨折诊疗指南(骨质疏松性骨折诊断及治疗原则)(2015) 邱贵兴 更新于2016-01-22 15:31 摘要: 1 概述 骨质疏松症是一种全身性、代谢性骨骼系统疾病,其病理特征为骨量降低、骨微细结构破坏、骨脆性增加,骨强度下降,易发生骨折。与年龄、性别、种族等因素密切相关,绝经后妇女多发。骨折是骨质疏松症最严重的后果,常是骨质疏松患者的首发症状和就诊原因。骨质疏松症分为原发性和继发性,本指南所指的骨折是原发性骨质疏松症导致的骨折。 1.1 骨质疏松性骨折的特点及治疗难点 ①患者多为老年人,常合并其他疾病,易发生并发症。 ②多为粉碎性骨折,内固定治疗稳定性差,内置物易松动、脱出,植骨易被吸收。 ③骨形成与骨痂成熟迟缓,易发生骨折延迟愈合,甚至不愈合。 ④卧床制动期将发生快速骨丢失,再骨折的风险明显增大。 ⑤致残率、致死率较高。 ⑥再骨折发生率高,髋部骨折患者1年内再次发生骨折达20%。 1.2 骨质疏松性骨折的治疗原则 骨质疏松性骨折的治疗基本原则是复位、固定、功能锻炼和抗骨质疏松。 2 骨质疏松性骨折诊断及鉴别诊断 2.1 诊断 2.1.1 病史、症状和体征 有骨质疏松性骨折史或轻微外伤史。可出现疼痛、肿胀、功能障碍等症状,畸形、骨擦感(音)、异常活动等体征,也有患者骨折后缺乏上述典型表现。椎体压缩性骨折,可致身高变矮或驼背畸形。 2.1.2 影像学检查 普通X线检查:①摄片应包括损伤部位上、下邻近关节,髋部骨折应包括双侧髋关节;②除有骨折征象外,还有骨质疏松的表现;③椎体压缩骨折时,有楔形变或“双凹征”,部分可表现为椎体内“真空征”、假关节形成。 CT检查:①移位复杂的髋部、踝部、肱骨近端骨折,需应用CT 和(或)三维成像;②为明确关节内或关节周围骨折、椎管内压迫情况等,可考虑CT检查。 MRI检查:①可诊断隐匿性骨折;②可判断骨折是否愈合,未愈合的骨折T1WI为低信号、T2WI为高或等信号,抑脂序列呈高信号。骨扫描(SPECT/ECT):适于不能行MRI 检查的患者,有助于判断疼痛责任椎体。 2.1.3 骨密度检查 拟诊为骨质疏松性骨折的患者在条件允许时可行骨密度检查,也可在术后进行。双能X线吸收法(DXA)测定:T 值≥-1.0 SD 属正常;-2.5 SD 少;T值≤-2.5 SD为骨质疏松症;伴有一处或多处非暴力性骨折为严重骨质疏松症。 2.1.4 实验室检查 常规术前检查,必要时检查血钙磷、24 h 尿钙、25(OH)VitD、降钙素和甲状旁腺激素等。根据病情需要,有条件者可检测骨转换生化标志物(包括骨形成和骨吸收指标): ①骨形成指标包括血清碱性磷酸酶、骨钙素、骨源性碱性磷酸酶、Ⅰ型前胶原C 端肽(P1CP)和N 端肽(P1NP)。 ②骨吸收指标包括晨空腹尿钙/肌酐比值、尿吡啶啉和脱氧吡啶啉、尿Ⅰ型胶原交联C-末端肽和N端肽、血清抗酒石酸酸性磷酸酶及Ⅰ型胶原交联C-末端肽(CTX),Ⅰ型胶原交联N-未端肽(NTX)等。 ③国际骨质疏松基金会(IOF)推荐首选Ⅰ型原胶原N-端前肽和血清Ⅰ型胶原交联C-末端肽这两项指标。 ④低骨密度并高骨转换率提示骨折风险明显增加。 ⑤骨转换指标可作为敏感的疗效观察指标,一般治疗后3 个月即可见明显变化。 2.2 诊断和鉴别诊断 骨质疏松性骨折的诊断应结合患者的年龄、性别、绝经史、脆性骨折史及临床表现等因素以及影像学检查和(或)骨密度检查、骨转换生化标志物等结果进行综合分析后作出诊断。需注意与转移性骨肿瘤、胸腰椎结核、多发性骨髓瘤、甲状旁腺功能亢进、慢性肾病-矿物质骨病等多种疾病鉴别。 3 常见骨质疏松性骨折部位、特点及治疗 3.1 脊柱骨折 为最常见的骨质疏松性骨折,骨质疏松性脊柱骨折往往外伤较轻,或无明显外伤史,因此,易漏诊或误诊为腰背肌劳损。 3.1.1 临床症状、体征 ①持续腰背、胸背部疼痛,可伴胸肋部痛。平卧休息时疼痛可减轻或消失,体位改变时疼痛加重。可出现脊柱后凸畸形和脊柱骨折骨不愈合[1]。 ②查体可见胸腰部活动受限,骨折责任椎压痛、叩击痛,一般无下肢神经损害表现(但如压缩或后凸畸形严重,也可出现神经损害表现)。 ③查体结合影像学检查可确定疼痛责任椎[2]。 3.1.2 临床分型 椎体压缩呈楔形骨折、双凹骨折和垂直压缩性骨折,Genant 影像分型为:①轻度压缩骨折,在原椎体高度上压缩20%~25%。②中度压缩骨折,在原椎体高度上压缩25%~40%。③重度压缩骨折,在原椎体高度上压缩>40%。 3.1.3 治疗 3.1.3.1 非手术治疗:①适应证:症状及体征较轻,影像学检查为轻度压缩骨折、无法耐受手术者可采取非手术治疗。②治疗方法:卧床休息:一般3~4 周,腰背部垫软枕,具体根据骨折损伤程度决定。支具:下地活动时建议佩戴。对症治疗:疼痛明显者,可给予镇痛药。降钙素能减少骨折后急性骨丢失,又对缓解骨折后急性骨痛有一定效果。 3.1.3.2 微创手术治疗:①适应证:非手术治疗无效、疼痛明显;不宜长时间卧床者;不稳定压缩骨折;骨折块不愈合或内部囊性变、椎体坏死;能耐受手术。②绝对禁忌证:无法耐受麻醉、手术的患者;无痛的骨质疏松性脊柱骨折。相对禁忌证:有出血倾向者;身体其他部位有活动性感染;椎体严重压缩骨折。③治疗方法:可选经皮椎体后凸成形术(PKP)或经皮椎体成形术(PVP)[3],建议术中同时行活检术。 3.1.3.3 开放手术治疗:有神经压迫症状、体征或需截骨矫形的患者,以及不适合微创手术的不稳定骨折患者,可考虑开放手术治疗。必要时可在内固定周围采用局部注射骨水泥增强技术,以增强内固定的稳定性。 3.1.3.4 疗效评价:可采用VAS疼痛评分、Oswestry 功能障碍指数(ODI)、SF-36 等评分系统,对患者的临床症状进行手术前后量化评估。 3.2 髋部骨折 髋部骨质疏松性骨折主要包括股骨转子间骨折和股骨颈骨折,是严重的骨质疏松性骨折,一般需要外科治疗。非手术治疗主要用于不能耐受麻醉和手术的患者。非手术治疗包括卧床、牵引、支具固定、营养支持等治疗措施。髋部骨折后有超过20%的患者会在1 年内因各种并发症死亡[4],20%的患者将在1年内再次骨折[5]。 3.2.1 股骨转子间骨折 3.2.1.1 临床分型:股骨转子间骨折常采用Evans 分型和AO分型,骨折稳定性的判断十分重要,Evans Ⅰa、Ⅰb型属稳定型,Ⅰc、Ⅰd和Ⅱ型属不稳定型。 3.2.1.2 手术治疗:若条件允许,应尽早手术治疗,并推荐早期部分或完全负重活动。①髓内固定:对于稳定型和不稳定型转子间骨折均可选择髓内固定。②髓外固定:主要适用于稳定型骨折。③人工髋关节置换:仅适用于一些特殊病例,例如严重骨质疏松患者,股骨转子间粉碎性骨折依靠内固定很难达到牢靠固定;或骨折同时伴有髋关节疾病,或陈旧性骨折患者。 3.2.2 股骨颈骨折 3.2.2.1 临床分型:股骨颈骨折通常采用Garden 分型。Garden Ⅰ型及Ⅱ型为无移位的股骨颈骨折,Ⅲ型及Ⅳ型为有移位的股骨颈骨折。 3.2.2.2 手术治疗:①空心加压螺钉内固定:适用于没有移位或低移位倾向的稳定型骨折。②动力髋螺钉:适用于骨折线近乎垂直、移位倾向大的患者。③髋关节置换:用于移位或不稳定型骨折。对于高龄、活动量不大、身体条件差、合并症多,髋臼无明显退变的患者推荐采用半髋置换。其他患者可选择全髋置换。 3.3 桡骨远端骨折 常呈粉碎性、累及关节面,易残留畸形和疼痛,造成前臂、腕关节和手部功能障碍。 3.3.1 临床分型 常用人名分型,如Colles骨折、Smith骨折、Barton骨折等,近年来AO分型应用更为广泛。 3.3.2 非手术治疗 对于可恢复关节面平整及正常掌倾角和尺偏角、以及能够恢复桡骨茎突高度的桡骨远端骨折,可采用手法复位、石膏固定等非手术治疗。 3.3.3 手术治疗 对复位后桡骨短缩超过3 mm、侧位X线片示背侧成角超过10°、关节面台阶超过2 mm的患者推荐手术治疗。目的是恢复关节面的平整及相邻关节面之间的吻合关系,重建关节的稳定性以及恢复无痛且功能良好的腕关节。根据骨折的具体情况选用经皮撬拨复位克氏针内固定、切开复位锁定加压接骨板(LCP)内固定、外固定支架、桡骨远端骨折髓内钉等技术。 3.4 肱骨近端骨折 3.4.1 临床分型 目前临床应用最广泛的是Neer分型。 3.4.2 非手术治疗 无移位或轻度移位的骨折,或不能耐受麻醉或手术的体弱患者可选择颈腕吊带悬吊治疗。 3.4.3 手术治疗 对于有移位骨折的患者,目前主张早期手术。包括张力带、拉力螺钉、经皮克氏针、锁定接骨板固定、髓内钉内固定等;对于老年高龄、严重粉碎性骨折或伴肱骨头骨折的患者,可行人工肱骨头置换术。术后肩关节应进行早期功能锻炼。 4 骨质疏松性骨折的其他治疗 4.1 系统性管理 骨质疏松性骨折患者,尤其老年患者,必须对其全身状况、器官功能、风险及预后做全面评估,实施手术或非手术的综合处理。 4.2 抗骨质疏松治疗 重视围手术期抗骨质疏松治疗。大量的动物实验和临床研究显示,现有的多数抗骨质疏松药物对骨折修复和骨折愈合无不良影响。抗骨吸收抑制剂可能会使骨折修复过程中的骨痂变大,此种大骨痂也可能提供了更高的生物力学刚度和强度。规范化的常规剂量的双膦酸盐对骨折愈合无不利影响,可考虑序贯治疗[6-13]。甲状旁腺素(PTH1-34)[14-16]和维生素K2[17-19]有利于成骨。鲑鱼降钙素能减少急性骨丢失、缓解骨质疏松性骨痛,必要时可采用间歇性重复给药[20,21]。绝经后骨质疏松症的骨质吸收迅速,骨代谢转换率高,为高转换型,治疗可考虑应用骨吸收抑制剂;部分老年性骨质疏松症为低转换型,可考虑联合应用骨形成促进剂,以改善骨微结构及促进骨量形成,降低再骨折风险。患者具体属于何种转换类型,可通过测定骨代谢指标帮助判定。 4.2.1 药物治疗[22] ①基础治疗药物:维生素D、钙制剂。建议每日额外补充元素钙500~600 mg[23-25]。每日补充普通维生素D 800~1000 IU。 ②活性维生素D:老年人肾功能不全及1α羟化酶缺乏者,应补充活性维生素D,注意监测血钙与尿钙[26-29]。 ③抗骨吸收药:双膦酸盐、降钙素、选择性雌激素受体调节剂、雌孕激素替代治疗等。 ④促骨形成药:PTH1-34片段。 ⑤双向作用机制药物:活性维生素D、维生素K2等。 ⑥中药:补肾壮骨类药物、含黄酮类生物活性成分等中药(详见国家基本药物目录,2012版)[30]。 4.2.2 用药原则 4.2.2.1 骨折前已用抗骨质疏松药物者,可继续应用。 4.2.2.2 骨折前未用抗骨质疏松药物者,根据患者情况分两类进行选择:①骨折后急诊或早期进行内固定手术者,在手术后患者全身情况稳定时,建议适时进行抗骨质疏松治疗。②骨折后暂时不做手术或保守治疗患者待全身创伤反应稳定时,建议适时进行抗骨质疏松治疗。 4.2.2.3 用药注意事项:①应选用基础药物。②依据骨转换类型决定选用抗骨吸收药物或促骨形成药物。③用药前应参照药物说明书,遇有不良反应应及时停药和处理,或更换不同药物。 4.3 物理疗法 物理疗法简便、无创、有效而安全,对骨折愈合有促进作用。低强度脉冲超声(LIPUS)、脉冲电磁场(PEMF)、体外冲击波(ESWT)、功能性电刺激(FES)和振动波等多种物理治疗方法均可选用。 4.4 康复训练 骨质疏松性骨折的恢复慢,康复期长。在不影响骨折制动及骨折愈合的前提下,应尽早开始康复训练。目的是恢复关节运动功能,减少肌肉萎缩,增强肌肉力量,促进骨折愈合和防止再发骨折。建议采用主动运动与被动运动相结合,以主动运动为主的运动方式。循序渐进,避免粗暴操作。 4.5 运动疗法 以负重运动和抗阻运动为主,如:快步走、哑铃操、举重、划船、蹬踏运动等。通过负重运动和力量训练,增加肌力,改善布态和平衡,减少摔倒和骨折的风险。注意制定个体化的运动处方,因人而异的选择运动方式,频率,时间,以及强度。 参考文献 [1] Wang G, Yang H, Chen K. Osteoporotic vertebral compression fractures with an intravertebral cleft treated by percutaneous balloon kyphoplasty. J Bone Joint Surg Br, 2010, 92(11): 1553-1557. [2] Mao H, Zou J, Geng D, et al. Osteoporotic vertebral fractures without compression: key factors of diagnosis and initial outcome of treatment with cement augmentation. Neuroradiology,2012, 54(10): 1137-1143. [3] 胡侦明, 杨惠林, 王根林, 等. 经皮椎体成形术治疗的相关建议. 中华骨与关节外科杂志, 2015, 8(5): 375-376. [4] Parker M, Johansen A. Hip fracture. BMJ, 2006, 333(7557): 27-30. [5] L?nnroos E, Kautiainen H, Karppi P, et al. Incidence of second hip fractures. A population- based study. Osteoporos Int, 2007, 18(9): 1279-1285. [6] Black DM, Delmas PD, Eastell R, et al. Once-yearly zoledronic acid for treatment of postmenopausal osteoporosis.N Engl J Med, 2007, 356(18): 1809-1822. [7] Black DM, Reid IR, Boonen S, et al. The effect of 3 versus 6 years of zoledronic acid treatment of osteoporosis: a randomized extension to the HORIZON-Pivotal Fracture Trial (PFT). J Bone Miner Res, 2012, 27(2): 243-254. [8] Black DM, Reid IR, Cauley JA, et al. The effect of 6 versus 9 years of zoledronic acid treatment in osteoporosis: a randomized second extension to the HORIZON-Pivotal Fracture Trial (PFT). J Bone Miner Res, 2015, 30(5): 934-944. [9] Lyles KW, Colón-Emeric CS, Magaziner JS, et al. Zoledronic acid and clinical fractures and mortality after hip fracture.N Engl J Med, 2007, 357(18): 1799-1809. [10] Black DM, SchwartzAV, Ensrud KE, et al. Effects of continuing or stopping alendronate after 5 years of treatment: the Fracture Intervention Trial Long-term Extension (FLEX): a randomized trial. JAMA, 2006, 296(24): 2927-2938. [11] Bone HG, Hosking D, Devogelaer JP, et al. Ten years' experience with alendronate for osteoporosis in postmenopausal women. N Engl J Med, 2004, 350(12): 1189-1199. [12] Zhang ZL, Liao EY, Xia WB, et al. Alendronate sodium/vitamin D3 combination tablet versus calcitriol for osteoporosis in Chinese postmenopausal women: a 6-month, randomized,open-label, active-comparator-controlled study with a 6-month extension. Osteoporos Int, 2015, 26(9): 2365-2374. [13] Black DM, Thompson DE, Bauer DC, et al. Fracture risk reduction with alendronate in women with osteoporosis: the Fracture Intervention Trial. J Clin Endocrinol Metab, 2000,85(11): 4118-4124. [14] Neer RM, Arnaud CD, Zanchetta JR, et al. Effect of parathyroid hormone (1-34) on fractures and bone mineral density in postmenopausal women with osteoporosis. N Engl J Med, 2001, 344(19): 1434-1441. [15] Fahrleitner-Pammer A, Langdahl BL, Marin F, et al. Fracture rate and back pain during and after discontinuation of teriparatide: 36-month data from the European Forsteo Observational Study (EFOS). Osteoporos Int, 2011, 22(10):2709-2719. [16] Chen JF, Yang KH, Zhang ZL, et al. A systematic review on the use of daily subcutaneous administration of teriparatide for treatment of patients with osteoporosis at high risk for fracture in Asia. Osteoporos Int, 2015, 26(1): 11-28. [17] Iwamoto J, Seki A, Sato Y, et al. Vitamin K2 promotes bone healing in a rat femoral osteotomy model with or without glucocorticoid treatment. CalcifTissue Int, 2010, 86(3): 234-241. [18] Cockayne S, Adamson J, Lanham-New S, et al. Vitamin K and the prevention of fractures: systematic review and metaanalysis of randomized controlled trials. Arch Intern Med,2006, 166(12): 1256-1261. [19] Huang ZB, Wan SL, Lu YJ, et al. Does vitamin K2 play a role in the prevention and treatment of osteoporosis for postmenopausal women: a meta- analysis of randomized controlled trials. Osteoporos Int, 2015, 26(3): 1175-1186. [20] Lyritis GP, Paspati I, Karachalios T, et al. Pain relief from nasal salmon calcitonin in osteoporotic vertebral crush fractures.A double blind, placebo-controlled clinical study. Acta Orthop Scand Suppl, 1997, 275: 112-114. [21] Tsakalakos N, Magiasis B, Tsekoura M, et al. The effect of short- term calcitonin administration on biochemical bone markers in patients with acute immobilization following hip fracture. Osteoporos Int, 1993, 3(6): 337-340. [22] 朱汉民, 邱贵兴, 李梅, 等. 原发性骨质疏松症的治疗与预防. 中华骨与关节外科杂志, 2015, 8(5): 377-384. [23] Khan A, Dubois S, Khan AA, et al. A randomized, doubleblind,placebo- controlled study to evaluate the effects of alendronate on bone mineral density and bone remodelling in perimenopausal women with low bone mineral density. JObstet Gynaecol Can, 2014, 36(11): 976-982. [24] Roberts KC, Brox WT. AAOS Clinical Practice Guideline:Management of Hip Fractures in the Elderly. J Am Acad Orthop Surg, 2015, 23(2): 138-140. [25] Cosman F, de Beur SJ, LeBoff MS, et al. Clinician's Guide to Prevention and Treatment of Osteoporosis. Osteoporos Int, 2014, 25(10): 2359-2381. [26] Larsen ER, Mosekilde L, Foldspang A. Vitamin D and calcium supplementation prevents osteoporotic fractures in elderly community dwelling residents: a pragmatic population-based 3- year intervention study. J Bone Miner Res,2004, 19(3): 370-378. [27] Moyer VA, U.S. Preventive Services Task Force. Vitamin D and calcium supplementation to prevent fractures in adults:U.S. Preventive Services Task Force recommendation statement.Ann Intern Med, 2013, 158(9): 691-696. [28] Avenell A, Mak JC, O'Connell D. Vitamin D and vitamin D analogues for preventing fractures in post- menopausal women and older men. Cochrane Database Syst Rev, 2014,4: CD000227. [29] Papadimitropoulos E, Wells G, Shea B, et al. Meta-analyses of therapies for postmenopausal osteoporosis. Ⅷ: Metaanalysis of the efficacy of vitamin D treatment in preventing osteoporosis in postmenopausal women. Endocr Rev,2002, 23(4): 560-569. [28] 中华人民共和国国家卫生和计划生育委员会.《国家基本药物目录》(2012 年版). 2013-05-01.
3561人已读 - 引用 髋关节术后康复指南2 完
应该的避免危险动作最开始活动时避免过度活动,否则会导致关节脱位,理疗师会讲述什么动作需要避免,最危险的动作是什么:坐 不能使你的膝关节交叉过身体中线错误→双足置于地上,双膝关节之间保持6英寸距离。正确→转身 避免将足固定而旋转患侧髋关节。错误→应该同时转动躯干和患足。正确→弯腰 不能完全弯腰错误→正确的做法是以一种装长柄抓钩延长正确→当你在家时应注意:1遵循外科医师的指导是非常重要的,指导意见是主治医师在出院之前决定的。2如果需要使用助行器或者拐杖,向医生问明患者可以负多少重量。3记得你会较平时更容易疲劳,可以计划每天上午十点左右和下午3点左右休息30-60分钟。4充分利用双臂起落座椅是比较安全和简单的做法,避免坐过低和厚软垫座椅。坐起的时候可以用电子或者枕头垫高垫着。5利用高位马桶在起来和坐下来时可以减少髋关节和膝关节的应力。6为了增加安全性和舒适度,洗浴时可以坐在浴缸座上。7使用长的搓澡巾可以到达下肢,女患者可以购买剃刀给自己的腿剃面。8避免扫地、拖地和使用吸尘器,用长把手羽毛单子打扫高位和地位置的灰尘。你的主治医师会告诉你什么时候可以扫地、拖地和使用吸尘器。9你可以乘坐轿车,但是必须按照医生的知道上下车,用枕头垫高车上的坐垫保护髋膝关节。10医生会告诉你什么时候可以驾车,一般情况下在手术后4-6个星期,如果你的汽车是手动变速器,医生会告诉你驾驶注意事项,确信你在驾驶时刹车没有不舒服。11便秘是患者术后最常见的问题,便秘可限制活动和止痛药物的应用。12主治医生会给你止痛方案,请按遗嘱服药物。13伤口周围稍微隆起是正常的,穿宽松的衣物可以减少对伤口的压力,找主治医生或者有许可证的专科医生做适当的伤口护理
894人已读 - 引用 膝关节置换病友联谊会
亲爱的患者朋友:为普及膝/髋关节疾病和关节置换知识,大坪医院关节外科将定期举办“关节置换病友联谊会”,邀请曾接受过关节置换和需要进行置换手术的患者朋友们参加。联谊会将采取知识讲座、病友座谈会、专家现场解答的形式,讲解关节疾病和置换手术知识,安排病友们介绍关节置换术后功能锻炼和保养的体会,并由关节外科专家就患者最关心的话题进行现场解答。中老年膝关节疾病的治疗时间:2013年5月18日(周六) 下午 14:00-16:00地点:大坪医院“第一住院部”C区三楼骨科会议室病友还可带上病历等资料到现场进行免费咨询。到场的病友都有一份精美礼品相送。欢迎您们的积极参加!
熊雁 副主任医师 陆军特色医学中心(大坪医院) 关节四肢外科1699人已读 - 引用 John N. Insall,MD (1930-2000) —— 现代人工膝关节之父
尽管现代人工膝关节置术的历史可以追溯到20世纪40年代,但真正的成功还是从1973年John N. Insall引入骨水泥固定的全髁膝(Total Condylar Knee)开始的。至今,全髁膝已成为评价后续数十种人工膝关节假体的金标准(15年随访,假体存留率94%),Insall因此被许多人称为现代人工膝关节之父。1930年6月19日,Insall出生在英国的博内茅斯,这是位于南安普敦西南部英吉利海峡入口的一个小村镇。他先后就读于剑桥大学和伦敦医院医学院,1956年毕业。随后他接受了总共5年的医院训练,2年在英国,3年在加拿大蒙特利尔。1961年,他作为纽约特种外科医院(HSS)矫形外科的fellowship人员而来到美国。当这一奖学金计划完成后,他返回英国,行了两年医。1965年,他重回HSS,当骨科主治医生,之后又成为膝关节组的主任,直到1991年。在1980年-1991年,他还同时担任康奈尔大学医学院的骨科教授。1991年,他与两位同行共同创建了Insall Scott Kelly(ISK)矫形外科与运动医学学院。1996年,他还被聘为阿尔伯特.爱因斯坦医学院矫形外科的临床教授。显然,Insall杰出贡献中的大部分是在HSS期间完成的。如前所述,他于1973年引入了全髁膝。实际上这绝不是一个一蹴而就的发明,而是经过了多年漫长的努力。Insall很早就开始对膝关节感兴趣,四十多年前就在JBJS上发表过有关截骨治疗膝关节骨性关节炎的文章。因此,全髁膝的问世只能认为是一种最后的水到渠成。虽然全髁膝的成功确立了Insall在骨科史中的地位,但他并未因此罢手。1978年,他又与工程师Albert Burstein博士合作,推出了Insall-Burstein后稳定膝。这一假体一度风靡全球。再之后,他还与人合作,从事旋转平台膝关节假体的研制。还推出了颇受好评的Legacy Knee。另外,在人工膝关节领域,Insall的贡献是全方位的,除外提出手术理念(比如全膝置换术中切除后交叉韧带就是他首先提出来的)、设计假体,他还热衷于配套手术器械的研制、手术切口的设计、膝关节功能的评价、患者的术后随访等等。与许多杰出的骨科先驱一样,Insall不仅是个优秀的发明家、高超的手术医生,还是一个出类拔萃的教育家。他为重要的医学教科书写过超过35章的内容,发表过150多篇文章。他的代表作《膝关节外科》已经出到第三版,并被译成多种文字,成为这一领域里的经典著作。他是许多全国性学术会议的主要讲演人,也是许多固定性学术讲座的重要报告者。他担纲的住院医生计划曾先后培养过60余位膝关节外科医生(其中的一些是眼下享誉世界的该领域的专家)。他们组织了一个Insall俱乐部,每年聚会一次,交流手术经验及研究进展。他是1983年成立的膝关节学会的创始人之一,并在1987年担任这一学会的主席。为眼下广泛应用的膝关节功能的膝关节学会评分系统(Knee Society scoring system)的设立作出了重要贡献(当然,另一个常用的膝关节功能评分系统——HSS评分,与他也不无关系)。学会为了纪念他的贡献,设立了Insall 奖(Insall Award),用于表彰年会上交流的有关临床效果和手术技术的杰出论文。无论是在公开场合还是私底下,Insall均被人看作是标准的英国绅士。能与人谈论几乎所有话题,却不会与人争执。他热爱高尔夫球、钟情在世界各地旅行。1999年5月,人们惊悉他患了肺癌,且已发生转移。从此他不再露面。在他生命的最后一年,Insall在家人的陪伴下回到康涅迭格州的海边,静度余生。差不多的20世纪的最后一天(2000年12月30日),Insall安静地告别了人世。
熊雁 副主任医师 陆军特色医学中心(大坪医院) 关节四肢外科3216人已读 - 引用 EULAR推出髋关节骨关节炎治疗指南
1998年,欧洲抗风湿病联盟(EULAR)通过专门工作组开始制定膝及髋关节的骨关节炎(OA)治疗指南。膝关节OA治疗指南于2000年发表,并于2003年进行了修订(见附录)。在2004年的EULAR会议上,该工作组首次推出髋关节OA治疗指南。制定髋关节OA治疗指南的过程分3步完成。首先,每位成员分别独立提出10条治疗方面的建议,然后通过3轮遴选产生最终10条。第二步,工作组系统研究每条建议。最后,工作组在综合考虑指南中各项建议的效果、安全性、可行性及费用的前提下形成共识。EULAR推荐的2004年髋关节OA治疗指南的10条建议如下:1.对乙酰氨基酚(最多4 g/d)有效且安全,在轻中度疼痛时首选,如有效,可长期口服。2.对乙酰氨基酚疗效欠佳的患者可加用或改用最小有效剂量NSAID。可能有胃肠不良反应的患者,可选用非选择性NSAID加胃保护剂或选择性COX-2抑制剂。3.硫酸葡聚糖胺、硫酸软骨素、双醋瑞因、非皂化鳄梨豆、透明质酸等可缓解症状且毒性低,但作用较弱。4.镇痛药与对乙酰氨基酚合用或单独使用,对于NSAIDs无效和/或耐受性差的患者是一种有效的替代治疗方法。5.关节内皮质激素注射(超声或X线引导下)可用于镇痛药或NSAIDs疗效欠佳的患者。6.非药物治疗应包括常规患者教育、锻炼、辅助工具(拐杖、鞋垫)应用以及肥胖患者减轻体重。7.对于顽固性关节疼痛或残疾并有影像学证据的髋关节OA患者,应考虑进行关节置换术。8.关节修复等手术可用于具有症状性髋关节OA的年轻患者,尤其是发育不良或内外翻畸形的患者更为适用。9.理想的治疗方法应包括非药物与药物治疗的联合应用。10.治疗方案应依据以下因素选择:a.髋关节OA危险因素(肥胖、不良力学因素、机体活动度、发育不良);b.一般危险因素(年龄、性别、伴随疾病和伴随用药);c.疼痛强度、残疾及功能障碍程度;d.组织破坏的部位和程度;e.患者的期望和要求。
熊雁 副主任医师 陆军特色医学中心(大坪医院) 关节四肢外科2576人已读



