河南省肿瘤医院放射介入科科普号
- 精选 肝癌的早期检出首选哪种影像检查?
肝癌的早期检出首选MRI的平扫加动态增强,因为MRI成像具有多序列、多参数等特点,而且软组织分辨率高,也就是能够显示毫米级的病变微小的变化,能够将肝硬化结节和早期肝癌区分出来!对于不容易发现和鉴别的早期肝癌,使用肝脏特异性MRI对比剂进行检查,有助于提高诊断准确性!
曲金荣 主任医师 河南省肿瘤医院 医学影像科250人已读 - 精选 一例胃造瘘患者造瘘管的更换及一点思考
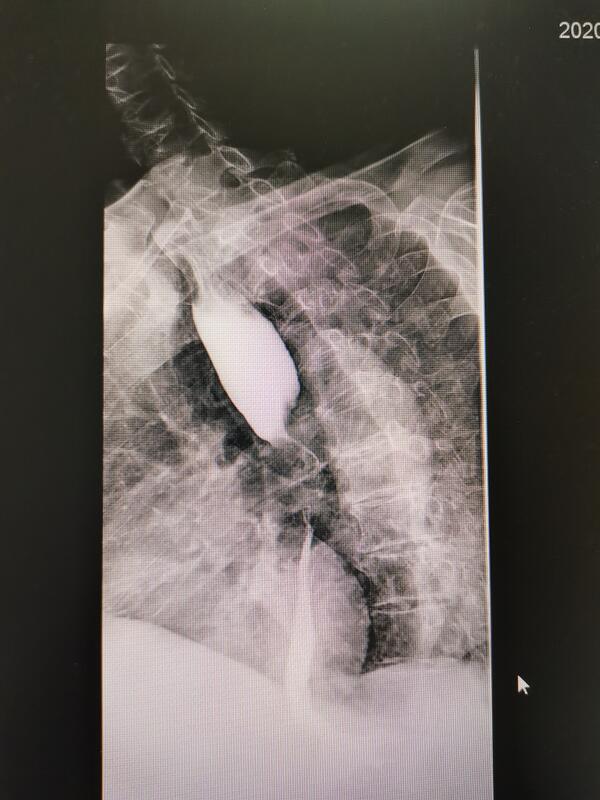
患者是食管癌放化疗后进食困难,营养差且高龄,让我们团队会诊看是否可以改善进食,对于食管癌导致不能进食的患者改善饮食的方法一般三种:营养管植入、支架,还有就是胃造瘘。考虑到病人年龄较大且有放疗史,我们担心出现肺炎及食管支架植入后遗症,和家属沟通后决定做胃造瘘。 虽然病人年龄较大85岁,因为微创,手术很顺利 2月后病人打电话说胃造瘘的地方有疼痛,通过造瘘管打饭也不太顺畅,我们建议她复查一下 于是我们通过原来的瘘口费了挺大劲重新更换了一个造瘘管 重新更换造瘘管3月后复查CT提示造瘘管位置良好 造瘘口脱出很少见,常见的原因是局部感染,营养不良,撕扯,造瘘管破裂。对于肿瘤病人来说由于很多种原因病人进食多了腹胀,进食少了反而感到舒服,这往往让家属或病人产生误解以为不需要进食那么多,实际上肿瘤病人由于消耗较正常人多反而需要比正常人更多的营养。还有营养不良的病人会更容易感染也会让管子脱出来。造瘘管脱出来最常见原因还是营养不良,我们追问病史发现病人每日通过造瘘管注入的营养液明显不够,我们就让她增加注入量后来复查就没有再出现脱出。
 肖金成 主任医师 河南省肿瘤医院 微创介入科1444人已读
肖金成 主任医师 河南省肿瘤医院 微创介入科1444人已读 - 精选 肝癌合并下腔静脉癌栓介入治疗效果好
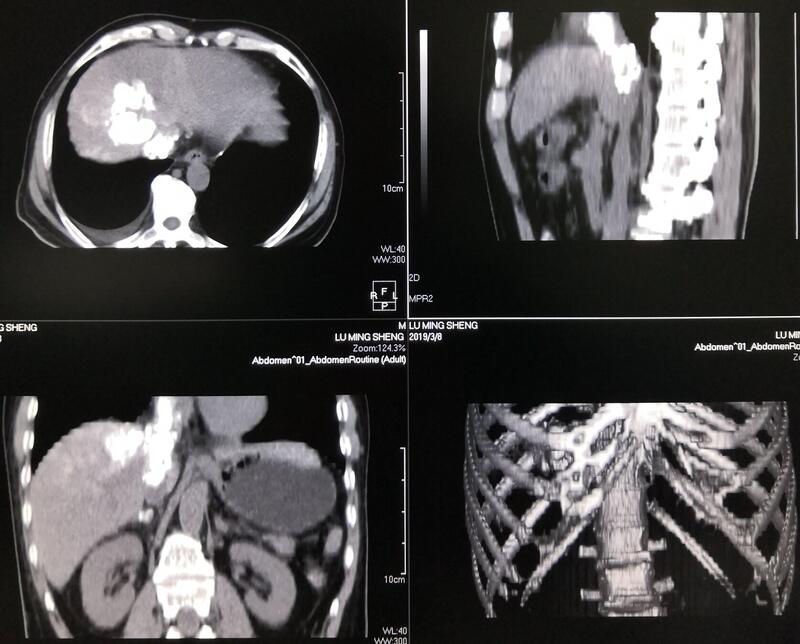
在肝癌确诊以及治疗过程中,下腔静脉癌栓的发生率大约占4%,一旦出现下腔静脉癌栓,患者预后极差,自然生存期极短,半年生存率约23%,一年生存率为0。下腔静脉癌栓可采用的治疗措施包括:一、外科手术(肝内原发肿瘤切除+癌栓取出术),中位生存期18.2个月(也就是说50%的患者活不过18.2个月);二、肝动脉化疗栓塞联合放疗(TACE联合放疗),中位生存期11.7个月。无论是外科手术还是TACE联合放疗,疗效都不能令人满意。文献报道的TACE联合放疗比外科手术疗效更差的原因未必是治疗方法有问题,而是TACE治疗未能做到精准栓塞。就如其他行业一样,用同样的方法,有人造出的是精品,有些人造出来的可能是次品。本人近两年收治了6例肝癌合并下腔静脉癌栓的患者,仅采用动脉化疗栓塞就取得了比外科手术切除更理想的疗效。中位生存期长达21个月。其中三例患者达到影像学完全缓解(国际通用的MRESIST评价标准)。之所以能够取得如此令人鼓舞的结果正是来自于术者的精准栓塞,使患者肝内原发病灶和下腔静脉内癌栓都得到彻底的栓塞。 图片中肝内和下腔静脉内白色的部分即为动脉栓塞后肿瘤和癌栓内充填的碘油栓塞剂。
 程洪涛 副主任医师 河南省肿瘤医院 微创介入科2064人已读
程洪涛 副主任医师 河南省肿瘤医院 微创介入科2064人已读 - 精选 痔疮也能介入治疗
痔动脉栓塞同事的家人,混合痔,严重时排便后痔疮内痔脱出不能还纳,疼痛难忍,还坚决排斥外科手术,长期受痔疮折磨,一周前做了介入治疗,介入术后3天出院,痔疮显著缩小,症状缓解。作为医生,看到患者症状缓解真的是无比欣慰。鉴于患者隐私,不能拍照。
程洪涛 副主任医师 河南省肿瘤医院 微创介入科2666人已读 - 精选 大肝癌的治疗
病例1:男性,52岁,肝左叶巨块型肝癌,发病时AFP>1210ng/mL。箭头所示为肝左叶巨块型肝癌TACE后情况,其中白色团块为TACE治疗时注入肿瘤内的碘油,箭头边缘为肿瘤边缘。射频消融后MRI显示肿瘤完全坏死,AFP降至20ng/mL以下。患者射频消融后已生存5年,至今无复发,无进展。病例2 男性,52岁,肝右叶膈肌下巨块型肝癌,AFP1100ng/mL。确诊未治时增强CT,箭头所指为肝右叶巨块型肝癌。TACE治疗后,CT可清晰显示肿瘤边界。射频消融后肿瘤完全坏死,AFP降至20ng/mL以下。至今已34个月无复发无进展。 病例3 女性,66岁,肝右叶巨块型肝癌。TACE后行微波消融术微波消融后MRI示肿瘤完全坏死。至今已23个月无复发无进展。病例4 男性,43岁,肝右叶肝癌,TACE后微波消融。发病至今14个月,微波消融后13个月。至今无复发无进展。
程洪涛 副主任医师 河南省肿瘤医院 微创介入科1355人已读 - 精选 TACE联合索拉非尼治疗原发性肝癌并肺转移
病例特点:原发性肝癌Ⅱb期(中国肝癌临床分期)合并慢性乙型病毒性肝炎患者进行TACE联合口服索拉非尼治疗及抗病毒治疗。肝内原发灶达CR,肺内转移灶达PR,生存期达3年4个月(至今)。病 史:男性,55岁,因“持续性右上腹隐痛”就诊,CT提示肝右叶巨块型肝癌,无血管侵犯及肝外转移(Ⅱb期)。乙肝病史30年,ALB 83U/L, HBVDNA 5×10 ^5/ml,诊断原发性肝癌,慢性乙型病毒性肝炎。行5次TACE治疗, 首次TACE后口服索拉非尼治疗,抗病毒治疗。治 疗:TACE 3次/ 前6个月内,第4次/第10个月,第5次/第1年11个月后。首次TACE后口服索拉非尼400mg bid。口服5个月时因2度不良反应减半量1周,后因3度不良反应停药2周,出现肺转移。之后不良反应控制,半量索拉非尼1周后加为足量口服至今。口服阿德福韦脂10mg qd至今。疗效评价:肝内原发灶达CR,肺内转移灶达PR,生存期达3年4个月(至今)。KPS评分100分,HBVDNA阴性,肝功Child A级。不良反应:4周出现1级手足皮肤反应,5个月手足皮肤反应加重2级, 对症处理7日后因症状加重为3级而停药2周。继续对症治疗,不良反应减为1级。经验分享:1. TACE联合索拉非尼可更有效控制肿瘤生长, 延长生存期。2. 索拉非尼不良反应可控制,出现不良反应的患者可以获得更好的生存期和疾病控制率 。3. 索拉非尼可以显著延长患者TACE的时间,减轻肝损伤,提高生存质量。。4. 重视抗肝炎病毒治疗 。5. 强调”身、心”治疗,提高沟通的技巧,重视沟通及随访。图1:治疗前CT提示肝内巨块型肝癌图2 经介入治疗DSA肝动脉造影肝内肿瘤已无活性。图3 复查CT提示肝内病灶碘油沉积较实密。图4 复查肺内转移瘤出现(图内白色小圆球)图5,口服索拉非尼后肺内转移灶明显缩小
郑琳 主任医师 河南省肿瘤医院 微创介入科2832人已读 - 引用 MRI在食管疾病的新应用
长期以来,食管癌一直困扰着人类的健康,食管癌是第7种最常见的恶性肿瘤类型,也是第6大癌症相关死亡原因,其死亡率占所有恶性肿瘤的5.3%。河南省是全世界食管癌高发区。超声胃镜(EUS)是食管病变最常用的检查方式,但是由于部分食管病变腔内生长致超声探头无法通过病变位置,而且目前临床上采用的检查方法EUS以及CT、PET-CT由于存在不同客观因素的限制,在诊断和分期上均不能满足临床需求。而传统的MRI在检查食管病变时面临很多挑战,主要原因是食管位于纵隔后方,成像时受许多运动相关的因素影响,如呼吸运动,心跳,食管自身蠕动和胸腔内的气体等,这些因素会导致磁场的不均匀,进而导致图像的磁敏感伪影,使活体的食管壁的层次显示依然存在许多技术难点。本课题组在国际上率先将MRI新技术应用于活体的食管,不断探索及优化MRI新技术的扫描方案及参数,建立了可用于食管诊断、分期的影像学技术规范,取得了突破性进展。食管癌根治切除术可以使早期食管癌(T1b、T2期)患者获得最长的无进展生存期,T3和T4a期是可切除的,而没有淋巴结转移的T3、T4a期患者接受术前新辅助化疗可以明显延长无进展生存期,对于不可切除食管癌,放化疗是首先的治疗方式。因此,术前精准T分期对食管癌治疗方式的选择及预后至关重要。在MRI上,食管腔由内向外的表现为正常黏膜层为低信号,黏膜下层为高信号,而肌层则又表现为低信号,肿瘤则可能为低信号或者高低信号混杂。我们采用MRI新技术对食管癌T分期进行了研究并于EUS的准确性进行了对比,在T1、2分期中,MRI新技术与EUS的准确性相当,而对T3、4病变的分期,MRI新技术的准确性要明显高于EUS(90.9%vs68.2%)。另外由于新辅助治疗会肿瘤发生细胞水肿、炎症坏死等,传统MRI在区分新辅助化疗后T分期的准确性有限。我们利用新辅助治疗后MRI新技术根据肿瘤治疗后肿瘤信号强度改变肿瘤强化,区分治疗后水肿、坏死及残余肿瘤,从而对肿瘤准确分期,使无创、实时、多次检测食管癌新辅助治疗后T分期成为可能。在过去的几十年里,许多内镜手术,包括内镜黏膜切除术、冷冻疗法和射频消融术,已被用于治疗黏膜内癌。但是,9%的侵犯粘膜肌层的食管癌病例中出现淋巴结转移,20%侵犯粘膜下三分之一的食管癌出现淋巴结转移。早期浸润性癌(EIC)、淋巴结转移可能性高的患者应考虑手术切除和淋巴结清扫。而对于高级别瘤变(MHN)及淋巴结转移可能性低的患者,考虑内镜或手术局部切除。因此,准确评估粘膜下侵犯情况对决定治疗的选择至关重要。我们研究了MRI在鉴别食管粘膜高级别肿瘤(MHN)和早期食管鳞癌(EISCC)中的能力,分析了病变形态、DWI信号、T2信号、强化特点及强化程度5个特征的鉴别能力,发现这5个特征均有鉴别能力,尤其是强化程度,MHN呈现明显强化,而EISCC无或轻度强化,我们还发现“心形”是MHN病灶典型的特征表现。除此之外,结合临床实际需求,我们发现MRI在很多方面都可以发挥临床价值。首先,食管MRI弥补了超声内镜因食管病变较大、侵犯较深时评价病变深度不易的局限性,特别是对那些食管癌局部进展晚期致管腔明显狭窄的患者,超声内镜无法通过病变段而导致无法评估病变分期的难题。第二、对于放化疗后的食管癌病变,由于水肿、坏死等的存在,CT无法正确区分病变的范围,对新出现的异常影的性质判定更是困难,而MRI可以结合多个序列信号的特点以及优越的软组织分辨率,清楚地分辨出病变的位置,在准确定位基础上进一步判断病变的性质。第三、食管癌术后吻合口瘘是常见的并发症,PET/CT上常常表现为不规则肿块影,而且由于炎症的原因表现为高代谢,很容易误认为肿瘤复发,但是根据形态、DWI等序列的信号及强化特点做出明确诊断。第四、MRI对食管其他病变也有良好的诊断作用。例如,食管的胃肠间质瘤(GISTs)和平滑肌瘤,二者都是粘膜下病变。平滑肌瘤GISTs占食管良性肿瘤的80%。平滑肌瘤肿块边缘光滑,食管远端多发,正常侧食管壁不增厚,软组织肿块周围界线清楚,在CT或MRI上与肌层相比呈等密度/信号,增强呈中等强化。1-3%的GISTs起源于食管,有恶变潜能。GISTs位置更远端、病变更大、密度/信号更不均匀,强化更明显,少数可出现粘膜溃疡,PET高代谢。近年来,我们应用MRI新技术在食管病变中的应用开展了大量研究,包括MRI评估食管癌分期、疗效及预后等,总结了食管癌的诊断和鉴别诊断特点,发表了很多篇中英文文章。另外,影像组学是目前的研究热点,与传统影像形态学的改变相比,应用影像组学特征不仅能提高诊断准确率,还能提供传统影像特征无法提供的信息。淋巴结性质的判定一直是困扰临床的难题,我们率先利用MRI影像组学特征评估其食管癌淋巴结转移中的价值,发现MRI影像组学特征有术前预测淋巴结转移的潜能。2020版中国临床肿瘤学会(CSCO)食管癌诊疗指南首次加入食管MRI检查并引用了我们的研究成果。MRI在食管疾病中应用前景得到了大家的关注与认可,随着未来更多研究的开展,MRI会在食管疾病诊治中发挥更大的价值。
曲金荣 主任医师 河南省肿瘤医院 医学影像科339人已读 - 引用 宫颈癌已经明确诊断,为什么治疗前医生还让我做磁共振检查?
宫颈癌明确诊断比较容易,通常妇科检查活检就可以确诊,但是确诊后医生还是会让患者再做磁共振检查,这是因为宫颈癌治疗方法的选择取决于病变的大小、与宫颈外膜的关系、与周围结构的关系等,而这些细节信息的显示目前主要靠磁共振检查,磁共振检查本身的特点能够将这些信息比较准确地显示出来!所以宫颈癌患者治疗前的影像学检查首选磁共振。
曲金荣 主任医师 河南省肿瘤医院 医学影像科408人已读 - 引用 直肠病变首选影像学检查是什么?
直肠病变首选的影像学检查是MRI, 无论良恶性病变,MRI可以明确病变的位置、范围、浸润深度和邻近周围结构的情况,通过上述征象的详细评估,以此作为下一步治疗方法的选择依据。MRI和CT比较,MRI能更好地显示肠管的层次结构,所以它是直肠病变影像学检查的首选!直肠MRI检查前要求清洁肠道,以避免肠内容物的干扰、影响对病变的显示!
曲金荣 主任医师 河南省肿瘤医院 医学影像科291人已读 - 引用 手术技巧之肺癌背侧野小病灶的消融治疗
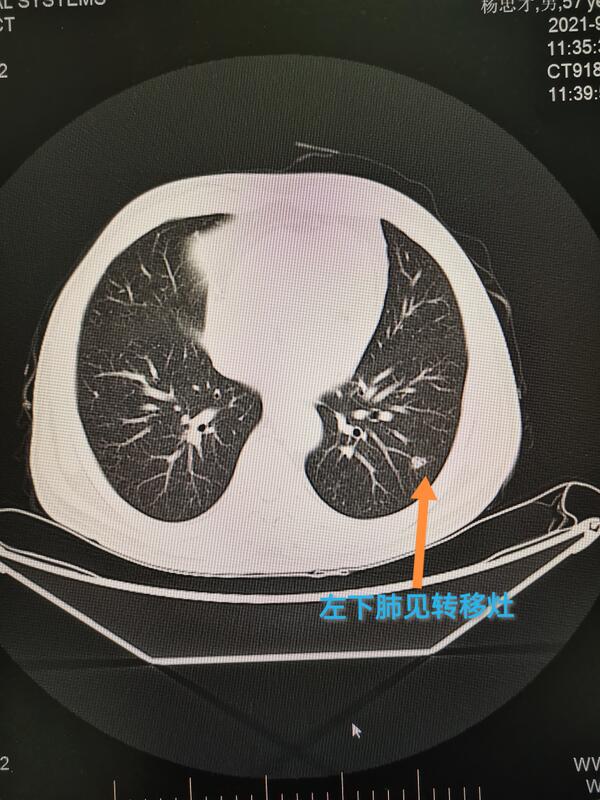
现在肺部小结节肿瘤的消融治疗因其损伤小、效果好、能最大限度保护肺功能已经越来越得到大家的认可。目前行肺部肿瘤的消融治疗采取的麻醉方式一般分局麻和全麻,二者各有优缺点,但对于病灶较小、位于下叶或者因年龄或其他原因不能很好配合者采取全麻会有更好的效果。但采取全麻时病人的背侧肺野在CT上会呈现出大片带状毛玻璃影从而使得靠近背侧肺野的小病灶无法显现而影响治疗。最近我们和麻醉科密切配合有效解决了这个问题。 这是一个直肠癌患者,术后化疗后,左肺下叶发现转移灶。 全身其他部位连续3个月未发现其他病灶,经MDT会诊后拟行消融治疗,我们选择了微波消融。全麻后采取仰卧位发现靠近背侧肺野大片毛玻璃影(所有全麻病人都有此征象),无法确认病灶位置。 我们开始认为是坠击性肺炎,采取抬高患侧部位,依然无法确认病灶 我们决定采取俯卧位(已经全麻了啊,真应该感谢麻醉科的那位兄弟),依然无法搞清楚 现在尴尬了,做还是不做?学术问题现在变成了哲学问题,一番心灵拷问再加上和麻醉医生沟通,决定减少正压通气量试试,然后奇迹出现了 看到病灶后,治疗就简单多了。治疗顺利完成。 其实全麻病人都会出现这种情况,原因有认为是坠积性炎症,有认为是全麻后肺内充气不完全有关,和麻醉医生沟通后认为正压通气遇到坠击可能会出现这种情况。现在俯卧位的肺内病灶是解决了了,下回准备搞个仰卧位的肺内病灶试试看。
 肖金成 主任医师 河南省肿瘤医院 微创介入科595人已读
肖金成 主任医师 河南省肿瘤医院 微创介入科595人已读



