金城江区人民医院科普号
- 精选 亚急性甲状腺炎诊疗新进展(转载)
亚急性甲状腺炎(subacute granulomatous thyroiditis,SAT),又称De Quervain甲状腺炎或巨细胞性甲状腺炎。本病常发生于病毒性上呼吸道感染之后,是颈前肿块和甲状腺疼痛的常见原因[1]。多数学者认为该病是一种可自行恢复的甲状腺非细菌感染性疾病,多是由病毒(柯萨奇病毒、EB病毒、腺病毒、埃可病毒、流感病毒及HIV等)感染后引起的变态反应[2],同时易感者也可能存在着自身免疫功能的异常。近年来许多科学工作者做了大量的SAT与病毒感染关系的研究工作[3],但病毒感染究竟在发病中起何作用,或只是一个不相干的事件还存在争议[4]。该病临床表现多种多样,特别是不典型的SAT与其他甲状腺疾病不易区分,易造成误诊,现就目前该病临床特点及诊断与治疗综述如下。 1 临床特点 本病的发病与季节变化密切相关,夏、初秋季节高发,女性发病率明显高于男性,约7∶1,尤以中青年女性发病率为高,中位年龄48岁[5]。通常发病前1~2周有前驱感染史,起病较急,典型病例可分为3期,分别是急性期(伴甲状腺功机能亢进),缓解期(伴甲状腺功机能减退,分过渡期和甲减期2期)和恢复期(甲状腺功能正常期)[6]。临床表现多数为甲状腺突然肿胀、疼痛、发硬及吞咽困难,可伴患侧耳屏处放散痛。常始于甲状腺的一侧,很快向腺体其他部位扩展。患者可有发热、血沉增快[1]。本病病程长短不一,可自数周至半年以上,一般为2~3个月,故称SAT。病情缓解后,长时间内仍有复发可能[7]。 2 诊断标准 ①甲状腺肿大、疼痛、质硬、有触痛,常伴上呼吸道感染的症状及体征:发热、乏力、纳差、颈部淋巴结肿大等;②红细胞沉降率加快;③一过性甲状腺功能亢进;④131I摄取率受抑制;⑤甲状腺自身抗体甲状腺微粒体抗体(TMAb)、甲状腺球蛋白抗体(TGAb)阴性或低滴度;⑥甲状腺穿刺或活检,可见多核巨细胞或肉芽肿改变。符合上述6条中的4条即可诊断SAT[8]。 3 诊断的进展 3.1 临床表现 起病前1~3周常有病毒性咽炎、腮腺炎、麻疹或其他病毒感染的症状,表现为甲状腺区的明显疼痛,可放射至耳部,吞咽时疼痛加剧[9],本病亦可有声音嘶哑及吞咽困难。但应值得注意的是,如患者缺少甲状腺局部疼痛,并不能排除SAT诊断。多数患者的症状于起病后3~4 d达到高峰,起病1周内,通常会出现甲状腺功能亢进的表现,包括精神亢奋,心悸乏力,颤抖多汗,长期以往患者则会表现为体重下降,伴有明显的倦怠感,这是本病的特点之一[10]。触诊甲状腺呈轻度到中度肿大,质地硬,伴结节,触痛明显,常可见到一叶甲状腺受侵较另一叶严重,在受到侵犯的甲状腺上的皮肤有发红、温暖。病情起伏波动持续3~6周,多于几月内消退,不遗留甲状腺功能异常。也有部分患者病情好转后,在数月可再次或可有多次病情复发或加重,少数最终变为甲状腺功能减退。 3.2 实验室检查进展 据实验室结果本病可分为3期,即甲状腺毒症期、甲减期和恢复期。①甲状腺毒症期:血清总三碘甲状腺原氨酸(T3)、总甲状腺素(T4)升高,促甲状腺素(thyroid stimulating hormone,TSH)降低,131I摄取率减低(24 h100 mm/h。②甲减期:血清T3、T4逐渐下降至正常水平以下,TSH回升高于正常值,131I摄取率逐渐恢复。③恢复期:血清T3、T4、TSH和131I摄取率恢复至正常[9,11]。在甲状腺显像方面,其结果受炎症严重程度的影响很大,当病变严重累及双侧甲状腺时,可表现为颈部组织放射性本底增高明显,甲状腺显像模糊,轮廓不清,甚至不显像。当病变只累及甲状腺某一部位时,临床上可扪及边界不清的肿块,甲状腺显影可见肿块部位呈放射性稀疏、缺损区。近年来随着技术的发展,Rao等[13]提出可通过测定唾液C反应蛋白(Salivary C-Reactive Protein)达到诊断和鉴别SAT的目的。它具有灵敏度高、无创、方便、快捷等优点,在临床上值得今后推广应用。 3.3 B型超声多普勒仪检查进展 SAT的B超声像图特征可描述为:单侧或双侧甲状腺肿大,病变若累及腺体被膜,则病灶处被膜连续性被打断,与颈前肌群分界欠清。甲状腺实质内出现弥漫性和局限性衰减的片状低回声,回声从外向内逐渐减低,有的患者甚至形成"假囊肿",即腺体内小片局部液化区;在回声减低的甲状腺内出现单个或多个低回声或无回声区,形态多不规则,偶可见钙化;CDFI检测显示正常甲状腺组织血流无变化,低回声区边缘血流信号稍增多。同时对甲状腺低回声区加压扫查时,表现为明显的压痛,此症状具有较高特异性,在其他甲状腺疾病中较为少见[14,15]。随着技术的发展,实时超声弹性成像技术也逐渐运用到SAT的诊断中。其原理是不同组织间的弹性系数不同,在受到外力压迫后组织发生变形的程度就不同,而将受压前后回声信号的变化转化为实时彩色图,可反映出组织硬度的信息。这项技术早先被应用于甲状腺良恶性肿瘤的鉴别,近来Xie Ping等[16]通过临床研究提出实时超声弹性成像技术对于鉴别SAT和结节性甲状腺肿有统计学意义。 3.4 电子计算机X射线断层扫描技术(CT) SAT的CT表现有一定的特征性:甲状腺体积多肿大,病变处甲状腺边缘模糊,与正常甲状腺组织界限不清。腺体呈弥漫片状或结节状低密度区,CT值一般在45 HU左右,密度低于骨骼肌,腺体边缘轮廓清晰。增强扫描呈轻度或明显不均匀强化[17]。周永等[18]在甲状腺增强扫描中观察到甲状腺"岛征"和浸润"过渡征",较具有特征性。 3.5 细针穿刺活检及细胞病理学改变 甲状腺明显肿大或甲状腺出现结节时,可行细针穿刺细胞学检查以明确诊断。该检查的特异性仅次于病理学检查,有经验的穿刺和细胞学检查其准确性可达95%,而在超声引导下对可疑区域的穿刺可进一步提高诊断的阳性率[19]。Mordes等[20]指出,SAT典型的细胞学特征表现为许多大的多核巨细胞,细胞核的数量可达上百个,染色质呈细颗粒状,胞质均一,富含颗粒;上皮组织细胞聚集形成的肉芽肿也是SAT的一个特征,也可鲜有甚至不出现。 4 治疗的进展 SAT是一种自限性疾病,早期治疗以减轻炎症反应及缓解疼痛为目的。轻症可用乙酰水杨酸(1~3 g/d,分次口服)、非甾体抗炎药(如吲哚美辛75~150 mg/d,分次口服)或COX-2抑制剂。对于严重病例,如疼痛发热明显,或以上药物治疗无效者,可使用糖皮质激素,初始泼尼松20~40 mg/d,维持1~2周,据症状、体征及ESR的变化缓慢减少剂量,总疗程不少于2~3个月。过快减量、过早停药可使病情反复,应注意避免。对于甲状腺毒症明显者,可使用β-受体阻滞剂,一般不使用抗甲状腺药物治疗[21]。值得注意的是,糖皮质激素对快速缓解临床症状起到很好的疗效,但研究表明在预防或减少甲状腺功能减低方面与未使用激素治疗组对比无明显差异[22]。近来有学者通过临床实验表明,SAT患者的氧化应激水平高于健康人,抗氧化能力低下,糖皮质激素及NASID均能改善SAT患者的氧化应激状态,且前者效果更为显著[23];而小剂量糖皮质激素联合消炎痛用于SAT的治疗又优于单一用药[24]。 近年新开展的治疗SAT方法是在甲状腺局部小剂量注射地塞米松[25]。方法:用一次性皮试针(1 ml)抽取地塞米松5 mg,选择甲状腺结节或明显肿大部位,行甲状腺单叶或双叶注射治疗,过程中注意避开血管。具体剂量为甲状腺Ⅰ度肿大者每次每叶注射地塞米松2.5 mg,甲状腺Ⅱ度肿大及以上者每次每叶注射地塞米松4 mg。每周注射2次,疗程结束标准为患者症状体征完全消失。该疗法既可快速缓解临床症状,缩短疗程,使肿大的甲状腺组织体积明显缩小,有助于促进甲状腺功能恢复,又可克服全身用药的缺陷,最大程度地避免激素使用的并发症[26],值得广泛推广。 5 结语 SAT是一种好发于30~50岁中青年女性的颈部疾病,颈前肿块和甲状腺疼痛为其主要症状[27]。目前该病的病因仍不十分清楚,可能与病毒感染和自身免疫反应有密切关系。据SAT特征性临床表现,结合实验室检查及B型超声、CT,必要时行甲状腺细针穿刺细胞学和病理学检查,可明确诊断,并可与其他甲状腺疾病鉴别[28]。目前治疗常应用非甾体抗炎药、糖皮质激素,抗病毒治疗也起到一定效果,而甲状腺局部小剂量注射地塞米松在今后的临床应用中值得推广。随着诊断技术和治疗方案的提高与完善,越来越多的SAT患者将会从中受益。
周玉 主治医师 河池市第三人民医院 医疗美容科1837人已读 - 精选 高龄乳腺癌的临床治疗策略
原文刊登于 Journal of Oncology Practice(ISSN: 1554-7477)乳腺癌是女性最常见的恶性肿瘤,发病率随着年龄的增加而增加。诊断乳腺癌的平均年龄为61岁,而大多数死于乳腺癌的妇女平均年龄为65岁及以上。公共卫生和医疗保健改善显著性延长了人的寿命,高龄老人(80岁及以上)人数迅速增加,现在美国高龄老人有900万。高龄老人的个体化治疗是复杂的,包括了明确的治疗目标和治疗价值,同时也要权衡风险,比如功能丧失和影响生活质量等治疗上潜在的风险。有关老年乳腺癌的循证治疗指南很少。临床试验数据主要来源于年轻患者,而缺乏评估可能影响老年人生活质量的毒副作用的必要的信息。医师制定治疗方案应考虑病人的预期寿命和老年评估结果,而老年评估包括功能状态、合并症、认知、社会支持、营养状况和心理状态。此外,治疗决策还应权衡病人的治疗目标、偏好和价值。本文综述了现有的文献,并专注于在治疗80岁及以上早期和转移性乳腺癌的患者建议中老年评估的作用。 一.老年评估和预期寿命评估 老年评估是有效衡量与老年化相关的关键领域的基石。大量的数据显示,老年评估可以发现肿瘤学专家不常发现的主要问题,这些问题很多已经证实有效的干预措施(如跌倒)。因此,老年乳腺癌患者开始治疗前至少进行的筛查和评估,。体力状态(KPS)作为老年患者的全面功能估计是不足的。有数据显示KPS评分提示功能正常,但经过老年评估后大约70%的患者有一个主要的不足,约20%有两个不足,这些不足可能影响治疗的耐受性和疗效。临床试验和社区机构证实使用癌症和老龄化研究小组(The Cancer and Aging Research Group)工具进行一个简短的老年评估是可行的,它也可以用来预测化疗相关的毒副反应。在临床实践中实施老年评估可以获得一个很好的治疗参考。 在制定治疗计划之前,也应为所有老年患者做一个预期寿命的评估。Cho等人开发了合并症—调整期望寿命的工具用于评估预期寿命。值得注意的是,对于80岁以上患者有无或低/中合并症,平均期望寿命是≥ 5年。老年评估所需要的相关因素也可用于验证模型,估计预期寿命更为精确。这种模型可能比临床医生的格式塔寿命期望(gestalt of life expectancy)工具估计得更好。 二.原发灶的管理 1.乳腺癌的表型 乳腺癌是异质性疾病,治疗决策是基于分期、组织学亚型、核分级和分子表型。至少有75%的80岁以上患者是HR阳性和HER2阴性型,而剩余的是更具侵袭性的三阴性、HER2阳性型。 2.内分泌治疗 80岁及以上患者的主要分子表型是HR阳性HER-2阴性。有部分此类病人有很多的合并症和预期寿命仅有几年。这些患者可以使用内分泌治疗就收到很好的效果。另外,这些HR阳性HER-2阴性的患者原发病灶不可切除时,更可能从新辅助内分泌治疗获益,使得肿瘤缩小,以便进一步行全乳切除术或保乳术。在这种情况下更优先使用芳香化酶抑制剂,因其在老年人中发生的副作用可接受,与他莫昔芬相比不会增加血栓或子宫癌的风险。一般来说,内分泌治疗可以控制肿瘤生长约18至24个月,这对于期望寿命短发患者是一个理想的治疗策略。药物开始治疗有效的时间可能需要几个月或更长的时间,但许多患者在整个生命周期可能得到持续的疾病控制。 3.手术 手术仍然是任何年龄阶段女性患者的标准治疗,除非他们无手术指证,或拒绝手术,或期望寿命短。80岁及以上患者通常对手术的耐受良好,以及并发症发生率较少。在一项入组120名80岁及以上老年患者的研究中,32%患者行单纯全乳切除术,27%行保乳术,6%行腋窝清扫术,主要并发症(大部分为伤口愈合不良)发生率约6%。大多数老年女性患者适合行保乳术,肿瘤较小和腋窝临床评估阴性(体格检查和影像学阴性)的大部分患者不太可能从前哨淋巴结活检受益,因为前哨淋巴结活检术并不改变治疗方案。临床上评估腋窝淋巴结阳性的患者应考虑腋窝淋巴结清扫术。 4.放疗 对于肿块较小(≤3厘米)、淋巴结阴性、HR阳性且HER2阴性、已行保乳术和内分泌治疗的乳腺癌患者,不进行放疗是可行的选择。不放疗对总生存率没有影响,但是一个乳腺癌复发相关的高风险因素。一个随机试验研究显示,对于T1N0M0的70岁老年女性患者,均接受保乳术和使用他莫昔芬内分泌治疗,术后无放疗组的局部区域复发率为10%,而术后放疗组的局部区域复发率为2%。两组的10年总体生存率几乎是相同的,且大多数患者死亡并非由乳腺癌引起。对于80岁及以上HR阴性且淋巴结阴性行保乳术的乳腺癌患者,建议放疗,因为这些患者的局部区域复发的大部分可能发生在诊断后的几年内。对于肿块较大的患者,特别是淋巴结受累的,放疗能提高生存率。然而,通常这些获益主要发生在诊断后的5-10年,对于预期寿命少于5年的患者获益极少或者没有获益,有一些综述讲述关于放射治疗在老年患者中的作用。 5.辅助全身治疗 在估计的预期寿命和进行老年评估后应与与病人讨论辅助全身治疗目标。内分泌治疗、化疗、抗HER-2靶向治疗的潜在价值治疗最好通过在线模型评估。PREDICT模型也可评估HER2阳性患者使用曲妥珠单抗的总体生存率的绝对获益。但目前没有模型可以评估80岁及以上的女性患者在系统性辅助治疗中是否获益。因此,最重要是根据临床诊断和病人的愿望是作出治疗决策。 HR阳性和HER2阴性型大于80岁的乳腺癌患者主要接受内分泌治疗,优选芳香化酶抑制剂。HR阴性患者推荐化疗。对于HER2阳性患者,化疗和曲妥珠单抗前应考虑绝对生存获益。患者接受化疗主要考虑因素是毒副作用。预测3级及以上的毒副反应的模型可以帮助决定是否化疗。此外,还应考虑可能因化疗不良反应而需要住院治疗。在一项研究中,65岁及以上的患者因化毒副作用需要住院治疗,接受多西他赛/环磷酰胺方案的住院率为13%,多西他赛/阿霉素/环磷酰胺住院率为24%,蒽环类/紫杉醇为20%,这些比例在80岁及以上的老年人可能更高。这些住院数据需要引起重视,因为老年患者的住院频率与功能下降、生存期短相关。对于辅助全身治疗的建议见附表。 附表.≥80岁患者的肿瘤分子表型和系统性治疗建议 肿瘤分子表型和所占的比率 肿瘤生物学特性和自然病史 内分泌治疗、化疗、抗-HER2治疗建议 HR阳性, HER2阴性; 大约占 75%-85% 大部分是 luminal A 或B型. 生长慢,大部分复发转移在诊断5年后 大部分要AI或他莫昔芬治疗;一些肿瘤较小(≤1 cm),核分级低级别可不行内分泌治疗;估计化疗生存获益≥5%和非乳腺癌预期寿命大于5年可考虑化疗*。 三阴性,大约占 10%-15% 大部分复发在诊断第一个5年内 化疗5年生存获益≥3%和非乳腺癌预期寿命大于5年可考虑化疗可考虑化疗。 HER2阳性大约占 10%-15% 大部分复发在诊断第一个5年内, HR阳性,HER2阳性自然病史较好,复发晚于HR阴性HER2阳性肿瘤 HR阳性可内分泌治疗,5年生存获益≥3%和非乳腺癌预期寿命大于5年可考虑化疗可考虑化疗和抗-HER2治疗。 *基于在线评估化疗或抗-HER2治疗的价值 (见 Adjuvant SystemicTherapy). 6.转移性疾病 转移性乳腺癌仍然是无法治愈的, 20%的转移患者生存期约为5年,治疗的目标是控制癌症转移的速度,并尽可能保持最好的功能和生活质量。老年患者即使存在转移,也有相当大部分的死于非乳腺癌的风险。在一项转移性乳腺癌妇女的研究中发现,21%的患者在5年内死亡,约30%的患者死于更长的随访出现非乳腺癌合并症。除了全身治疗、姑息治疗、如放射治疗骨转移和脑转移由于毒性低应予以考虑。 HR阳性且HER2阴性的大于80岁的转移性乳腺癌患者,主要的治疗方法是内分泌治疗,建议优先使用芳香化酶抑制剂,而不是他莫昔芬。而内分泌联合细胞周期蛋白激酶依赖性抑制剂--帕博西尼或/和依维莫司治疗数据仍欠缺令人信服的证据。对于内分泌耐药和三阴型转移性乳腺癌患者,考虑化疗。一些研究表明80多岁患者可受益于姑息性化疗,年龄≥80岁各种癌症患者接受化疗的已被证实与高住院率(32%)、输血(18%)、和剂量减少,延迟和缺少(68%)相关。化疗首选序贯单药化疗,紫杉醇周疗、口服药卡培他滨证实有效,纳米白蛋白结合型紫杉醇、Eribulin、阿霉素脂质体、吉西他滨和其他药也已经应用在老年患者中。HER2阳性肿瘤曲妥珠单抗也可考虑使用,如果转移性乳腺癌的老年患者的预期寿命合适,紫杉醇加曲妥珠单抗及帕妥珠单抗方案可以考虑。另一种新药,ado-trastuzumab emtansine因毒副作用较小可以作为这些老年患者的单药治疗但数据有限。 7.支持和姑息治疗 姑息治疗可提高癌症患者的生活和生存质量,一个理想的治疗团队应包括患者的初级保健医生、社会工作者、姑息治疗专家、肿瘤学专家。 总结,大于80岁乳腺癌患者的治疗应该结合预期寿命、治疗可能的获益、患者的治疗目标、治疗潜在的副作用以及对功能和生活质量的影响来综合考虑治疗方案。
周玉 主治医师 河池市第三人民医院 医疗美容科2717人已读 - 精选 孕妇得了甲状腺疾病怎么办?
孕妇为什么容易得甲状腺疾病? 妊娠状态下,甲状腺素需要量增加,机体的基础代谢率明显升高,甲状腺不得不加班工作、扩大产能,以满足母亲和胎儿的生理需求。甲状腺及其产生的甲状腺素水平发生变化,可能会发生甲状腺疾病。 另外怀孕和哺乳期对碘的需要量增加,此时如碘摄入不足或碘缺乏,易出现甲状腺疾病。其他引起甲状腺疾病的原因包括桥本甲状腺炎,这是一种自身免疫性甲状腺疾病,由免疫系统异常攻击和破坏甲状腺细胞造成。 孕妇得了甲状腺疾病有什么影响? 甲亢或甲减如果没有得到及时的诊断和治疗,都会对怀孕的女性及其后代造成严重的负面影响。甲状腺疾病增加胎儿早产、死产、胎儿生长发育障碍,以及发生胎盘早剥的危险。 妊娠期发现甲亢怎么办? 妊娠期甲状腺功能筛查在妊娠8周以前,最好在怀孕前筛查。 1.对于T4明显升高伴有TPOAb阳性,且TSH(促甲状腺激素)降低的,排除其他原因的(如妊娠甲亢综合征),考虑临床甲亢,根据怀孕的时间,选择合适的物治疗且需要每2~6周监测FT4和TSH,并调整用药。 2.而对于T4轻度升高,TSH降低,TPOAb阴性,可能为妊娠一过性甲亢,可以4周后复查,一般不需要抗甲状腺药物治疗。 甲状腺疾病会遗传给宝宝吗? 母亲有甲状腺疾病的话,其后代中有一半左右可能会在长大后得甲状腺疾病。因此,患有甲状腺疾病的母亲和她们的孩子都应该了解甲状腺疾病的症状和体征,定期检查甲状腺,这一点非常重要。
周玉 主治医师 河池市第三人民医院 医疗美容科7531人已读 - 引用 前胸部瘢痕增生
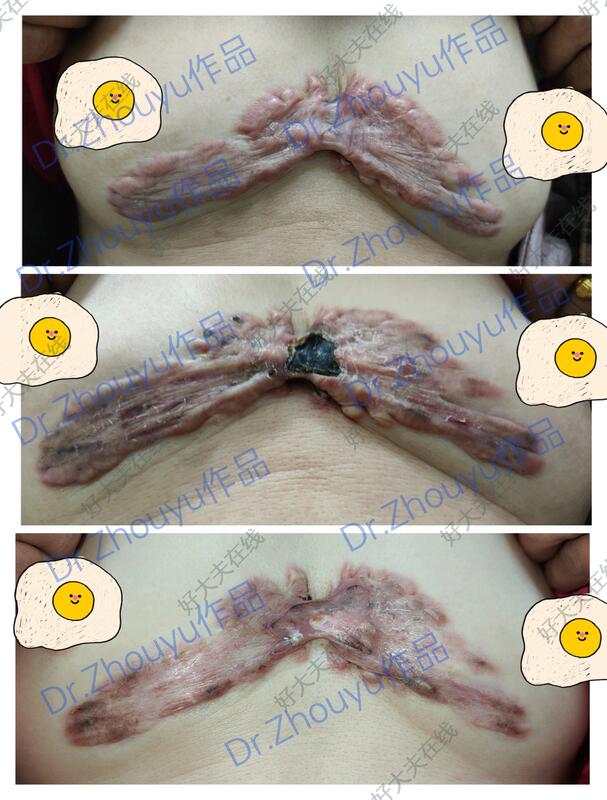
治疗前 前胸部瘢痕10余年,缓慢性增大,伴瘙痒,刺痛不适,伴有挛缩,影响外观。现在治疗第4个月,该案例仍在治疗中。 治疗中 采用药物局部注射治疗(5-Fu+曲安奈德),每次治疗间隔28天。 治疗后 治疗后3月 如图所示,治疗前至治疗后第4个月,局部瘢痕萎缩塌陷明显,但仍未完全抑制瘢痕,仍在继续治疗中
 周玉 主治医师 河池市第三人民医院 医疗美容科77人已读
周玉 主治医师 河池市第三人民医院 医疗美容科77人已读 - 乳腺疾病饮食指导(一)
这是一篇关于乳腺癌患者的饮食指导,主要内容是关于乳腺癌患者术后的饮食。手术治疗是乳腺癌最常见的治疗手段之一,营养不良可增加术后并发症风险和死亡风险。在一项对48例手术治疗的乳腺癌患者进行研究:随机将其分成观察组(常规护理联合营养治疗)和对照组(常规护理),研究结果发现,观察组伤口愈合率明显高于对照组,愈合时间明显短于对照组。营养膳食建议: 乳腺癌患者确诊后应进行营养风险筛查与营养评估,发现营养不良时应立即进行营养治疗,并在疾病过程中定期监测。乳腺癌患者营养风险筛查推荐采用NRS2002,营养评估推荐采用PG‐SGA量表。乳腺癌患者能量供给为25~30kcal/(kg·d),必要时可根据具体情况进行个体化的动态调整。 乳腺癌患者蛋白质的摄入量为1.2~1.5g/(kg·d),存在严重消耗的患者蛋白质的摄入量可增至1.5~2.0g/(kg·d)。饮食中ω‐3PUFA与ω‐6PUFA相对摄入比增加、低脂奶制品的摄入或增加奶制品的摄入频率可能降低乳腺癌的发生风险,摄入含咖啡因的咖啡可以降低绝经后女性乳腺癌的发病率,食用大豆食品可显著降低女性乳腺癌的死亡和复发风险。应监测乳腺癌患者体重,进行体重管理,维持健康体重(体质指数18.5~23.9kg/m2)。维持健康体重的干预措施:每2周定时(早晨起床排便后空腹)监测体重1次并记录。每周至少150min的中等强度体力活动(每周5次,每次30min);每周至少2次力量性训练(大肌群抗阻运动)。建议增加蔬菜、水果和全谷类食物、优质蛋白的摄入,限制酒精、红肉和加工肉制品的摄入。《中国肿瘤营养治疗指南2015版》和ESPEN指南指出,肿瘤患者能量摄入推荐量与普通健康人无异,建议卧床患者给予20~25kcal/(kg·d)的能量供给;有活动能力的患者应给予25~30kcal/(kg·d)的能量供给。ZuconiCP等对17例乳腺癌患者和19例健康女性进行了营养评估,结果显示乳腺癌患者的REE与健康女性相似,可根据25kcal/(kg·d)的快速公式计算。考虑到大多乳腺癌患者的活动能力不受限,能量需求与健康女性相似,通常情况下建议乳腺癌患者能量供给为25~30kcal/(kg·d)。乳腺癌患者的能量需求也会受到饮食、生活习惯、运动量、体重、肿瘤负荷状态、机体代谢状态等多种因素的影响,必要时需要根据具体情况进行个体化的动态调整。蛋白质是人体重要的组成成分,在生命活动中发挥着重要的作用。ESPEN指南推荐肿瘤患者的蛋白质摄入量至少1.0g/(kg·d),根据情况可增加至1.5g/(kg·d)。在缺乏运动和存在全身性炎症反应的情况下,蛋白质目标供给量可达到1.2~2.0g/(kg·d)。《中国肿瘤营养治疗指南》(2015版)建议肿瘤患者蛋白质供给量为1.0~1.5g/(kg·d),严重消耗者可将蛋白质供给量调整至1.5~2.0g/(kg·d)。研究表明,抗肿瘤治疗过程中由于不良反应导致的恶心、呕吐、食欲减退、虚弱乏力,会使乳腺癌患者体力活动减少,引起体重和脂肪组织增加,瘦体组织明显减少,增加并发症的数量和严重程度。这种以脂肪量增加和肌肉质量、力量减少为特征的体重增加,称为肌肉减少性肥胖(sarcopenicobesity,SO),可通过补充足量的蛋白质1.2~1.5g/(kg·d)预防。基于上述证据,建议乳腺癌患者蛋白质摄入量为1.2~1.5g/(kg·d),存在严重消耗的乳腺癌患者,蛋白质摄入量可调整至1.5~2.0g/(kg·d)。
 周玉 主治医师 河池市第三人民医院 医疗美容科暂无购买
周玉 主治医师 河池市第三人民医院 医疗美容科暂无购买 - 引用 孕妇得了甲状腺疾病怎么办?
孕妇为什么容易得甲状腺疾病? 妊娠状态下,甲状腺素需要量增加,机体的基础代谢率明显升高,甲状腺不得不加班工作、扩大产能,以满足母亲和胎儿的生理需求。甲状腺及其产生的甲状腺素水平发生变化,可能会发生甲状腺疾病。 另外怀孕和哺乳期对碘的需要量增加,此时如碘摄入不足或碘缺乏,易出现甲状腺疾病。其他引起甲状腺疾病的原因包括桥本甲状腺炎,这是一种自身免疫性甲状腺疾病,由免疫系统异常攻击和破坏甲状腺细胞造成。 孕妇得了甲状腺疾病有什么影响? 甲亢或甲减如果没有得到及时的诊断和治疗,都会对怀孕的女性及其后代造成严重的负面影响。甲状腺疾病增加胎儿早产、死产、胎儿生长发育障碍,以及发生胎盘早剥的危险。 妊娠期发现甲亢怎么办? 妊娠期甲状腺功能筛查在妊娠8周以前,最好在怀孕前筛查。 1.对于T4明显升高伴有TPOAb阳性,且TSH(促甲状腺激素)降低的,排除其他原因的(如妊娠甲亢综合征),考虑临床甲亢,根据怀孕的时间,选择合适的物治疗且需要每2~6周监测FT4和TSH,并调整用药。 2.而对于T4轻度升高,TSH降低,TPOAb阴性,可能为妊娠一过性甲亢,可以4周后复查,一般不需要抗甲状腺药物治疗。 甲状腺疾病会遗传给宝宝吗? 母亲有甲状腺疾病的话,其后代中有一半左右可能会在长大后得甲状腺疾病。因此,患有甲状腺疾病的母亲和她们的孩子都应该了解甲状腺疾病的症状和体征,定期检查甲状腺,这一点非常重要。
周玉 主治医师 河池市第三人民医院 医疗美容科899人已读 - 引用 检查发现乳腺结节怎么办(转载)
既然非典型导管增生与乳腺癌相关,那么我们关注的重点应是这类患者。乳腺结节是指不能扪及肿块,但超声检查发现的小低回声病灶或乳腺X检查发现的小致密影,因多考虑性病变,BI-RADS分级属2级或3级,所以统称为乳腺结节,以区别可扪及的乳腺肿块,这类患者往往比较紧张,成天担心是乳腺癌。这类病变是否都需要活检呢?患者常常会不断询问医生这个问题以求得明确的答案和心理安慰,但医生又担心漏诊或延迟诊断而回答的模梭两可,反过来又增加了患者的心理负担。其实根据目前的研究这就类病变98-99%都是良性的,只有1-2%可能是早期乳腺癌或原位癌[3,7]。所以,不管是否有乳房疼痛,对于乳腺结节患者,医生应按影像学检查的BI-RADS分级评估结果给患者提出处理意见,对于影像学检查发现的BI-RADS分级为2级的乳腺结节,应每1年定期检查一次;BI-RADS分级为3级乳腺结节,则3- 6个月后复查,随访检查过程中如升为4级则进行活检。但对患者非常焦虑,或年龄大于50岁,或临床需要(如乳腺癌家族史或BRCA基因突变携带者)也可按相关指南,对超声评估为3级的患者进行即时经皮活检,以避免延迟诊断或过度活检。 总之,在乳腺疾病的诊疗过程中,应尽量避免下“乳腺增生”的诊断,而乳痛症是生理性变化,要充分告知正确的相关信息,以免妇女过度焦虑影响生活质量,并造成过度诊疗;要重点关注非典型增生病变,积极预防,降低乳腺癌风险。
周玉 主治医师 河池市第三人民医院 医疗美容科1637人已读 - 引用 什么样的乳腺增生会增加癌变风险(转载)
一些妇女经常会咨询自已的“乳腺增生”是否会癌变,若解释不当很容易引起她们严重的焦虑。关于乳腺增生性病变与乳腺癌风险的关系,很多针对乳腺良性病变的相关文献已做详细阐述。基本可将乳腺增生性病变分为三类: 非增生性病变(NP)如乳痛症、腺病、囊肿、纤维腺瘤和轻度导管增生等;增生性病变不伴非典型增生(PWA)如中度导管增生、乳头状瘤伴导管增生等;非典型增生(AH)如导管或小叶非典型增生。根据以往大量研究证明[2],单纯乳房疼痛和NP均属于生理性的乳腺增生性病变,临床上诊断乳痛症,并不增加乳腺癌风险。PWA仅轻度增加风险,这占绝大多数乳腺良性病变(NP和PWA,约占96%)的妇女不需要特殊处理,可按普通妇女进行定期随访即可,药物预防治疗也并无必要;在影像学评估为良性乳腺疾病而进行微创活组织检查中[3],乳腺癌和非典型增生仅分别占1. 1%和1. 7%。虽然非典型增生的检出率占良性乳腺疾病的极小部分,但伴有非典型增生的良性病变其发生乳腺癌的危险性明显增加,大约是普通人群的3.5-5倍。非典型增生具有中度发展成浸润性乳腺癌的风险,约3.7%~22% 的病例可能发展为浸润性癌。故此部分妇女属于高风险人群,应按美国临床肿瘤学会的高危风险妇女筛查与预防指南进行密切筛查随访,甚至可用化学药物预防或预防性切除乳房来降低风险。目前采用的三苯氧胺、阿那曲唑和依西美坦可使非典型增生妇女乳腺癌发生率降低约40%~50%[4-6]。所以,与乳腺癌相关的主要是乳腺导管非典型增生病变,这类病变可通过影像检查发现和经皮活检或手术活检确诊,并有明确的预防指南,大家可以依照指南和规范来处理这类病变,避免过度诊断和治疗。
周玉 主治医师 河池市第三人民医院 医疗美容科1860人已读 - 引用 治疗转移性乳腺癌
原文“ Curing Metastatic BreastCancer ”刊登于 Journal of OncologyPractice(ISSN: 1554-7477)即使在肿瘤治疗突飞猛进的今天,转移性乳腺癌由于其顽固的耐药性仍然是目前抗癌治疗中难以攻克的疾病。面对患者的咨询,即使少数患者能够长期生存,肿瘤学家也几乎不提治愈的可能性。美国癌症协会数据显示:转移性乳腺癌的5年生存率仅为22%。无独有偶,来自美国东部肿瘤协作组(ECOG)的III期临床实验数据显示转移性乳腺癌的生存期近数十年基本没有改变。 对于大多数的转移性乳腺癌而言,事实的确如此。然而,1-2%的少数患者能够被治愈也是不争的事实。既然少数患者能够获得治愈,那么能不能使得越来越多的“少数”得到治愈呢? 一、目前转移性乳腺癌的治愈可能性 1、辅助化疗 辅助化疗治疗转移病灶其实是指对体内的微转移灶的治疗。辅助治疗通过消除体内的微转移灶从而使得患者获得长期生存,同样的方案使用在广泛转移的同一个患者却不能达到同样治愈的效果,提示肿瘤负荷对治愈的重要性,超过了一定范围的肿瘤负荷使得肿瘤治愈变得不可能。 2、局部复发后的辅助治疗 几代肿瘤学者都认为局部复发是全身广泛转移的先兆。最近COLAR研究结果显示局部复发乳腺癌局部治疗后全身化疗能够降低转移性患者死亡率,从而认为部分局部复发乳腺癌患者能够从这种“辅助化疗”中获益。 3、姑息性化疗 一项来自于美国MD Anderson癌症中心的基于蒽环类化疗方案治疗转移性乳腺癌的实验数据显示1-2%的少数患者能够达到超过10年的长期生存;东部肿瘤协作组的II期临床实验数据同样提到有少数患者也能够获得长期生存(>15年)。以上数据提示,即使是转移性乳腺癌患者,也能够通过姑息性化疗治愈。 4、低负荷肿瘤转移灶的治疗 多个文献提示,低负荷转移灶肿瘤(oligometastatic,寡转移指1-2个器官的转移,除外切除的原发灶)是潜在可治愈的疾病,治疗应相对积极。最具代表性的是Kobayashi的研究,他的研究入组患者75人,入组患者接受系统的全身治疗和适当的局部治疗后,20年总生存率为52%。基于实验随访的缺陷等原因,该数据并不能代表所有的转移性乳腺癌患者,但是同样提示我们,是有一定比率的患者通过适当的系统治疗能够达到长期生存。 二、提高转移性乳腺癌治愈率的前景 尽管提高乳腺癌治愈率的前景无法预测,但是基于现有的研究成果和科技手段,作者认为以下方面可能有助于提高转移性乳腺癌的治愈率。 1、通过更精良的影像技术早期发现转移灶 一直以来,肿瘤学者都认为肿瘤负荷与转移性乳腺癌治疗的结果关系密切。因此,早期发现转移灶也变得十分重要。然而,对于这一观点也有许多争议,90年代两项重要的关于早期乳腺癌与监测的试验结果显示,转移灶的早发现并没有为患者带来生存获益。然而,COLAR研究结果将局部复发作为全身转移的先兆,并认为局部处理后的全身化疗能够为这部分患者带来生存获益。先进的影像检查能够越来越精细的发现微小转移灶,如何处理不到一毫米的微小转移灶也是目前所面对的挑战和课题。 2、早期检测可治疗的基因组损伤 肿瘤细胞在发生多次突变后变得更加“聪明”,并导致了肿瘤的异质性,这也是肿瘤发生药物抗性的原因之一。早期检测基因组损伤,能够帮助发现药物抗性机制并治疗。目前,循环肿瘤DNA(ctDNA)的检测已经使这一难题变得可能,检测到ctDNA及形成明确转移灶的时间间隔似乎能够为转移性乳腺癌的治疗争取更好的治疗时间。南北肿瘤协作组007试验结果否定了这一推测,ctDNA在转移性乳腺癌中的关键作用应该在于预测微转移更有效的治疗方案选择。 3、产生大量的异常反应 异常反应NCI定义为:接受某种治疗能够达到CR或PR持续时间短于6个月的人群小于总研究人群的10%。从这些异常反应人群的组织中提取的DNA或RNA进行整条染色体的测序或mRNA测序。希望通过分析这些异常反应的基因排列发现新的异常的分子改变,从而找到新的治疗靶点或通路。目前关于该领域的研究非常多,但是,目前尚未得出有价值的研究成果。 4、免疫治疗方法 针对肿瘤细胞和肿瘤微环境免疫细胞的免疫检查点抑制剂的效果良好,引起人们越来越多的关注。免疫检查点(immune checkpoint)能够阻碍或终止免疫活动来防止自身免疫和导致自身耐受,但是,肿瘤也可利用这些途径来逃避免疫损伤,阻断免疫检查点的抗体,如抗CTLA-4,抗PD-1和抗PD-L1抗体能够延缓肿瘤的生长,延长生存期。 一些关于肿瘤浸润淋巴细胞的研究显示肿瘤浸润淋巴细胞是强有力的预后因子,免疫治疗及免疫微环境对肿瘤的治疗至关重要。对于乳腺癌,免疫治疗才处于刚刚起步的阶段,随着今后更多研究的深入,免疫治疗对于转移性乳腺癌是否可治愈将起到至关重要的作用。
周玉 主治医师 河池市第三人民医院 医疗美容科1439人已读 - 引用 甲状腺术中如何避免喉返神经损伤
本文原载于《国际外科学杂志》2015年第2期 喉返神经(Recurrent?laryngeal?nerve,RLN)损伤?一直是甲状腺手术中最常见和严重的并发症之一。?公元2世纪Galen第一个发现并描述了RLN。公元?1?000年Abul?Kasim是有资料记载的第一位施行甲状?腺切除术的人,其提出术中不能切断RLN。此后甲状?腺手术由于其高病死率一直无重大的进展。19世纪?Kocher是甲状腺外科集大成者,其提出的精细手术使?甲状腺手术病死率下降到小于l%,囊内解剖也使?RLN的损伤率下降。1938年Lahey报道了3?000余?例甲状腺切除术,提出了术中解剖RLN“没有增加,?而是肯定降低了RLN损伤的数量。至今,术中解?剖显露已成为RLN保护的“金标准”。单侧RLN损?伤引起声音嘶哑、发声和吸气的缩短,双侧损伤可导?致呛水、呼吸困难,甚至危及生命的声门梗阻。这?些症状严重影响患者生活质量,也是甲状腺术后医疗?诉讼的主要原因。随着手术技巧的逐步提高,近年来?RLN损伤率逐年下降,暂时性RLN损伤率为3%一?14%,永久性的损伤率为1%一3%[3-4]。? 1 RLN损伤的原因? 1.1?RLN的解剖? RLN与甲状腺、甲状腺下动脉关系密切,本身存在分支,以及自身的变异均易造成神经的损伤。? 1.1.1?RLN与甲状腺下动脉解剖关系 RLN与甲状腺下动脉关系密切,但变异很大。有研究尸体解剖了?160条喉返神经发现:在左侧,86.25%的喉返神经位于?甲状腺下动脉后,7.5%的神经位于动脉前,2.5%的神?经穿行于动脉分支之间;在右侧,75%的神经位于动脉?前,10%的神经位于动脉后,5%的神经穿行于动脉分支之间。其余为不确定。神经位于血管深部较安?全,而位于动脉前及穿行于动脉分支之间均极易损伤。?左侧RLN行走于动脉后者居多,右侧RLN行走在动脉?前或分支问者居多。因此右侧神经更易损伤,这是由?于左右侧RLN的行走路线不同而造成的。由于甲状?腺下动脉与RLN解剖关系如此密切且复杂,因此分离?血管与神经时极易造成RLN的损伤。? 1.1.2?RLN的分支及分支 变异RLN上行至喉内?或在入喉处分为前后2支,偶为3支,这些分支与喉?功能有关,称为喉支。前支携带负责内收和外展声带?的喉内肌运动纤维。RLN存在分支变异,即喉返神经?在距环甲关节较远的地方,分为2支或2支以上,相伴或分开上行,并在不同部位人喉。RLN异常分支的?分叉处往往发生在与甲状腺下动脉交叉处。因此如?果从甲状腺下动脉处开始寻找识别RLN,则易损伤其?分支。研究发现这些异常分支的分叉点与喉的平均?距离为21.5?mm,因此在RLN入喉前最后2?cm是损?伤的高危部位,其原因除神经存在分支外,还包括:?RLN在那里被Zuckerkandl结节所覆盖;神经外侧的?血管筋膜层含有甲状腺下动脉的三级分支,与神经相勾绕伴行;内侧即为Berry’S韧带,这个部位的神经要?承受最大的潜在牵引力。? 1.1.3?喉不返神经? 喉不返神经是RLN罕见的解?剖畸形,极易在术中造成损伤。右侧的发病率在?0.3%~0.8%,左侧极为罕见,发病率在0.004%。?原因是由于右锁骨下动脉起始异常,因而右喉下神经?不经右锁骨下动脉折回而是从迷走神经直接发出。?在左侧喉不返神经只有在胚胎期动脉导管消失或者?右位主动脉弓时发生,而动脉导管消失的胎儿是无法?存活的,所以左侧喉不返罕见。通过术前确认右头臂干缺如,就能明确锁骨下动脉存在起始异常,预先就?能认识到喉不返神经。对于CT扫描提示血管异常?(右锁骨下动脉变异)的患者要注意喉不返神经存在?的可能。但也有无任何血管畸形的喉不返神经被报道。术中发现识别喉不返神经一直是一个难点,术者需时时提高警惕。? 1.1.4?Zuckerkandl结节? 1902年,奥地利解剖学?家Zuckerkandl最先提出Zuckerkandl结节这个概念,?这个特殊的解剖结构被定义为向后延伸的侧面裂片?组成的甲状腺组织。Pelizzo根据大小将其分为0—?3级:0级,无法辨认;1级,甲状腺叶外侧边缘增厚;?2级,小于1?am;3级,大于1?cm。并报道其发病率大?于50%。?Zuckerkandl结节使腺体侧面变大,使RLN看起来?像从侧面的裂隙进入了甲状腺实质。Zuckerkandl结节?的外科学意义可以概括为:甲状腺全切除术必须完整?解剖和切除Zuckerkandl结节;结节和RLN关系紧密,?一方面结节可作为寻找RLN的解剖标志,另一方面结?节增加了RLN损伤的危险性。认清结节与RLN之间?的解剖关系是保证甲状腺手术安全所必需。? 1.2喉返神经的脆弱性? RLN纤细,横径约为(1.93±0.35)mm,每根神经由3层的结缔组织包围,分别是神经内膜、神经束?膜和神经外膜,研究提示65.7%的RLN只有2~8层?薄的被膜,极易受损。牵拉、钳夹、缺血、切割、烧?灼、瘢痕粘连、血肿压迫都会导致其损伤,引起术后声?音嘶哑,可以是暂时性的,也可以是永久性的。牵拉?损伤是暂时性喉返神经损伤最常见的原因。? 1.3能量工具的使用? 近年来随着高科技的发展,越来越多的能量器械?被应用于甲状腺手术。高频电刀是最传统的电外科器械,已有80多年的历史。其原理是利用脉冲时间?极短的高频电流引发人体组织中的离子,在黏滞体液?中震荡产生的热能而进行工作的。其可以完成切割、?止血等操作。当电刀的工作电极与人体接触时,由于?接触的有效面积小,电极本身的高阻抗使高电流密度?在局部组织中通过,直接产生高热引起组织的分离和?凝固。其引起的热损伤也是公认最为严重的。高频电刀头的最高瞬间温度可达400℃。20世纪60年?代,双极电凝技术开始进入了手术室。在双极电凝?中,电流通过2个电极完成整个循环,从而对2个电极之间的组织产生热效应,达到止血和切割效果,但?其仍存在周围损伤的可能。超声刀1972年被引入外?科领域。目前在甲状腺外科领域应用越来越广泛。?超声刀的原理是通过主机产生55?000?Hz的谐波,传?导到刀刃振动发出相同频率的谐波,经高频超声震?荡,使所接触组织细胞内水汽化,蛋白氢键断裂,组织?被凝固后切开。超声刀引起的组织应力和摩擦所产?生的热,温度一般在低于80℃。获得的低温可以减?少组织的焦化和干燥,有限的热量使热损伤降低到了?最低程度。但随着使用的普及,越来越多的超声刀使?用不当引起的喉返神经热损伤被报道,如何减少此类?损伤也受到广泛关注。? 2 喉返神经损伤的预防? ? 熟悉喉返神经的解剖,术中显露神经,精细操作,?正确使用能量器械,合理应用神经监测都有助于预防?术中喉返神经的损伤。? 2.1术中喉返神经显露? 由于甲状腺结节摘除或腺体部分切除基本废止,?甲状腺术中常规显露喉返神经已经得到公认。Hermann等研究了15?513例甲状腺手术患者共计?26?323条喉返神经,永久性的RLN损伤率在神经暴?露组(41/10?458)与非暴露组(174/15?865)分别为?0.4%和1.1%(P≤0.001)。用大样本验证了喉返神?经显露可以减少术中的损伤率。?常用的寻找RLN的方法有3种:(1)传统的方?法,即在气管食管沟处寻找RLN,但这种方法效果较差,手术过程中对腺体的牵拉往往使RLN偏离气管?食管沟或气管食管沟在牵拉下消失。(2)从甲状腺?下极一气管一颈总动脉三角区疏松结缔组织内解剖?RLN,此处血管较少,被认为适于解剖。当然前文所?述血管与神经解剖存在大量变异性,使用这种方法需?谨慎细致,分离出神经主干,再向上解剖可发现RLN?所有分支,可避免损伤。(3)从环甲关节附近寻找?RLN,因为RLN的人喉处在环甲关节处是恒定不变?的,但存在RLN分支变异时,易损伤其分支。? 2.2喉返神经操作的精细化? 手术操作时应耐心细致,动作轻柔,保持术野清?晰,出血时切忌大块钳夹、结扎或者缝扎,缝扎止血?时,注意不要缝到神经的被膜,避免牵拉,钳夹神经,?避免导致神经水肿及影响神经周围的血液供应。同?时RLN的解剖要适度,处理甲状腺下动脉时,辨认下?动脉至腺体各分支的解剖走行,紧贴甲状腺分离结扎?甲状腺下动脉分支,而不是结扎血管的主干。游离?RLN自甲状腺下动脉至人喉处,不刻意解剖神经的分支,以免破坏神经的营养血管。理论上应保留覆盖在?RLN表面的一层筋膜,这样可以把血液供应的损伤降?到最低。精细解剖Zuckerkandl结节。外科医师必须?认真识别结节与RLN之间的关系,细致分离。?若RLN被转移的淋巴结或肿瘤组织所侵犯,可?用钝锐性相结合的方式分离神经,在可能的情况下,?尽可能保全RLN。?在寻找神经困难时,需警惕喉不返神经。除非RLN?已被识别,任何喉与血管之问横向的条索状结构(除甲?状腺中静脉)都应被重视,警惕喉不返神经的存在。 ? 2.3安全使用能量工具? 安全使用能量器械,需掌握各类能量器械的特?点,使用时的安全范围。高频电刀热损伤最严重。但?其使用灵活,迅速,适宜一些精细解剖。笔者的经验?认为刀头距离喉返神经不小于1?mm,持续作用时间?不大于3?s,功率不大于90?W。近年来Ligasure能量?平台被应用于手术,其是双极电凝加上了实时反馈技?术和智能主机技术,由于其工作频率和输出功率是按?人类工程学设计安全值,工作时电流只通过2个钳?间,只对其间钳夹的组织起作用,不会对周围的组织?造成损伤。这使得其更加安全、准确。超声刀可以凝?闭5?mm以下血管,以及断面直接切割,无需缝合。?且随着超声刀的革新,日益轻便,不仅适合甲状腺腔?镜手术,同样适用于开放手术的操作。因温度超过?63℃时,作用于组织时间≥3?s时,蛋白质就会变性。?目前认为3?mm以上距离是超声刀头的安全距离,持?续作用时间不大于3?s。 2.4喉返神经检测的使用? 术中神经监测(Intraoperative?nerve?monitoring,?IONM)在甲状腺术中使用率为20%~40%。IONM?是一项可以帮助识别RLN并判断其功能的技术,其?可以帮助判断RLN的线路,识别喉不返神经,监测?RLN的功能。视觉上完整的神经,由于钳夹、牵?拉、热损伤、缺血、压迫等原因也会引起损伤,IONM可?以指导术中的手术策略,对那些已有单侧神经损伤的?患者,应用IONM将对对侧手术作出指导意义。而对?于双侧损伤者,则可术中即行预防性气管切开。?IONM可提高RLN识别率;快速定位RLN,准确预测?解剖变异;降低RLN损伤率,确定损伤部位;保证功?能完整性,术中诊断RLN状态。但IONM是否有利?于预防RLN的损伤仍有争议。有研究认为非连续性?的IONM对于减少RLN损伤无显著帮助,将应用?IONM与单独可视化相比,RLN术后损伤率减少,但?并没有统计学意义。但在甲状腺恶性肿瘤、甲状腺再?次手术、胸骨后或巨大甲状腺肿、已有单侧声带麻痹,?对侧叶需行手术治疗者中,IONM有利于神经保护。对于术中发生意外RLN横断时,IONM可以?帮助寻找断端,有利于RLN一期吻合。IONM有助于发现喉不返神经,刺激迷走神经后潜伏期短于?3.5?ms,提示喉不返神经。 IONM有很高的阴性预测值92%一100%,即信号完整,则神经功能正常。而其阳性预测值则非?常差10%~70%。这是由于IONM存在一些潜在的?陷阱,如设备故障、设备安装不当、肌松药的不合理应?用等导致信号丢失。设备设置问题是假阳性IONM?结果的常见原因,为了防止这种情况的发生,标准的?设备设置和气管插管流程是必需的。? IONM仍需要大样本随机对照试验来进一步证实?其临床运用价值,目前已建立了标准化的四步程序,?学者们也在进一步完善其标准化使用规范。因此?IONM不可作为RLN识别和保护的唯一方法,但其确?实是辨认和保护RLN的重要辅助手段,尤其是高危?患者的手术[20|。笔者认为IONM在不断发展中有着?相当广阔的应用前景。? 综上所述,如何预防RLN损伤一直是甲状腺手?术中的难点。这与RLN本身复杂多变的解剖因素有?关,与其自身的脆弱性有关,同时也与术者对神经的?认识度,操作技巧有关。坚持术中解剖暴露神经,精?细化操作,准确应用各类能量器械,合理应用IONM,?一定会有助于减少术中的RLN损伤率。
周玉 主治医师 河池市第三人民医院 医疗美容科5904人已读



