中国科学院大学重庆医院(重庆...科普号
- 引用 30种肿瘤标志物合集(下)
肿瘤标志物,是指特征性存在于恶性肿瘤细胞,或由恶性肿瘤细胞异常产生的物质,或是宿主对肿瘤的刺激反应而产生的物质,并能反映肿瘤发生、发展,监测肿瘤对治疗反应的一类物质。肿瘤标志物存在于肿瘤患者的组织、体液和排泄物中,能够被免疫学、生物学及化学的方法所检测。本期就临床上常见的肿瘤标志物进行汇总分享。 降钙素(CT)CT是由甲状腺C型细胞分泌的一种由32个氨基酸组成的单链多肽激素。血清钙升高时,CT分泌增加,抑制钙自骨中释放,增加尿磷,降低血钙和血磷。常用于监测甲状髓样瘤的治疗疗效,以及筛查甲状髓样瘤患者的无症状家族成员。此外,肺癌、乳腺癌、消化系统恶性肿瘤患者的血清CT也有升高。其他如新生儿、儿童、妊娠、肾病、胰岛素瘤以及长期使用质子泵抑制剂等也可见CT升高。 血清CT 正常参考值为0-100ng/L。 人绒毛膜促性腺激素(βHCG)βHCG是一类糖蛋白类激素,由胎盘滋养细胞合成,受孕8天时血液和尿液中即可检测到βHCG的升高。βHCG是恶性滋养细胞肿瘤诊断、监测疗效和估计预后的重要指标。由于βHCG无法透过血脑屏障,若脑脊液中出现βHCG升高,且与血清βHCG比值大于1:60,则说明合并脑转移。此外,在恶性肿瘤,如睾丸精原细胞癌、肝癌、肺癌、胃肠道肿瘤等可见βHCG升高。在良性病变如肝硬化、十二指肠溃疡、子宫内膜异位、卵巢囊肿等患者血清中,可见βHCG轻微升高。 血清βHCG正常参考值:男性0-2.5U/ml,非妊娠女性0-5U/ml。 嗜铬粒蛋白A(CGA)CGA是一种酸性可溶蛋白,普遍存在于神经内分泌组织中,在神经内分泌肿瘤、类癌、神经母细胞瘤和小细胞肺癌中有较高的表达,在慢性心衰、长期使用质子泵抑制剂的患者血清中亦有轻微升高。 血清CGA正常参考值为39ng/L。 促胃泌素释放肽(ProGRP)ProGRP是一种胃肠激素,存在于胎儿肺中的神经纤维、脑和神经内分泌细胞,在小细胞肺癌以及神经内分泌肿瘤中可见其升高。由于ProGRP主要经由肾脏代谢,因此肾功能不全的患者也可见血清ProGRP升高。 血清ProGRP正常参考值为0-69.2pg/ml。 香草苦杏仁酸(VMA)神经母细胞瘤能合成分泌大量儿茶酚胺类物质,而VMA是儿茶酚胺的一种重要代谢产物,,24 h尿VMA是神经母细胞瘤较为特异性的一种标志物,对神经母细胞瘤的诊断具有重要的意义。此外,在嗜铬细胞瘤、神经节神经瘤、横纹肌肉瘤、原始神经外胚层肿瘤患者尿液中,也可见VMA升高。若患者摄入香蕉、香草、茶、咖啡、冰淇淋、巧克力、四环素、甲基多巴、单胺氧化酶抑制剂可导致尿液VMA升高。 24小时尿液VMA正常参考值为8-35mmol。 高香草酸(HVA)神经母细胞瘤能合成分泌大量儿茶酚胺类物质,其中HVA是儿茶酚胺最主要的终末代谢产物,24h尿液HVA总量是诊断神经母细胞瘤的经典方法。若患者摄入香蕉、香草、茶、咖啡、冰淇淋、巧克力、四环素、甲基多巴、单胺氧化酶抑制剂可导致尿液HVA升高,此外精神病以及抑郁症患者尿HVA也有轻微升高。 24小时尿液HVA正常参考值为0-40mmol。 β2微球蛋白(β2M)β2M是细胞表面人类白细胞抗原轻链部分,它是某些恶性肿瘤细胞膜上的相关抗原,故可以看作肿瘤标志物。其升高见于各种淋巴细胞肿瘤、多发性骨髓瘤、慢性淋巴细胞白血病、肺癌、乳腺癌、消化道癌。由于它在肿瘤早期便可升高,因而可用于一些肿瘤的鉴别诊断。脑脊液出现β2M意味肿瘤脑转移。必须指出的是,β2M在肾脏疾病和肝炎均可升高。 血清β2M的正常参考值为≤2.5mg/L。 人附睾蛋白4(HE4)HE4基因最早是从人的附睾中克隆,HE4属于一种酸性小分子分泌型糖蛋白,与附睾以及生殖特异度相关。在正常卵巢组织中,HE4不表达或低表达,当发生卵巢癌后,会出现高表达。此外,在子宫内膜癌、乳腺癌、肺癌、胃癌、胰腺癌患者血清中也有不同程度的升高。 血清HE4的正常参考值为0-72pmol/L。 甲状腺球蛋白(Tg)Tg存在于甲状腺滤泡腔内,在正常生理条件下人血清Tg很少,可将其作为判断体内存在由功能的甲状腺组织的重要标志物。在先天性甲状腺功能低下患者,检测Tg可鉴别甲状腺完全缺损、甲状腺发育不全。甲状腺球蛋白也被认为是甲状腺体形完整性的特殊标志物。是分化型甲状腺癌(DTC)的肿瘤标志物,可作为分化型甲状腺癌患者治疗后随访的重要参考指标。Tg升高也可见于甲状腺疾病(如甲状腺功能亢进症、毒性结节性甲状腺肿、亚急性甲状腺炎和慢性淋巴细胞性甲状腺炎)。 血清Tg正常参考值为0-33μg/L,若甲状腺完整切除,则应为0-2μg/L。 尿核基质蛋白22(NMP22)NMP22是构成细胞核内部框架,并与DNA复制、RNA合成、激素合成有关。在肿瘤细胞内,核有丝分裂器蛋白的升高与恶性细胞的细胞核结构/形态改变相符合。尿液中由膀胱肿瘤细胞释出的核分裂器蛋白进行检测,通常膀胱癌上皮细胞内NMP22的含量比正常尿路上皮高几十倍。因此,尿NMP22常被用作膀胱癌的肿瘤标志物。在前列腺增生和前列腺炎患者尿液中也可见NMP22升高。 尿NMP22正常参考值为
 唐敏 副主任医师 重庆市人民医院 肿瘤科7023人已读
唐敏 副主任医师 重庆市人民医院 肿瘤科7023人已读 - 引用 30种肿瘤标志物合集(上)
肿瘤标志物,是指特征性存在于恶性肿瘤细胞,或由恶性肿瘤细胞异常产生的物质,或是宿主对肿瘤的刺激反应而产生的物质,并能反映肿瘤发生、发展,监测肿瘤对治疗反应的一类物质。肿瘤标志物存在于肿瘤患者的组织、体
 唐敏 副主任医师 重庆市人民医院 肿瘤科4324人已读
唐敏 副主任医师 重庆市人民医院 肿瘤科4324人已读 - 引用 侵袭性纤维瘤病的前世今生
1838年Muller将侵袭性纤维瘤病(Aggressive Fibromatosis, AF)命名为Desmoid tumor即硬纤维瘤,又称韧带样纤维瘤(Desmoid-type fibromatosis)等。2002年WHO将AF定义为发生于深部肌腱膜组织的克隆性纤维母细胞增生性肿瘤,产生丰富胶原纤维为特征,累及骨骼肌腱膜和筋膜,具有进行性侵润周围肌肉软组织生长,局部复发倾向,无转移能力的特点。扩大切除是最有效治疗方式。其无包膜浸润性生长特性导致不易达到切缘阴性,累及重要脏器时常难以切除,甚至危及生命,放疗等辅助治疗降低了复发率。就近来国内外对该病的认识及治疗新进展作此文献综述。 1、疾病特点 (1)流行病学与病因:AF发病率仅占软组织肿瘤的3%及全部恶性肿瘤的0.03%,美国年发病率2-4/100000。仍缺乏国内AF的流行病学资料。任何年龄均可发病,青年为高发年龄,无明显性别差异。多为单发,约5%为多发,儿童好发于四肢,成年好发于躯干。病因不明,可能与内分泌,结缔组织生长调节异常及遗传缺陷有关。雌激素影响纤维母细胞有丝分裂可能参与AF发生。分子水平研究发现激活Wnt信号通路是AF的主要发生机制:AF特征性出现Wnt信号通路中的腺瘤样结肠息肉基因 (adenomatous polyposis coli,APC)突变失活,或编码β-catenin的CTNNB1基因突变,导致β-catenin蛋白异常高表达。细胞质内游离β-catenin蛋白水平升高在伤口愈合及纤维增生性疾病及AF发生中起重要作用。Wnt信号通路异常,触发COX-2介导激活血小板生长因子受体(platelet-derived growth factor receptor, PDGFR,α&β)及其配体表达增加也参与AF发生。 (2)分型:根据AF发生部位分为:腹部外型 (约50~60%),腹壁型(约25%)和腹内型(约15%)。 腹壁外型AF:好发于颈肩部、胸壁和下肢,累及关节者甚至需行截肢手术。 (3)生物学行为:介于成纤维细胞瘤与纤维肉瘤之间,恶性倾向体现为侵袭性生长及术后顽固复发,复发灶病理及MRI信号特征多与原发灶相同,但生长更迅速,侵及范围更广泛,甚至侵犯重要器官而危及生命,亦有多病灶复发者,罕见恶变为纤维肉瘤者,尚无淋巴系统或血行转移报告。生物学行为存在明显异质性,生长速度各异,Nakayama认为近50%的AF可能呈自限性,长期稳定无进展或逐渐自行消退。 (4)病理及免疫组化: 肉眼观:肿物位于肌肉与腱膜和深筋膜相连处,形态不规则,边界不清,无包膜,苍白质硬韧,切面纹理呈编织状,内无坏死。发生于肠系膜或盆腔者可有间质黏液样改变。 显微镜观:AF由处于增生不同分化阶段的梭形的纤维母细胞和肌纤维母细胞组成,平行束状排列,胶原纤维嵌插其间,胶原含量比分化好的纤维肉瘤多;无变性坏死,细胞核染色呈点彩状,1~3个小核仁,无病理性核分裂及异型性。肿瘤边缘常含有被浸润的肌肉组织。 免疫组化:特征性胞质和核内β-catenin弥漫阳性,vimentin,SMA(smooth muscle actin),雄激素受体、cathepsin D,生长抑素,Ki-67阳性,80%的AF中雌激素受体(estrogen receptor,ER)β阳性;而S-100、CD34、ERα、孕酮受体、Her2、desmin、cytokeratins、c-kit常阴性。其他成纤维细胞肿瘤核内β-catenin阴性;孤立性纤维性肿瘤CD34阳性;GIST则CD34,c-kit阳性。 (5)临床表现:躯干或肢体触及边界不清,质硬无波动不能推动的无痛肿块,皮肤正常,多无淋巴结肿大。肿瘤大小与发生部位、病程长短及生长速度有关,直径数至数十厘米;压迫或累及相邻器官或神经、血管、关节时可出现相关症状。应注意患者是否合并FAP及Gardner综合征。 2、诊断及鉴别诊断 (1)诊断依据:根据影像特征及组织病理确诊。由于AF少见,侵袭性生长,影像学虽有其特征,但仍难以准确鉴别其他软组织肿瘤,术前误诊率高。凡软组织肿块,应想到AF的可能,曾诊断“纤维瘤”术后复发的患者应复查原病理切片,切勿将AF误诊为单纯纤维瘤。 影像学首选MRI结合DWI(扩散加权成像)术前评估侵犯范围,是否累及周边血管、骨质破坏或侵犯脏器,制订手术方案,并作为准确的随诊工具。MRI见肿瘤沿肌肉走行,边缘不光整无包膜,爪样浸润周边肌肉,肿瘤无囊变坏死,无钙化、脂肪、瘤周水肿,多无骨质破坏。AF的T1WI呈等、稍低信号;需要强调T2WI呈略高信号,动态增强MRI呈明显持续强化或进行性延迟强化,伴各序列中存在梭形低信号无强化的致密胶原,具有重要鉴别诊断价值,而绝大多数恶性肿瘤T2WI仅呈高信号。CT显示肿瘤边界不清,平扫密度均匀,增强后不均匀强化,见与肌纤维走向一致的小梁状、梭形低密度区分散其间。超声或CT引导下穿刺活检(fine needle aspiration cytology,FNAC)免疫组化染色(至少染β-catenin,c-kit,CD-34,desmin)可术前确诊。 (2)鉴别诊断:需考虑AF发生部位,主要应与纤维瘤、纤维肉瘤、恶性纤维组织细胞瘤、神经源性肿瘤、骨化性肌炎、结节性筋膜炎;胃肠道间质瘤,子宫或卵巢来源肿瘤、淋巴瘤、平滑肌肉瘤、腹膜后纤维化等鉴别。 3、治疗: (1)外科手术:手术切除仍是AF最有效治疗方法,但因其无包膜及浸润性生长特点,术中很难确认肿瘤边界及清晰分辨瘢痕及结缔组织,多数学者主张切缘距肿瘤2~3cm扩大切除,将受累肌肉、腱膜、骨膜、骨质一并切除,以确保切缘阴性(R0)。观察标本切缘应无质硬组织,术中应行切缘多点冰冻病理至确认R0。发生在肠系膜、颈部、纵隔等特殊部位的AF常引起致命并发症,应积极手术切除。可切除范围及切缘状态与发生部位有关:如AF与神经、血管、脏器、骨膜关系密切,常因必需保留肢体或器官结构功能,切除范围受限,且重建困难,难以达到R0切除。Micke等Meta分析了13个临床中心的698例AF患者,切缘状况与复发之间关系:即使R0切除,局部复发率仍有12%~27%;镜下切缘阳性(R1)复发率42%~68%;肉眼切缘阳性(R2)复发率100%,总体术后复发率约40%。几乎均为原位或相邻肌腱膜复发,平均复发时间13~23个月,95%发生在5年内;再手术复发率更高,散发型腹部外型AF的复发几率更高,儿童复发率高且间隔时间更短。初次切缘阳性极易短期内复发,使可能存在基因突变的细胞置于组织创伤修复环境中,扮演了复发促进因素。但AF毕竟不同于恶性肿瘤,复发并不意味着失控的结局。术后强调定期复查B超及MRI,复发患者应在MRI评估病灶可切除性后积极再次手术,力争切缘阴性。 手术切除范围仍存在争议,有学者并不强调积极扩大切除,建议在难以达到R0切除时应保留器官功能性切除加术后放疗(function-sparing resection plus postoperative radiotherapy)。Salas统计426例AF,R0切除的5年PFS(progression-free survival)62.5%,而R0对照R1的PFS并无显著差异,R2则显著预后不良。对复发但病情无进展,再手术将产生严重残障(特别是四肢)等并发症的患者,建议等待观察。 (2)辅助治疗:虽然扩大切除理论上可能治愈,但临床实际仍伴随较高术后复发率,尚须采取放疗,化疗,非甾体抗炎药(NSAIDs),雌激素拮抗剂(selective estrogen receptor modulators(SERMs),激酶抑制剂TKI(tyrosine kinase inhibitors)等辅助治疗。Marco Fiore回顾性分析142例AF,提出一线保守治疗策略(front-line nonaggressive policy),尝试分阶段治疗来得到最佳肿瘤局部控制,同时保障最佳生活质量:无症状者单纯观察→药物治疗→扩大切除手术及放疗;尽量避免手术引起的功能损失及放疗并发症,等待观察组5年PFS49.9%,仅药物治疗组为58.6% (P = 0.3196)。 R0者无需放疗,而对高危患者及切缘阳性或无法手术切除的患者均建议放疗。推荐对R1患者给50Gy~60Gy。Shin认为术后放疗明显推迟了复发,但似乎并未改善远期预后。 应用SERMs他莫昔芬(三苯氧胺,Tamoxifen)或雷洛昔芬(Raloxifene)有效率为40%。塞来昔布(Celecoxib,西乐葆Celebrex)。COX-2(环加氧酶cyclooxygenase-2)抑制剂美洛昔康(Meloxicam)可有效控制散发腹部外型AF。 伊马替尼(Imatinib)抑制靶点为c-KIT、ABL、ARG和PDGFR-A&B激酶,由于AF并无典型以上基因突变,对Imatinib总体反应率10~23%,仅作挽救治疗。 4、预后及影响因素 无论采取何种治疗,AF平均复发率24~77%。10年及20年生存率为94%和86%,8%的AF患者因侵犯重要器官或大血管导致死亡。多因素分析发现AF的发病部位、病灶深度大小、年龄、性别均与复发无关,切缘阳性及手术切除史是术后复发独立影响因素。也有学者认为AF的个体生物学行为将更大程度地决定预后。编码β-catenin的基因CTNNB1外显子3上S45F突变,已被证实是散发型AF的术后高复发的分子预测因素。 5、结语 由于侵袭性纤维瘤病少见,目前多为回顾性或初步研究,缺乏前瞻性多中心联合研究及随机对照试验证据性经验积累。术中准确判断切除范围,力争初次达到R0切除,是提高完全缓解率、降低复发率的重要手段。手术加辅助放疗是有效的首选治疗,NSAIDs、抗雌激素药物、化疗、靶向治疗等个体化方案已成为新的辅助治疗选择。
罗治彬 主任医师 重庆市人民医院 肿瘤科2346人已读 - 引用 肿瘤标志物检测的临床价值及其正确运用
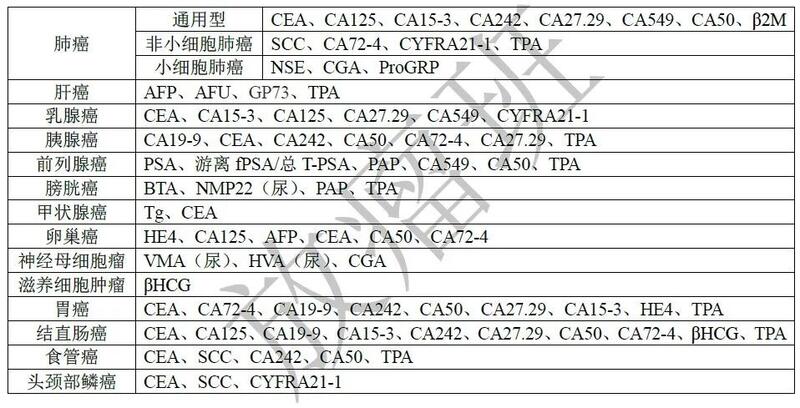
一、肿瘤标记物是什么? 肿瘤标记物是肿瘤细胞产生和释放的某种物质,常以抗原、酶、激素或代谢产物的形式存在于肿瘤细胞内或宿主体液中,根据其生化或免疫特性可以识别或诊断肿瘤,常常用于肿瘤高危人群的筛选、辅助诊断、疗效评价、病情随访,以及肿瘤复发和预后的预测等。 二、分类 肿瘤标记物大致分为肿瘤细胞分泌物和肿瘤细胞表达物两类。 (一)肿瘤细胞分泌物 这类标志物是肿瘤细胞在发生、发展中产生的物质,肿瘤生长越旺盛、其量越多,反之,肿瘤生长被压制、其产生量也减少。这些物质往往是糖蛋白,可以通过检验血等体液查出并进行监测。它们往往在肿瘤很小时即可被检测出来,有助于早期发现病灶;则提示疗效可能不佳;如手术切除肿瘤一段时间后标记物进行性升高,则往往提示体内可能已经有肿瘤细胞增殖、生长,如在治疗后明显降低,则提示治疗有效,反之,需严密监视。因此,有经验的肿瘤科医生往往会在对患者做影像检查、评估瘤体大小的同时抽血检查、动态观察相应标记物,以了解肿瘤生长是否仍然活跃、治疗后其活性是否被抑制等。它们的特点是反映灵敏、往往能早于CT、MRI等手段早期判断肿瘤生长状态,提醒医生是否需要更换治疗;其弱点是准确性较低、不如影像学诊断可靠;因此,往往需要共同检验几个标记物、动态观察其变化、并结合其他临床表征作出判断。 (二)特殊标记物 又可称为"肿瘤细胞表达物"往往是肿瘤细胞膜或细胞内结构上的某些特殊结构点,例如上皮生长因子受体(EGFR)、血管内皮生长因子受体(VEGFR)、雌激素受体(ER)、孕激素受体(PR)、CD20受体、PD-1受体等。它们多半在肿瘤细胞表面多、正常细胞表面少,可以被某些药物特异性识别并结合、从而成为这些药物追踪、打击的"靶子",顾名思义,此类药物被称为"靶向药物",其相应的治疗也被称为"靶向治疗"。例如:EGFR抑制剂、抗血管生成治疗药物、雌激素拮抗剂、CD20单克隆抗体等,已广泛用于肺癌、乳腺癌、淋巴瘤等恶性肿瘤的治疗。因此,有经验的外科医生、肿瘤科医生往往会用手术切除或穿刺活检的肿瘤组织标本去做靶向检测,了解其有无某些特异标志的表达以及表达水平的高、低,为确定以后的治疗方案提供参考。 三、肿瘤标志物的临床价值 肿瘤标志物的监测是有其独特价值的,临床上常用于:肿瘤高危人群的筛选和辅助诊断;动态监测以评价治疗效果;病情随访,肿瘤复发和预后的预测,早期预警肿瘤发生、发展;在无法取得肿瘤标本、明确病理诊断时对肿瘤性质做出某些提示、为试验性治疗提供参考依据。 四、临床应用及注意事项 1、肿瘤标记物灵敏度高,但特异性偏低,因此需要没1-2个月动态观察; 2、要有针对性地联合监测,防止发生误判误用,但也不能搞大包围而滥用。比如: (1)肺癌肿瘤标记物群:CEA、Cyfra21-1、NSE等; (2)消化道肿瘤标记物群:CEA、CA199、CA242、CA724等; (3)特异性高的就针对性监测:CA153(乳腺癌等)、CA125(卵巢癌等)、AFP(肝癌等)、PSA(前列腺癌等)、HCG(绒癌等)。 3、不同单位的肿瘤标记物检测:仪器不同、方法不同、试剂盒不同、检测人员不同,对监测结果都有不同程度的干扰,因此不必去纠缠检测值数字的细小差别,只需要观察其动态变化的趋势即可。 4、近年来,新的肿瘤标记物不断发现、检查手段不断完善,使得其灵敏性和准确性不断提高。 相信今后"肿瘤标记物学"这一新兴学科会取得更长足的发展、为早期反映体内肿瘤变化状态提供更充足的依据。 References 1.‘The role of tumour marker testing in earlier diagnosis of cancer’ will be presented by Dr Craig Barrington during Poster Display Session on Sunday, 10 September 2017, 13:15 to 14:15 (CEST) in Hall 8. 2.Cancers of unknown primary site: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Annals of Oncology. 2015;26(Supplement 5):v133–v138. doi:10.1093/annonc/mdv305 3.Metastatic malignant disease of unknown primary origin in adults: diagnosis and management. National Institute for Health and Care Excellence (NICE). Clinical guideline. 26 July 2010 nice.org.uk/guidance/cg104
罗治彬 主任医师 重庆市人民医院 肿瘤科1250人已读



