珠海市人民医院肝病科科普号
- 精选 经颈静脉肝内门体分流术(TIPS)2017专家共识
中华医学会放射学分会介入学组 经颈静脉肝内门体分流术(TIPS)是指经颈静脉入路从肝静脉穿刺肝内门静脉,在肝静脉与门静脉之间建立门-体分流道,以达到降低门静脉压力、治疗食管胃静脉曲张破裂出血和顽固性腹腔积液等一系列门静脉高压并发症的微创介入治疗技术。 自20世纪80年代末R.ssle等首次采用TIPS成功治疗1例门静脉高压静脉曲张出血伴大量腹腔积液患者以来,该技术广泛用于治疗门静脉高压并发症,适应证也逐步扩展。TIPS技术20世纪90年代初被引入中国,在徐克等国内最早开展TIPS 的一批介入放射学专家的不懈努力下,TIPS技术得以在全国范围内大力推广,并取得了可喜的成绩。 经过近30年的不断探索和发展,对TIPS的适应证、禁忌证、技术操作标准、血管内支架的选择和术后并发症等方面的认识已经有了明显提升。为了进一步规范TIPS的临床应用并提高疗效,中华医学会放射学分会介入学组组织有关专家,参考近年来国内外同类文献并结合我国的实践经验,在最新门静脉高压或TIPS相关专家共识或指南的基础上,经反复讨论后初步达成以下共识,以期对临床实践起到指导作用。 本共识以已发表的文献为基础,主要面向临床医师,在应用中兼顾灵活性。采用证据质量分级和推荐强度系统(GRADE)。证据质量分为高(A)、中(B)、低或极低(C)3个等级,推荐强度分为强(1)、弱(2)2个等级(表1)。证据质量越高,推荐强度越强。在没有明确证据存在的条件下,推荐意见主要基于参与讨论专家的共识。 TIPS 适应证 一、急性食管静脉曲张出血的推荐意见 1 “挽救性”TIPS:肝功能Child-Pugh A级经药物和内镜治疗失败的急性出血,覆膜支架TIPS可以作为挽救措施(B,1)。 急性食管胃静脉曲张出血是肝硬化患者的致命性并发症,6周病死率高达15%~20%。目前,急性静脉曲张出血的标准治疗方法是血管活性药物(特利加压素或生长抑素等)联合内镜治疗(内镜套扎),并尽早使用抗生素。对于经药物及内镜治疗5d 内不能控制的出血或再出血,可选择“挽救性”TIPS治疗。15项观察性研究的结果显示,TIPS对急性静脉曲张出血患者的出血控制率达90%~100%。 2. 早期TIPS:对于食管静脉曲张及Ⅰ型、Ⅱ型食管胃静脉曲张(GOV1 和GOV2)急性出血的患者,在初次药物联合内镜治疗后,若存在治疗失败的高危因素(Child-Pugh 评分C 级GOV1)、大小、红色征及肝功能不全严重程度相关。 急性胃曲张静脉出血首选治疗与食管静脉曲张出血类似,包括液体复苏、血管活性药物、抗生素和诊断性内镜等。对保守治疗难以控制的急性胃静脉曲张出血,挽救性TIPS可以使高达95%的患者获得迅速止血。对于再出血风险较高的胃底曲张静脉出血(GOV2和IGV1),可以优先考虑行TIPS。 GOV1再出血的预防策略与食管曲张静脉类似。TIPS预防胃静脉曲张再出血的效果与预防食管静脉曲张再出血相当。TIPS治疗组胃静脉曲张再出血发生率明显低于内镜下注射组织胶,但TIPS组HE发生率较高,且生存率未改善。需要注意的是,胃静脉曲张出血患者的术前门静脉压力梯度(PPG)通常低于食管静脉曲张出血患者。因此,单纯的减压治疗可能不是最佳治疗方法,应在减压的同时联合曲张静脉或自发性分流道栓塞。对于存在较大自发性胃-肾、脾-肾分流道的患者,或有TIPS禁忌证的患者(如高龄、顽固性HE、肝功能较差等),可以考虑行球囊导管闭塞下逆行性静脉栓塞术(BRTO)。 四、顽固性腹腔积液、肝性胸腔积液和肝肾综合征的推荐意见 1. 对肝硬化顽固性或复发性腹腔积液:对肝硬化顽固性或复发性腹腔积液患者,建议优先考虑覆膜支架TIPS 治疗。对有心脏舒张功能障碍(二尖瓣口舒张早期峰值/舒张晚期血流峰值≤1)、年龄>60 岁、胆红素>3 g/L、血小板计数3 g/L、血小板计数13分或者终末期肝病评分>18分。 4.重度肺动脉高压。 5.严重肾功能不全。 6.快速进展的肝衰竭。 7.肝脏弥漫性恶性肿瘤。 8.对比剂过敏。 二、相对禁忌证 1.先天性肝内胆管囊状扩张(Caroli病)、胆道阻塞性扩张。 2.肝脏体积明显缩小。 3.多囊性肝病。 4.门静脉海绵样变。 5.中度肺动脉高压。 6.重度或顽固性HE。 7.胆红素>3 g/L。 8.重度凝血病。 TIPS 术前检查和评估 TIPS术前检查和评估内容主要包括实验室检查(血常规、凝血功能、肝功能、肾功能等),影像检查(了解肝后段下腔静脉、肝静脉与门静脉的位置关系,PVT范围及程度等),上消化道内镜(对曲张静脉进行分类)。肝硬化患者,应首先明确肝硬化病因和诊断,全面检查并发症,排除显性HE患者。顽固性胸腔积液或腹腔积液患者,术前应行胸腔穿刺术或腹腔穿刺术。 值得注意的是,对所有准备接受TIPS的患者,建议行超声心动图检查以排除显著收缩性或舒张性心功能不全。对于超声心动图上收缩性肺动脉压>50 mmHg(1 mmHg=0.133 kPa)、充血性心力衰竭、三尖瓣反流或心肌病的患者建议进行右心置管来进一步排除肺动脉高压(平均肺动脉压>45 mmHg为重度肺动脉高压、平均肺动脉压35~45 mmHg 为中度肺动脉高压、平均肺动脉压25~34 mmHg为轻度肺动脉高压)。 TIPS 技术操作流程和重要注意事项 一、门静脉显像 必要时先行间接门静脉造影术,有条件者可行肝静脉球囊阻断逆行CO2造影术。 二、麻醉 根据医疗中心的条件、操作者的经验以及患者状态决定麻醉方法。该技术可在局部麻醉下完成。对于年老、儿童或对疼痛耐受性差的患者可联合使用异丙酚和瑞芬太尼。对于急性出血且血流动力学不稳定的患者可采用全身麻醉和气管插管。 三、颈内静脉穿刺 通常选择右侧颈内静脉穿刺,如果右侧颈内静脉由于解剖等原因无法穿刺成功,可以尝试穿刺左侧颈内静脉或股静脉。鼓励采用超声引导下经颈内静脉穿刺(尤其对于伴有颈内静脉解剖异常或颈内静脉血栓的患者),可以减少穿刺并发症。 四、肝静脉插管 颈内静脉穿刺成功后,将导丝送入下腔静脉,调整导丝进入肝右静脉或肝中静脉,将穿刺系统选择性插入肝静脉,测量并记录游离肝静脉压。有条件者建议准确测量HVPG。如果无法进行肝静脉置管,可以进行超声引导下肝静脉穿刺。如果无可用肝静脉,可以直接从下腔静脉穿刺门静脉。 五、门静脉穿刺 门静脉穿刺常用的定向方法包括影像资料、门静脉造影、CO2逆行造影和实时超声引导等。在这些方法的指导下,通常选择距离最短、弯曲角度最小的门静脉进行穿刺。对于肝静脉、门静脉走行及位置关系相对复杂的患者(如肝右叶萎缩、BCS、PVT),术前CT和MRI可以帮助操作者判断从肝静脉穿刺门静脉的最佳途径。对肝静脉萎缩、闭塞或寻找困难的门静脉高压患者,可以选择第二肝门附近的下腔静脉肝后段进行门静脉穿刺。 六、建立门腔通道 从肝静脉穿刺门静脉成功后,通过注射对比剂判断所穿刺管腔是否为肝内门静脉分支。判断准确无误后,用超滑导丝调整进入脾静脉或肠系膜上静脉进行直接门静脉造影,测量基线水平的门静脉压力、下腔静脉压力,计算门静脉和下腔静脉压力差,作为门静脉压力梯度(PPG)。 七、球囊导管扩张术及血管内支架植入术 沿导丝送入球囊导管并扩张穿刺道,通常采用8 mm球囊。结合球囊扩张时的切迹及血管造影结果选择合适的血管内支架,定位后释放。释放支架时要注意各种支架的特性。随机对照研究结果显示,覆膜支架TIPS可以显著降低支架功能障碍,但对HE和生存无明显影响。 如果使用TIPS专用支架(美国Gore and Associates 公司Viatorr 支架),远心端覆膜部分应开始于门静脉和肝实质的汇合处,近心端应到达肝静脉下腔静脉入口处,同时避免支架过度进入下腔静脉或右心房,以免增加今后肝移植手术的难度。对于非TIPS专用支架,近心端标准同上,支架下端应尽可能顺应门静脉走行。对于术中支架两端位置欠佳者,可直接叠放支架予以矫正。检查血流通过支架的顺畅性,并再次测量门静脉和脾静脉压力及下腔静脉压力,计算PPG。 八、术后PPG的测量和最佳阈值 PPG的测量建议选择门静脉-下腔静脉压力梯度(在清醒或轻度镇静的状态下,分别在门静脉主干和下腔静脉支架引流处测量,对于急诊TIPS,建议在患者状态稳定后重复测量PPG)。 有些医疗中心采用门静脉压力与右心房压力的差值作为PPG,但由于右心房压力代表胸腔压力,比腹压略低,并不能很好地体现跨肝脏的压力梯度。门静脉-下腔静脉压力梯度要比门静脉-右心房压力梯度低2.5mmHg。对于曲张静脉破裂出血,PPG降低到12mmHg 或以下,曲张静脉再出血的风险显著降低。PPG比基线水平降低50%以上可以显著降低曲张静脉再出血风险[。 对于胃底曲张静脉,目前最佳PPG尚未确定,通常认为预防胃底静脉曲张破裂出血所需的压力要低于12 mmHg。顽固性腹腔积液患者术后最佳PPG 尚不清楚,推荐降至8mmHg以下。由于腹腔积液的形成不仅与门静脉高压相关,而且受到肾功能的影响,因此很难确定顽固性腹腔积液患者的降压最佳阈值。 九、门体侧支血管的栓塞 是否在TIPS手术的同时进行侧支血管栓塞目前仍存在争议。一项纳入6项研究的Meta分析结果显示,TIPS术中联合曲张静脉栓塞较单独TIPS降低了再出血发生率,而支架狭窄、HE发生率差异无统计学意义。伴有顽固性HE的肝硬化患者中,71%的患者存在脾肾分流道。因此,栓塞大的自发性门腔分流道可以作为顽固性HE的一个治疗靶点,从而有效降低HE的发生。门体侧支血管栓塞可在门腔静脉通道建立以后直接栓塞,也可以在支架植入后进行。 推荐意见:肝静脉置管后建议准确测量HVPG(B,1)。支架上端应达到肝静脉入下腔静脉口,非TIPS专用支架下端应顺应门静脉走行(B,1)。PPG的测量建议选择门静脉-下腔静脉压力梯度(B,1)。 对曲张静脉出血,建议PPG 降低到12 mmHg 以下或降低50%(A,1)。对顽固性腹腔积液患者实施TIPS治疗,HVPG降低的要求虽然目前尚无明确证据,但推荐降至8 mmHg以下(C,2)。 TIPS 并发症及处理 一、手术相关并发症 目前TIPS操作相关并发症并不常见,而且会随着操作者经验的提高而减少。其中腹腔内出血是最严重的TIPS 操作相关并发症。误穿刺肝动脉、胆管、肝外门静脉,操作时导丝引起肠系膜血管壁撕裂伤均可造成腹腔出血,肝被膜穿刺伤亦可造成出血;此外,部分患者的肝脏缩小,且伴发的张力性腹腔积液使肝脏上移,也将增加穿刺至肝外门静脉造成血管壁撕裂伤出血的风险。 多数出血是为自限性,可通过植入覆膜支架进行止血。对于大出血患者应密切观察,必要时行外科开腹修补术。其他并发症如误穿刺入胆囊胆管致门静脉胆管瘘或胆汁性腹膜炎、穿刺后感染或脓肿形成、心律失常、支架移位等较少见。 二、支架功能障碍 裸支架TIPS后1年分流道狭窄率高达50%,覆膜支架TIPS 后1 年支架功能障碍发生率降至12%。支架的位置与术后支架功能障碍的发生有密切联系,支架上端尽可能接近肝静脉入下腔静脉口,非TIPS专用支架门静脉端应顺应血管走行,以降低术后狭窄率。TIPS术后是否进行抗凝尚缺乏循证医学证据。 三、HE TIPS 术后1 年HE 发生率为15%~48%,多出现在术后1~3 个月。目前对HE 分级多参照West-haven 标准。年龄>65 岁、肝功较差、术前HE史或术前轻微HE是TIPS术后HE的主要预测因素。目前尚无措施可以有效预防TIPS 术后HE。利福昔明、拉克替醇以及术后输注白蛋白都不能有效预防TIPS术后HE的发生。使用小直径支架是否可以预防术后HE的发生,目前仍存在争议,需要进一步研究证实。 TIPS术后HE的治疗首先应积极寻找及祛除诱因。治疗HE的主要药物包括乳果糖、利福昔明、门冬氨酸鸟氨酸、支链氨基酸等,对以上治疗无效的顽固性HE患者,可以选择支架限流或封堵术改善HE,但随着门静脉压力的升高,曲张静脉出血或腹腔积液可能会复发。对于伴有粗大自发性门腔分流道的患者,可以通过栓塞或封堵粗大自发性门腔分流道来改善HE。部分顽固性HE是由肝功能恶化引起而非过度分流导致,即使给予限流或封堵分流道也不会明显改善。因此,采用支架限流或封堵术时,应当综合考虑,权衡利弊。目前,肝移植被认为是难治性HE的最终治疗方法。 推荐意见:推荐使用覆膜支架预防TIPS 术后支架功能障碍的发生,应尽可能选用TIPS 专用支架(A,1)。目前尚无有效的方法预防TIPS 术后HE(B,1)。对于伴有粗大自发性门腔分流道的患者,可以通过栓塞或封堵粗大自发性门腔分流道来改善HE(C,2)。对肝功能较好的顽固性HE 患者,可以选择支架限流或封堵术改善HE(B,2)。 TIPS将传统的外科分流模式改变为肝内分流模式,兼备创伤小、无需全身麻醉以及并发症少等优点。早期TIPS可以改善高危急性曲张静脉出血患者的生存。覆膜支架TIPS在改善顽固性或复发性腹腔积液生存方面的证据逐渐增强。在其他情况下,TIPS通常作为肝硬化消化道出血保守治疗或标准治疗失败后的二线治疗方法。对于PVT 或BCS等肝脏血管疾病,哪些患者可以从TIPS中最大获益目前仍有待进一步的研究。TIPS术后HE等并发症仍制约着TIPS的广泛应用,改良穿刺、分流路径或限制分流的支架研发值得期待。 专家共识委员会成员(按照姓氏拼音顺序排序):程英升(上海市第十医院介入科);程永德(介入放射学杂志编辑部);崔进国(白求恩国际和平医院放射诊断科);单鸿(广州中山大学第三附属医院放射介入科);高宏(中华放射学杂志编辑部);顾建平(南京市第一医院放射影像科);郭志(天津肿瘤医院介入治疗科);韩国宏(第四军医大学西京消化病医院消化介入科);姜卫剑(解放军火箭军总医院血管神经外科);李麟逊(江苏省人民医院放射科);李肖(四川大学华西医院介入诊疗中心);李选(北京大学第三医院介入血管外科);李彦豪(南方医科大学南方医院放射介入科);刘兆玉(中国医科大学附属盛京医院放射科);卢再鸣(中国医科大学附属盛京医院放射科);陆骊工(珠海市人民医院);欧阳强(上海新华医院放射科);任伟新(新疆医科大学第一附属医院放射介入科);史红(中华医学电子音像出版社);滕皋军(东南大学中大医院放射科);王峰(大连医科大学附属第一医院介入科);王建华(复旦大学附属中山医院介入科);徐克(中国医科大学附属第一医院放射科);殷占新(第四军医大学西京消化病医院消化介入科);翟仁友(首都医科大学附属北京朝阳医院放射科);张晓冬(中华放射学杂志编辑部);郑传胜(华中科技大学同济医学院附属协和医院放射介入科);钟红珊(中国医科大学附属第一医院放射科);周石(贵阳医学院附属医院介入科);朱康顺(广州中山大学附属第三医院介入科);邹英华(北京大学第一医院介入血管外科) 本共识未受到相关设备、材料和药物企业的影响
杨晴 主任医师 珠海市人民医院医疗集团 肝病科9612人已读 - 精选 原发性肝癌诊疗规范(2017年版)
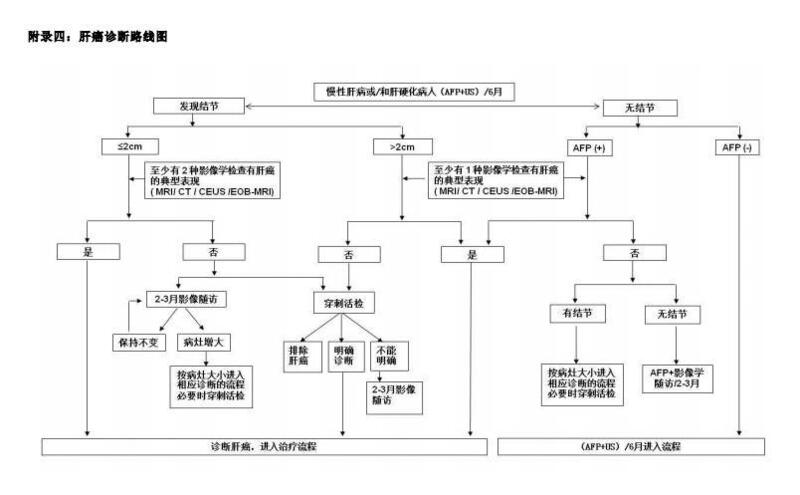
原发性肝癌诊疗规范(2017年版) 一、概述 原发性肝癌是目前我国第四位的常见恶性肿瘤及第三位的肿瘤致死病因,严重威胁我国人民的生命和健康1,2。原发性肝癌主要包括肝细胞癌(Hepatocellular Carcinoma,HCC)、肝内胆管癌(Intrahepatic Cholangiocarcinoma,ICC)和HCC-ICC混合型三种不同病理类型,三者在发病机制、生物学行为、组织学形态、治疗方法以及预后等方面差异较大,其中肝细胞癌占到85%-90%以上,因此本规范中的“肝癌”指肝细胞癌。 二、筛查和诊断 (一)高危人群的监测筛查: 对肝癌高危人群的筛查,有助于早期发现、早期诊断、早期治疗,是提高肝癌疗效的关键。在我国,肝癌的高危人群主要包括:具有乙型肝炎病毒(Hepatitis B virus,HBV)和/或丙型肝炎病毒(Hepatitis C virus,HCV)感染、长期酗酒、非酒精脂肪性肝炎、食用被黄曲霉毒素污染食物、各种原因引起的肝硬化、以及有肝癌家族史等的人群,尤其是年龄40岁以上的男性风险更大。血清甲胎蛋白(Alpha-fetoprotein,AFP)和肝脏超声检查是早期筛查的主要手段,建议高危人群每隔6个月进行至少一次检查3。 (二)肝癌的影像学检查: 各种影像学检查手段各有特点,应该强调综合应用、优势互补、全面评估。 1. 超声检查(Ultrasonography, US): 腹部超声检查因操作简便、灵活直观、无创便携等特点,是临床上最常用的肝脏影像学检查方法。常规超声筛查可以早期、敏感地检出肝内可疑占位性病变,准确鉴别是囊性或实质性占位,并观察肝内或腹部有无其他相关转移灶。彩色多普勒血流成像不仅可以观察病灶内血供,也可明确病灶与肝内重要血管的毗邻关系,为临床治疗方法的选择及手术方案的制定提供重要信息。实时超声造影技术可以揭示肝肿瘤的血流动力学改变,帮助鉴别和诊断不同性质的肝肿瘤,凭借实时显像和多切面显像的灵活特性,在评价肝肿瘤的微血管灌注和引导介入治疗方面具有优势。 2. X线计算机断层成像(Computed Tomography, CT): 常规采用平扫+增强扫描方式(常用碘对比剂),其检出和诊断小肝癌能力总体略逊于磁共振成像。目前除常见应用于肝癌临床诊断及分期外,更多应用于肝癌局部治疗的疗效评价,特别对经肝动脉化疗栓塞(Transarterialchemoembolization,TACE)后碘油沉积观察有优势。同时,借助CT的三维肝体积和肿瘤体积测量、肺和骨等其它脏器转移评价,临床应用广泛。 3. 磁共振成像(Magnetic Resonance Imaging, MRI): 常规采用平扫+增强扫描方式(常用对比剂Gd-DTPA),因其具有无辐射影响,组织分辨率高,可以多方位、多序列参数成像,并具有形态结合功能(包括弥散加权成像、灌注加权成像和波谱分析)综合成像技术能力,成为临床肝癌检出、诊断和疗效评价的常用影像技术。若结合肝细胞特异性对比剂(Gd-EOB-DTPA)使用,可提高≤1.0cm肝癌的检出率和对肝癌诊断及鉴别诊断的准确性4-9。 在MRI或 CT增强扫描动脉期(主要在动脉晚期),肝癌呈不均匀明显强化,偶可呈均匀明显强化,尤其是≤5.0cm的肝癌,门脉期和/或实质平衡期扫描肿瘤强化明显减弱或降低,这种“快进快出”的增强方式是肝癌诊断的特点10,11。 肝癌MRI和CT诊断,尚需结合其它征象(如假包膜等),尤其是MRI其它序列上相关征象进行综合判断,方能提高肝癌诊断准确性。 4.数字减影血管造影(Digital SubtractionAngiography, DSA): DSA是一种侵入性创伤性检查,多主张采用经选择性或超选择性肝动脉进行DSA检查,该技术更多用于肝癌局部治疗或急性肝癌破裂出血治疗等。肝癌在DSA的主要表现是肿瘤血管和肿瘤染色,还可以明确显示肝肿瘤数目、大小及其血供情况。DSA能够为血管解剖变异和重要血管解剖关系以及门静脉浸润提供正确客观的信息,对于判断手术切除的可能性和彻底性以及决定合理的治疗方案有重要价值。 5.核医学影像检查: (1)正电子发射计算机断层成像(Positron Emission Tomography/CT, PET/CT) :氟-18-脱氧葡萄糖(18F-FDG)PET/CT全身显像的优势在于:①对肿瘤进行分期,通过一次检查能够全面评价淋巴结转移及远处器官的转移12,13(证据等级1);②再分期,因PET功能影像不受解剖结构的影响,可准确显示解剖结构发生变化后或者是解剖结构复杂部位的复发转移灶14,15(证据等级2);③疗效评价,对于抑制肿瘤活性的靶向药物,疗效评价更加敏感、准确16,17(证据等级2);④指导放疗生物靶区的勾画、穿刺活检部位14,15(证据等级2);⑤评价肿瘤的恶性程度和预后18-20(证据等级2)。碳-11标记的乙酸盐(11C-acetate)或胆碱(11C-choline)PET显像可提高对高分化肝癌诊断的灵敏度,与18F-FDG PET/CT显像具有互补作用21,22。 (2)发射单光子计算机断层扫描仪(SPECT-CT): SPECT/CT已逐渐替代SPECT成为核医学单光子显像的主流设备,选择全身平面显像所发现的病灶,再进行局部SPECT/CT融合影像检查,可同时获得病灶部位的SPECT和诊断CT图像,诊断准确性得以显著提高23。 6. 肝穿刺活检: 具有典型肝癌影像学特征的占位性病变,符合肝癌的临床诊断标准的病人,通常不需要以诊断为目的肝穿刺活检24。对于缺乏典型肝癌影像学特征的占位性病变,肝穿刺活检可获得病理诊断,对于确立肝癌的诊断、指导治疗、判断预后非常重要。 肝穿刺活检需要在超声或CT引导下进行,可采用18G或16G肝穿刺空芯针活检获得组织学诊断,也可用细针穿刺获得细胞学诊断。肝穿刺活检主要的风险是出血或针道种植。因此,术前应检查血小板和凝血功能,对于有严重出血倾向或严重心肺、脑、肾疾患和全身衰竭的病人,应避免肝穿刺活检。为了避免肿瘤结节破裂和针道种植,在选择穿刺路径需要经过正常的肝组织,避免直接穿刺肝脏表面的结节。推荐在肿瘤和肿瘤旁肝组织分别穿刺1条组织,以便客观对照提高诊断准确性。肝穿刺的病理诊断存在一定的假阴性率,阴性结果不能完全排除肝癌的可能。 (三)肝癌的血清学分子标记物: 血清甲胎蛋白(Alpha-fetoprotein, AFP)是当前诊断肝癌常用而又重要的方法。诊断标准:AFP≥400μg/L,排除慢性或活动性肝炎、肝硬化、睾丸或卵巢胚胎源性肿瘤以及怀孕等。AFP低度升高者,应作动态观察,并与肝功能变化对比分析,有助于诊断。约30%的肝癌病人AFP水平正常,检测甲胎蛋白异质体,有助于提高诊断率25。其它常用的肝癌诊断分子标志物:包括α-L-岩藻苷酶、异常凝血酶原等。 (四)肝癌的病理学诊断: 1. 肝癌病理学诊断标准: 肝脏占位病灶或者肝外转移灶活检或手术切除组织标本,经病理组织学和/或细胞学检查诊断为肝癌。病理诊断须与临床证据相结合,全面了解病人的HBV/HCV感染史、肿瘤标志物以及影像学检查等信息。 2. 肝癌病理诊断规范: 肝癌病理诊断规范由标本处理、标本取材、病理检查和病理报告等部分组成。 (1)标本处理要点:①手术医生应在病理申请单上标注送检标本的部位、种类和数量,对手术切缘和重要病变可用染料染色或缝线加以标记;②尽可能将肿瘤标本在离体30 min以内完整送达病理科切开固定;③10%中性福尔马林溶液固定 12~24 小时。 (2)标本取材要点:肝癌周边区域是肿瘤生物学行为的代表性区域26。为此,应采用“7点”基线取材法(图 1),在肿瘤的12 点、3点、6点和9点位置上于癌与癌旁肝组织交界处取材按1:1取材;在肿瘤内部至少取材 1 块;对距肿瘤边缘≤1cm(近癌旁)和>1cm(远癌旁)范围内的肝组织分别取材1块。鉴于多结节性肝癌具有单中心和多中心两种起源方式,在不能除外由肝内转移引起的卫星结节的情况下,单个肿瘤最大直径≤3cm的肝癌,应全部取材检查。实际取材的部位和数量还须根据肿瘤的直径和数量等情况考虑27(证据等级2)。 图 1. 肝脏肿瘤标本基线取材部位示意图 (3)病理描述要点: ①大体标本描述28:重点描述肿瘤的大小、数量、颜色、质地、与血管和胆管的关系、包膜状况、周围肝组织病变、肝硬化类型、肿瘤至切缘的距离以及切缘受累情况等。 ②显微镜下描述28:肝癌的诊断参照WHO2010版(参见附录二),重点描述以下内容:肝癌的分化程度:可采用国际上常用的 Edmondson-Steiner 四级(I-IV)分级法(参见附录三);肝癌的组织学类型:常见有细梁型、粗梁型、假腺管型和团片型等;肝癌的特殊细胞类型:如透明细胞型、富脂型、梭形细胞型和未分化型等;肿瘤坏死(如肝动脉化疗栓塞治疗后)、淋巴细胞浸润及间质纤维化的范围和程度;肝癌生长方式:包括癌周浸润、包膜侵犯或突破、微血管侵犯和卫星结节等;慢性肝病评估:肝癌常伴随不同程度的慢性病毒性肝炎或肝硬化,推荐采用较为简便的Scheuer 评分系统和中国慢性病毒性肝炎组织学分级和分期标准29-31。 微血管侵犯(Microvascular invasion ,MVI)是指在显微镜下于内皮细胞衬覆的脉管腔内见到癌细胞巢团,以门静脉分支为主(含包膜内血管)32(证据等级1);病理分级方法:M0:未发现 MVI;M1(低危组):≤5 个 MVI,且发生于近癌旁肝组织;M2(高危组):> 5 个MVI,或MVI发生于远癌旁肝组织33。MVI是评估肝癌复发风险和选择治疗方案的重要参考依据,应作为常规病理检查指标34-36(证据等级2)。 ③免疫组化检查:常用的肝细胞性标志物有Hep Par-1、GPC-3、CD10、Arg-1和GS等;常用的胆管细胞标志物有CK7、CK19和MUC-1等。需要合理组合使用免疫组化标志物,对HCC与ICC,以及原发性肝癌与转移性肝癌进行鉴别诊断28,33。 ④特殊类型肝癌:混合型肝癌:在同一个肿瘤结节内同时存在HCC和ICC两种组织学成分;双表型肝癌:HCC同时表达胆管癌蛋白标志物;纤维板层型肝癌:癌细胞富含嗜酸性颗粒状胞浆,癌组织被平行排列的板层状胶原纤维组织分隔成巢状28,33。 3.肝癌病理诊断报告: 由大体标本描述、显微镜下描述、免疫组化检查结果、典型病理照片及病理诊断名称等部分组成。此外,还可附有与肝癌克隆起源、药物靶点检测、生物学行为评估以及预后判断等相关的分子病理学检查结果,提供临床参考。 (五)肝癌的临床诊断标准及路线图: 乙型或丙型肝炎以及肝硬化是肝癌的高危因素,对于肝脏占位性病变的诊断和鉴别诊断有重要的价值。近年来,非酒精性脂肪性肝炎(NASH)与肝癌的关系越来越引起重视。—— AFP在缺乏敏感的影像学方法情况下曾用于肝癌的临床诊断,如果AFP≥400μg/L,在排除妊娠、慢性或活动性肝病以及生殖腺胚胎源性肿瘤情况下,则高度提示肝癌。 结合肝癌发生的高危因素、影像学特征以及血清学分子标记物,依据路线图的步骤对肝癌做出临床诊断(参见附录四)。 1. 有乙型肝炎或丙型肝炎,或者有任何原因引起肝硬化者,至少每隔6个月进行一次超声及AFP检测,发现肝内直径≤2cm结节,动态增强MRI、动态增强CT、超声造影及普美显动态增强MRI四项检查中至少有两项显示有动脉期病灶明显强化、门脉或延迟期强化下降的“快进快出”的肝癌典型特征,则可做出肝癌的临床诊断;对于发现肝内直径>2cm的结节,则上述四种影像学检查中只要有一项有典型的肝癌特征,即可临床诊断为肝癌。 2. 有乙型肝炎或丙型肝炎,或者有任何原因引起肝硬化者,随访发现肝内直径≤2cm结节,若上述四种影像学检查中无或只有一项检查有典型的肝癌特征,可进行肝穿刺活检或每2-3个月密切的影像学随访以确立诊断;对于发现肝内直径>2cm的结节,上述四种影像学检查无典型的肝癌特征,则需进行肝穿刺活检以确立诊断。 3. 有乙型肝炎或丙型肝炎,或者有任何原因引起肝硬化者,如AFP升高,特别是持续增高,应该进行上述四种影像学检查以确立肝癌的诊断,如未发现肝内结节,在排除妊娠、活动性肝病、生殖胚胎源性肿瘤以上消化道癌的前提下,应该密切随访AFP水平以及每隔2-3个月一次的影像学复查。 三、分期 肝癌的分期对于预后的评估、合理治疗方案的选择至关重要。影响肝癌病人预后的因素很多,包括肿瘤因素、病人一般情况及肝功能情况,据此国外有多种的分期方案,如:BCLC、TNM、JSH、APASL等分期。依据中国的具体国情及实践积累,推荐下述肝癌的分期方案,包括:Ia期、Ib期、IIa期、IIb期、IIIa期、IIIb期、IV期,具体分期方案参见附录五。 四、治疗 肝癌治疗领域的特点是多种方法、多个学科共存,而以治疗手段的分科诊疗体制与实现有序规范的肝癌治疗之间存在一定的矛盾。因此肝癌诊疗须重视多学科诊疗团队的模式,从而避免单科治疗的局限性,为病人提供一站式医疗服务、促进学科交流,并促进建立在多学科共识基础上的治疗原则和指南。合理治疗方法的选择需要有高级别循证依据支持,但也需要同时考虑地区和经济水平差异。 (一)肝切除术: 肝癌的外科治疗是肝癌病人获得长期生存最重要的手段,主要包括肝切除术和肝移植术。 1.肝切除术的基本原则: (1)彻底性:完整切除肿瘤,使切缘无残留肿瘤; (2)安全性:保留有足够功能肝组织(具有良好血供以及良好的血液和胆汁回流)以术后肝功能代偿,降低手术死亡率及手术并发症。 2.术前肝功能储备的评估: 在术前应对病人的全身情况及肝功能储备进行全面评价:常采用美国东部肿瘤协作组提出的功能状态评分(ECOG PS)来评估病人的全身情况;采用Child-Pugh评分、吲哚氰绿(ICG)清除试验37或瞬时弹性成像测定肝脏硬度37-40评价肝功能储备情况;如预期保留肝组织体积较小,则采用CT和/或MRI测定剩余肝的体积,并计算剩余肝体积占标准化肝脏体积的百分比38。一般认为Child-Pugh A级、ICG15<20%-30%是实施手术切除的必要条件;余肝体积须占标准肝体积的40%以上(肝硬化病人),或30%以上(无肝硬化病人)也是实施手术切除的必要条件。 3.肝癌切除的适应证: (1)肝脏储备功能良好的Ia期、Ib期和IIa期肝癌是手术切除的首选适应证,尽管有以往研究显示对于直径≤3cm肝癌,切除和射频消融疗效无差异41(证据等级1),但最近的研究显示外科切除的远期疗效更好42-44(证据等级1)。 (2)在部分IIb期和IIIa期肝癌病人中,手术切除有可能获得比其他治疗方式更好的效果45,46(证据等级1),但需更为谨慎的术前评估。对于多发性肝癌,相关研究显示,在满足手术安全性的条件下,肿瘤数目≤3枚的多发性肝癌病人可能从手术获益45,47(证据等级1);若肿瘤数目>3枚,即使已手术切除,在多数情况下其疗效也并不优于TACE等非手术治疗。 (3)对于其它IIb期和IIIa期肝癌,如有以下情况也可考虑手术切除,如肿瘤数目>3枚,但肿瘤局限在同一段或同侧半肝者,或可同时行术中射频消融处理切除范围外的病灶;合并门静脉主干或分支癌栓者,若肿瘤局限于半肝,且预期术中癌栓可完整切除或取净,可考虑手术切除肿瘤并经门静脉取栓,术后再结合TACE、门静脉化疗或其他全身治疗措施;如合并胆管癌栓且伴有梗阻性黄疸,肝内病灶亦可切除的病人;伴有肝门部淋巴结转移者,切除肿瘤的同时行淋巴结清扫或术后外放射治疗;周围脏器受侵犯,但可一并切除者。 此外,对于术中探查不适宜切除的肝癌,可考虑术中肝动脉结扎(已少用,有时用于肝癌破裂出血时的手术止血)和(或)肝动脉、门静脉插管化疗、或术中其他的局部治疗措施等。 4. 肝癌根治性切除标准: (1)术中判断标准:①肝静脉、门静脉、胆管以及下腔静脉未见肉眼癌栓;②无邻近脏器侵犯,无肝门淋巴结或远处转移;③肝脏切缘距肿瘤边界>1cm;如切缘< 1cm,但切除肝断面组织学检查无肿瘤细胞残留,即切缘阴性。 (2)术后判断标准:①术后2个月行超声、CT、MRI(必须有其中两项)检查未发现肿瘤病灶;②如术前AFP 升高,则要求术后2个月AFP 定量测定,其水平在正常范围(极个别病人AFP降至正常的时间超过2个月)。 5.手术切除技术: 常用的肝切除主要是包括入肝和出肝血流控制技术、肝脏离断技术以及止血技术。手术技术方面,有经验的医师可开展腹腔镜或机器人辅助微创肝切除术。微创手术具有创伤小和术后恢复快等优点48(证据等级2),但其长期疗效仍需要与传统的开腹手术进行前瞻性的多中心的随机对照研究。经腹腔镜行肝癌切除的指征:①病变位于CouinaudII、III、IVb、V、VI段;②病变大小以不影响第一和第二肝门的解剖为准,一般不超过10cm;③有丰富经验的医师可逐步开展腹腔镜半肝切除、肝3叶切除和CouinaudI、VII、VIII段肝切除。 切除范围较大导致余肝体积过少或顾忌余肝的功能,是阻碍根治性切除的主要原因。为了提高肝癌的可切除性,可采用如下方法: (1)术前TACE可使部分病人的肿瘤缩小后再切除49,50; (2)经门静脉栓塞(Portalvein thrombosis,PVE)或门静脉结扎(Portalvein ligation,PVL)主瘤所在半肝,使余肝代偿性增大后再切除51。临床报告其并发症不多,因需4-6周时间等待对侧肝组织体积增大,为减少等待期间肿瘤进展的风险,可考虑与TACE联合52。 (3)联合肝脏分隔和门静脉结扎的二步肝切除术(Associatingliver partition and portal vein ligation for staged hepatectomy,ALPPS)是近年发展的新技术53,,适合于预期残余肝脏体积占标准肝体积不足30%-40%的病人,经过I期的肝脏分隔或离断和患侧门静脉分支结扎后,健侧剩余肝脏体积(futureliver reserve, FLR)一般在1-2周后增生30%-70%以上,FLR占标准肝脏体积至少30%以上,可接受安全的II期切除。术前评估非常重要,需要考虑肝硬化的程度、病人年龄、短期承受两次手术的能力和肿瘤快速进展的风险54;此外可借助腹腔镜技术或消融技术等降低二次手术的创伤55。ALPPS的禁忌证:①存在不可切除的肝外转移灶;②严重的门静脉高压症;③全身麻醉高风险病人以及一般状况较差不能耐受大手术的病人;④I期手术后FLR中有肉眼可见肝癌结节。ALPPS应用可在短期内提高肝癌的切除率,但同时也存在高并发症发生率及死亡率,应谨慎、合理地选择手术对象。 (4)对于开腹后探查发现肝硬化较重、肿瘤位置深在、多结节的肿瘤,术中消融可降低手术风险。 解剖性切除与非解剖性切除均为常用的手术技术。对于巨大肿瘤,可采用不游离肝周韧带的前径路肝切除法56。对于多发性肿瘤,可采用手术切除结合术中消融(如术中射频等)方式治疗,切除肝脏边缘肿瘤,消融深部肿瘤。对于门静脉癌栓者,行门静脉取栓术时应暂时阻断健侧门静脉血流,防止癌栓播散57。对于肝静脉癌栓或腔静脉癌栓者,可行全肝血流阻断,尽可能整块去除癌栓58。合并右心房癌栓者,可开胸切开右心房取出癌栓,同时切除肝肿瘤。合并腔静脉或右心房癌栓时手术风险较大,应慎重选择。对于肝癌伴胆管癌栓者,在去除癌栓的同时,若肿瘤已部分侵犯胆管壁,则应同时切除受累胆管并重建胆道,以降低局部复发率59。 6. 术前治疗: 对于不可切除肝癌,肝动脉结扎插管、TACE、外放射等治疗可能导致肿瘤降期从而使部分病人获得手术切除的机会,降期后切除的肝癌病人可能获得较好的长期生存效果49。对于可切除肝癌,术前TACE并不能改善病人生存60,61(证据等级2)。 7.术后治疗(转移复发的防治): 肝癌手术切除后5年肿瘤复发转移率高达40%-70%,这与术前可能已存在微小播散灶或者多中心发生有关,故所有病人术后需要接受密切随访。一旦发现肿瘤复发,根据肿瘤复发的特征,可以选择再次手术切除、局部消融、TACE、放疗或系统治疗等,延长病人生存期。对于高危复发者,有临床研究证实术后TACE治疗有一定的效果,能发现并控制术后肝内微小残癌62(证据等级4),但该结论需要进一步证实。此外,对于伴有门静脉癌栓病人术后经门静脉置管化疗联合肝动脉化疗栓塞,也可延长病人生存63。尽管有临床随机研究提示,干扰素α可减少复发延长生存64-66(证据等级1),但仍存争议67,目前仅推荐应用于合并慢性乙肝背景的肝癌术后病人。有报道发现肝癌miR-26a表达与干扰素α辅助治疗的疗效相关68,该结果也需要进一步多中心随机对照证实。亦有大会报道,国内多中心随机平行对照研究结果表明,中药槐耳颗粒对肝癌根治性切除术后的病人有一定的预防复发转移作用。 (二)肝移植术 1.肝癌肝移植适应证: 肝移植是肝癌根治性治疗手段之一,尤其适用于有失代偿肝硬化背景、不适合切除的小肝癌病人。合适的适应证是提高肝癌肝移植疗效,保证宝贵的供肝资源得到公平合理应用的关键。 关于肝移植适应证,国际上主要采用米兰(Milan)标准,美国加州大学旧金山分校(UCSF)标准等。国内尚无统一标准,已有多家单位和学者陆续提出了不同的标准,包括杭州标准71、上海复旦标准72、华西标准73和三亚共识74等。各家标准对于无大血管侵犯、淋巴结转移及肝外转移的要求都比较一致,但是对于肿瘤的大小和数目的要求不尽相同。上述国内标准均不同程度的扩大了肝癌肝移植的适用范围,可使更多的肝癌病人因肝移植手术受益,并未明显降低术后总体生存率和无瘤生存率。但仍需多中心协作研究以支持和证明,从而获得高级别的循证医学证据。经专家组充分讨论,现阶段本规范推荐采用UCSF标准。 2.肝癌肝移植术后复发的预防: 肝癌肝移植术后的肿瘤复发明显减低了移植后生存率。其危险因素包括肿瘤分期、血管侵犯、AFP水平、免疫抑制剂累积用药剂量量等。减少移植后早期钙调磷酸酶抑制剂的用量可能降低肿瘤复发率75(证据等级2)。肝癌肝移植采用mTOR抑制剂的免疫抑制方案亦可能预防肿瘤复发,提高生存率76,77(证据等级2),但尚需多中心随机临床研究的进一步证实。 (三)局部消融治疗 尽管外科手术是肝癌的首选治疗方法,但因肝癌病人大多合并有肝硬化,或者在确诊时大部分病人已达中晚期,能获得手术切除机会的病人约20%-30%。近年来广泛应用的局部消融治疗,具有创伤小、疗效确切的特点,使一些不耐受手术切除的肝癌病人亦可获得根治的机会。 局部消融治疗是借助医学影像技术的引导对肿瘤靶向定位,局部采用物理或化学的方法直接杀灭肿瘤组织的一类治疗手段。主要包括射频消融(Radiofrequency ablation,RFA)、微波消融(Microwave ablation,MWA)、冷冻治疗、高功率超声聚焦消融(High power focused ultrasound ablation,HIFU)以及无水乙醇注射治疗(Percutaneous ethanol injection,PEI)等。局部消融最常用超声引导,具有方便、实时、高效的特点。CT及MRI结合多模态影像系统可用于观察超声无法探及的病灶。CT及MRI引导技术还可应用于肺、肾上腺、骨等转移灶的消融等。 消融的路径有经皮、腹腔镜、或开腹三种方式。大多数的小肝癌可以经皮穿刺消融,具有经济、方便、微创的特点。位于肝包膜下的肝癌,特别是突出肝包膜外的肝癌,经皮穿刺消融风险较大,或者影像学引导困难的肝癌,可考虑经开腹消融和经腹腔镜消融的方法。 局部消融治疗适用于单个肿瘤直径≤5cm;或肿瘤结节不超过3个、最大肿瘤直径≤3cm;无血管、胆管和邻近器官侵犯以及远处转移78-80(证据等级1),肝功能分级为Child-Pugh A或B级的肝癌病人,可获得根治性的治疗效果。对于不能手术切除的直径3-7cm的单发肿瘤或多发肿瘤,可联合TACE81,82(证据等级1)。 1.常见消融手段包括: (1)RFA:是肝癌微创治疗的最具代表性消融方式,其优点是操作方便,住院时间短,疗效确切,花费相对较低,特别适用于高龄病人。对于直径≤3cm肝癌病人,RFA的无瘤生存率略逊于手术切除43,78(证据等级1)。与PEI相比,RFA具有根治率高、所需治疗次数少和远期生存率高的显著优势。RFA治疗的精髓是对肿瘤整体灭活并尽量减少正常肝组织损伤,其前提是对肿瘤浸润范围和卫星灶的确认。因此,十分强调治疗前精确的影像学检查。超声造影技术有助于确认肿瘤的实际大小和形态,界定肿瘤浸润范围,检出微小肝癌和卫星灶,为制定消融方案灭活肿瘤提供了可靠的参考依据。 (2)MWA:是我国常用的热消融方法,在局部疗效、并发症发生率以及远期生存方面与RFA相比都无显著差异。其特点是消融效率高,避免RFA所存在的“热沉效应”。现在的MWA技术也能一次性灭活肿瘤,血供丰富的肿瘤,可先凝固阻断肿瘤主要滋养血管,再灭活肿瘤,可以提高疗效。建立温度监控系统可以调控有效热场范围,保证凝固效果。随机对照研究显示,两者之间无论是在局部疗效和并发症方面,还是生存率方面都无统计学差异85(证据等级1),MWA和RFA,这两种消融方式的选择可根据肿瘤的大小、位置,选择更适宜的消融方式83(证据等级3)。 (3)PEI:适用于直径≤3cm以内肝癌的治疗,局部复发率高于RFA,但PEI对直径≤2cm的肝癌消融效果确切,远期疗效类似于RFA。PEI的优点是安全,特别适用于癌灶贴近肝门、胆囊及胃肠道组织,而热消融治疗(RFA和MWA)可能容易造成损伤的情况下。 2.基本技术要求需要注意以下方面: (1)操作医师必须经过严格培训和足够的实践积累,治疗前应该全面而充分地评估病人的全身状况,肝功能状态,肿瘤的大小、位置、数目等。要注意肿瘤与邻近器官的关系,制定合理的穿刺路径及消融范围,在保证安全的前提下,达到足够的安全范围。 (2)根据肿瘤的大小、位置,强调选择适合的影像引导技术(超声或CT)和消融手段(RFA、MWA或PEI)。 (3)肿瘤距肝门部肝总管、左右肝管的距离应至少为5mm。不推荐对>5cm的病灶单纯施行消融治疗。对于多个病灶或更大的肿瘤,根据病人肝功能状况,采取治疗前TACE+消融联合治疗,效果优于单纯的消融治疗。 (4)消融范围应力求包括5mm的癌旁组织,以获得“安全边缘”,彻底杀灭肿瘤。对于边界不清晰、形状不规则的浸润型癌或转移癌灶,在邻近肝组织及结构条件许可的情况下,建议适当扩大消融范围。 3.对于直径≤5cm的肝癌治疗选择: 数项临床前瞻性随机对照和系统回顾性分析显示,手术切除宜首选42-44,78(证据等级1)。在临床实践中,应该根据病人的一般状况和肝功能,肿瘤的大小、数目、位置决定,以及从事消融治疗的医师的技术和经验,全面考虑后选择合适的初始治疗手段。通常认为,如果病人能够耐受肝切除术,以及肝癌位置表浅或位于肝脏边缘,应首选手术切除。局部消融可作为手术切除之外的另一种治疗选择。对于2-3个癌灶位于不同区域、或者位居肝脏深部或中央型≤5cm的肝癌,局部消融可以达到手术切除疗效,获得微创下根治性消融。 4.肝癌消融治疗后应重视的评估和随访: 评估局部疗效的规范方法是在消融后1个月左右,复查肝脏动态增强CT或MRI,或者超声造影,以评价消融效果。消融效果可分为:①完全消融(Complete response,CR):经动态增强CT或MRI扫描,或者超声造影随访,肿瘤所在区域为低密度(超声表现为高回声),动脉期未见强化;②不完全消融(In-complete response,ICR):经动态增强CT或MRI扫描,或者超声造影随访,肿瘤病灶内局部动脉期有强化,提示有肿瘤残留。对治疗后有肿瘤残留者,可以进行再次消融治疗;若2次消融后仍有肿瘤残留,视为消融治疗失败,应放弃消融疗法,改用其他疗法。完全消融后应定期随访复查,通常情况下每隔2~3月复查肿瘤标志物、彩超、MRI或CT,以便及时发现可能的局部复发病灶和肝内新发病灶,利用经皮消融微创安全和简便易于反复施行的优点,有效地控制肿瘤进展。 (四)TACE治疗 TACE治疗在国内亦称介入疗法、介入治疗Interventionaltreatment),目前被公认为肝癌非手术治疗的最常用方法之一84-89(证据等级1)。 1.基本原则: (1)要求在数字减影血管造影机下进行;(2)必须严格掌握临床适应证;(3)必须强调超选择插管至肿瘤的供养血管内治疗;(4)必须强调保护病人的肝功能;(5)必须强调治疗的规范化和个体化;(6)如经过4-5次TACE治疗后,肿瘤仍继续进展,应考虑换用或联合其它治疗方法,如外科手术、局部消融和系统治疗以及放疗等。 2.适应证: (1)IIb期、IIIa期和IIIb期的部分病人,肝功能分级Child-PughA或B级,ECOG评分0-2;(2)可以手术切除,但由于其他原因(如高龄、严重肝硬化等)不能或不愿接受手术的Ib期和IIa期病人;(3)多发结节型肝癌;(4)门静脉主干未完全阻塞,或虽完全阻塞但肝动脉与门静脉间代偿性侧支血管形成;(5)肝肿瘤破裂出血或肝动脉-门脉静分流造成门静脉高压出血;(6)控制局部疼痛、出血以及栓堵动静脉瘘;(7)肝癌切除术后,DSA造影可以早期发现残癌或复发灶,并给予介入治疗。 3.禁忌证: (1)肝功能严重障碍(Child-Pugh C级),包括黄疸、肝性脑病、难治性腹水或肝肾综合征;(2)凝血功能严重减退,且无法纠正;(3)门静脉主干完全被癌栓栓塞,且侧支血管形成少;(4)合并活动性肝炎或严重感染且不能同时治疗者;(5)肿瘤远处广泛转移,估计生存期<3个月者;(6)恶液质或多器官功能衰竭者;(7)肿瘤占全肝比例≥70%癌灶(如果肝功能基本正常,可考虑采用少量碘油乳剂分次栓塞);(8)外周血白细胞和血小板显著减少,白细胞<3.0×109/L(非绝对禁忌,如脾功能亢进者,与化疗性白细胞减少有所不同),血小板<50×109/L;(9)肾功能障碍:肌酐>2mg/dl或者肌酐清除率<30ml/min。 4.操作程序要点和分类90(证据等级3): (1)肝动脉造影,通常采用Seldinger方法,经皮穿刺股动脉插管,导管置于腹腔干或肝总动脉行DSA造影,造影图像采集应包括动脉期、实质期及静脉期;应做肠系膜上动脉造影、注意寻找侧枝供血。仔细分析造影表现,明确肿瘤的部位、大小、数目以及供血动脉。 (2)根据肝动脉插管化疗、栓塞操作的不同,通常分为:①肝动脉灌注化疗:经肿瘤供血动脉灌注化疗,常用化疗药物有蒽环类、铂类等。②肝动脉栓塞:单纯用栓塞剂堵塞肝肿瘤的供血动脉。③肝动脉化疗栓塞:把化疗药物与栓塞剂混合在一起,经肿瘤的供血动脉支注入。TACE治疗最常用的栓塞剂就是碘油乳剂、标准化明胶海绵颗粒,还有药物洗脱微球。先灌注一部分化疗药物,一般灌注时间不应<20 min。然后将另一部分化疗药物与碘油混合成乳剂进行栓塞。碘油用量一般为5-20 ml,不超过30 ml。在透视监视下依据肿瘤区碘油沉积是否浓密、瘤周是否已出现门静脉小分支影为界限。在碘油乳剂栓塞后加用颗粒性栓塞剂(如:标准化明胶海绵颗粒、微球、聚乙烯醇颗粒等)。提倡使用超液化乙碘油与化疗药物充分混合成乳剂,尽量避免栓塞剂返流栓塞正常肝组织或进入非靶器官。栓塞时应尽量栓塞肿瘤的所有供养血管,以尽量使肿瘤去血管化。 5.TACE术后常见不良反应: 栓塞后综合症,是TACE治疗的最常见不良反应,主要表现为发热、疼痛、恶心和呕吐等。发热、疼痛的发生原因是肝动脉被栓塞后引起局部组织缺血、坏死,而恶心、呕吐主要与化疗药物有关。此外,还有穿刺部位出血、白细胞下降、一过性肝功能异常、肾功能损害以及排尿困难等其他常见不良反应。介入治疗术后的不良反应会持续5-7天,经对症治疗后大多数病人可以完全恢复。 6疗效评价: 根据实体瘤mRECIST评价标准以及EASL评价标准评估肝癌疗效,长期疗效指标为病人总生存时间(Overall survival,OS);短期疗效:评价指标为肿瘤的影像学应答和手术至疾病进展时间(Time to progress,TTP)。 7.影响TACE远期疗效的主要因素包括84: (1)肝硬化程度、肝功能状态;(2)血清AFP水平;(3)肿瘤的容积和负荷量;(4)肿瘤包膜是否完整;(5)门静脉有无癌栓;(6)肿瘤血供情况;(7)肿瘤的病理分型。 8.随访及TACE间隔期间治疗: 一般建议第一次TACE治疗后3-6周时复查CT和/或MRI、肿瘤相关标志物、肝肾功能和血常规检查等;若影像学检查显示肝脏的瘤灶内的碘油沉积浓密、瘤组织坏死并且无增大和无新病灶,暂时不做TACE治疗。至于后续TACE治疗的频率应依随访结果而定,主要包括病人对上一次治疗的反应、肝功能和体能状况的变化。随访时间可间隔1-3个月或更长时间,依据CT和/或MRI动态增强扫描评价肝脏肿瘤的存活情况,以决定是否需要再次进行TACE治疗。目前主张综合TACE治疗,即TACE联合其它治疗方法,目的是控制肿瘤、提高病人生活质量和让病人带瘤长期生存。 9.TACE治疗时注意点: (1)提倡用微导管超选择性插管。插入肿瘤的供血动脉支,精准地注入碘油乳剂和颗粒性栓塞剂,提高疗效和保护肝功能。 (2)可使用门静脉内支架置放术和碘-125粒子条或碘-125粒子门静脉支架置放术,有效处理门静脉主干癌栓91(证据等级2)。 (3)TACE联合消融治疗:目前有两种TACE联合热消融治疗方式。①序贯消融:先行TACE治疗,术后1-4周内加用射频或微波消融。②同步消融:在TACE治疗时,同时给予射频或微波消融,可以明显提高临床疗效,并减轻肝功能损伤92(证据等级2)。 (4)颗粒性栓塞剂的应用:包括标准化明胶海绵颗粒、聚乙烯醇颗粒、微球、药物洗脱微球等。常规TACE常使用标准化明胶海绵微粒与碘油联合。药物性洗脱微球(Drug-eluting beads,DEB)是一种新的栓塞剂,可携带化疗药物。文献报道DEB在肿瘤客观有效率及总获益率方面具有优势。但是,近期文献报道结果显示两种方法治疗肝癌的疗效无显著性差异。 (5)重视局部加局部治疗和局部联合全身治疗84:①TACE联合消融(RFA、MWA等)治疗91(证据等级2);②TACE联合放射治疗91(证据等级2):主要指门静脉主干癌栓、下腔静脉癌栓和局限性大肝癌介入治疗后的治疗;③TACE联合II期外科手术切除:大肝癌或巨块型肝癌在TACE治疗后缩小并获得手术机会时,推荐外科手术切除91(证据等级3);④TACE联合全身治疗:包括联合分子靶向药物三氧化二砷、放射免疫靶向药物、基因治疗、免疫治疗及全身化疗等。 (五)放射治疗 放射治疗(简称放疗)分为外放疗和内放疗。外放疗是利用放疗设备产生的射线(光子或粒子)从体外对肿瘤照射。内放疗是利用放射性核素,经机体管道或通过针道植入肿瘤内。 1.外放射治疗: (1)适应证: 对伴有门静脉/下腔静脉癌栓或肝外转移的IIIa期、IIIb期肝癌病人,多属于姑息性放疗,有一部分病人肿瘤缩小或降期,可获得手术切除机会93-95(证据等级3)。肝外转移包括淋巴结转移、肺转移、骨转移、肾上腺转移、脑转移、腹膜和胸腔内膜转移等,也可用于等待肝癌肝移植前的治疗。对肝外转移的病人,外放疗可减轻疼痛、梗阻或出血等症状,使肿瘤发展减缓,从而延长生存期96-98(证据等级3)。中央型肝癌切缘距肿瘤≤1cm的窄切缘术后可以辅助放疗99(证据等级3)。 (2)照射靶区: 大体肿瘤体积(GrossTumor Volume,GTV)在增强CT中定义,必要时也需要参考MRI影像。肝癌出现淋巴引流区转移较少见,因此,临床靶体积(Clinical Target Volume,CTV)不包括淋巴引流区。对于已经出现淋巴结转移的病人,必须包括其下一站的淋巴引流区,作为CTV。其余情况(如局限于肝内、癌栓、肾上腺、肺转移等)的CTV为影像学可见的病灶外扩2到4 mm100。肿瘤移动度可以通过透视评估,但4D模拟CT技术更为准确。在常规放疗技术情况下,计划靶体积(Planning Target Volume,PTV)一般在CTV基础上外放5-15 mm。 肝内靶区的勾划必须有动脉相、静脉相互相参考;MRI对肝内病灶较清楚,PET/CT可以了解肝外病灶情况,靶区的确定尽量多种影像学资料互相参考。肝癌放疗野设计的一个重要原则是充分利用正常肝组织所具有的强大再生能力,在设计放射野时,尤其是大肝癌,最好能保留一部分正常肝组织不受照射,从而使部分正常肝组织能得到再生。 (3)照射剂量和正常组织耐受剂量: 立体定向放疗时,肝功能为Child-PughA级,正常肝体积超过700 ml,<15 Gy×3次,正常肝>800 ml,<18 Gy×3次是安全剂量;一般推荐放疗剂量≥30-60 Gy/3-6次101。对姑息性放疗的肝癌病人,肿瘤的放疗剂量基本上取决于全肝和/或周围胃肠道的耐受量,大部分的报道以40-70Gy常规分割剂量。 正常组织耐受剂量:肝功能为Child-PughA者,常规分割放疗时,全肝的耐受量为28-30 Gy102,或非常规低分割放疗(每次分割剂量4-8 Gy)全肝的耐受量为23 Gy103。肝功能为Child-Pugh B者,肝脏对射线的耐受量明显下降。由于亚洲HCC病人常伴有肝硬化和脾功能亢进,导致胃肠道瘀血和凝血功能差,胃肠道的放射耐受剂量低于RTOG推荐的剂量104。 (4)放疗技术: 建议应用三维适形放疗(3-DConformal radiotherapy,CRT))、调强放疗(Intensity modulated radiationtherapy,IMRT)、图像引导放疗(Image guided radiation therapy,IGRT)或立体定向放疗(Stereotactic body radiationtherapy,SBRT)。图像引导下的调强放射治疗技术优于三维适形放疗105,螺旋断层放疗设备作为图像引导下的调强放疗,适合多发病灶的肝癌病人。肝癌的立体定向放射治疗必须满足以下条件:有四维CT的影像设备引导或肿瘤追踪系统,非常精确的病人体位固定,放射治疗前的个体化图像校正,放射治疗设备能聚焦到肿瘤以及肿瘤之外的射线梯度下降快。目前缺乏较高级别的临床资料支持质子放疗在肝癌病人的生存率优于光子。 呼吸运动是导致肝脏肿瘤在放疗过程中运动和形变的主要原因。目前可采取多种技术以减少呼吸运动带来的影响,如门控技术、实时追踪技术和呼吸控制技术,根据四维CT确定内靶区(Internal target volume,ITV)等等。腹部加压简单易行,减少肝脏的呼吸动度,压腹部位在剑突与脐连线上半部,可最大程度减小肝脏呼吸动度106。 2.内放射治疗: 放射性粒子植入是局部治疗肝癌的一种有效方法,包括90Y微球疗法107、131I单克隆抗体108、放射性碘化油109、125I粒子植入等,放射性粒子可持续产生低能X射线、γ射线或β射线,在肿瘤组织内或在受肿瘤侵犯的管腔(门静脉、下腔静脉或胆道)内植入放射性粒子后,通过持续低剂量辐射,最大程度杀伤肿瘤细胞。粒子植入技术包括组织间植入、门静脉植入、下腔静脉植入和胆道内植入,分别治疗肝内病灶、门静脉癌栓、下腔静脉癌栓和胆管内癌或癌栓。 (六)全身治疗 对于没有禁忌证的晚期肝癌病人,全身治疗可以减轻肿瘤负荷,改善肿瘤相关症状,提高生活质量,延长生存时间。 1.抗肿瘤治疗及其疗效评价 (1)分子靶向药物: 迄今为止,索拉非尼仍然是唯一获得批准治疗晚期肝癌的分子靶向药物。两项大型国际多中心III期临床试验均充分证明了索拉非尼对于不同国家地区、不同肝病背景的晚期肝癌都具有一定的生存获益110(证据等级1)。常规推荐用法为400mg,po.,bid,应用时需注意对肝功能的影响。最常见的不良反应为腹泻、体重下降、手足综合征、皮疹、心肌缺血以及高血压等(证据等级1),一般发生在治疗开始后的2-6周内,可用于肝功能Child A、B级的病人(证据等级1)。而相对于肝功能Child B级,ChildA级的病人生存获益更明显111。 (2)系统化疗: 传统的细胞毒性药物,包括阿霉素、表阿霉素、氟尿嘧啶、顺铂和丝裂霉素等,在肝癌中的单药或传统联合用药有效率均不高,且毒副作用大,可重复性差。一个主要原因为化疗药物不但会激活乙肝病毒复制,还会损害病人的肝功能,加重肝炎肝硬化,导致化疗无法带来生存效益。 根据EACH研究后期随访的数据,含奥沙利铂的FOLFOX4方案在整体反应率、疾病控制率、无进展生存期、总生存期方面,均优于传统化疗药物阿霉素,且耐受性和安全性较好112(证据等级2)。因此,奥沙利铂在我国被批准用于治疗不适合手术切除或局部治疗的局部晚期和转移性肝癌。 化疗适应证主要为:①合并有肝外转移的晚期病人;②虽为局部病变,但不适合手术治疗和TACE者,如肝脏弥漫性病变或肝血管变异;③合并门静脉主干或下腔静脉瘤栓者;④多次TACE后肝血管阻塞和/或TACE治疗后复发的病人。 化疗禁忌证为:①ECOG PS评分>2,Child-Pugh评分>7分;②白细胞计数<3.0 X 109/L或中性粒细胞计数<l.5×109/L,血小板计数<60×109/L,血红蛋白<90g/L;③肝、肾功能明显异常,氨基转移酶(AST或ALT)>5倍正常值和/或胆红素显著升高>2倍正常值,血清白蛋白<28g/L,肌酐(Cr)≥正常值上限,肌酐清除率(CCr)<50ml/min;④具有感染发热、出血倾向、中-大量腹腔积液和肝性脑病。 其他药物:三氧化二砷治疗中晚期原发性肝癌具有一定的姑息治疗作用113(证据等级3)。在临床应用时,应注意监测肝肾毒性。 (3)免疫治疗: 肝癌免疫治疗主要包括免疫调节剂(干扰素α、胸腺肽α1(胸腺法新)等)65,114、免疫检查点阻断剂(CTLA-4阻断剂、PD-1/PD-L1阻断剂等)、肿瘤疫苗(树突细胞疫苗等)、细胞免疫治疗(细胞因子诱导的杀伤细胞,即CIK)113,115。这些治疗手段均有一定的抗肿瘤作用,但尚待大规模的临床研究加以验证。 (4)中医药: 中医中药治疗能够改善症状,提高机体的抵抗力,减轻放化疗不良反应,提高生活质量。除了采用传统的辨证论治、服用汤剂之外,我国药监部门业已批准了若干种现代中药制剂如槐耳颗粒、康莱特、华蟾素、榄香烯、肝复乐等用于治疗肝癌116,117,具有一定的疗效,病人的依从性、安全性和耐受性均较好(证据等级4)。但是,这些药物尚缺乏高级别的循证医学证据加以充分支持。 (5)全身治疗的疗效评估: 对于化疗病人,仍然采用Recist 1.1标准,可同时参考血清学肿瘤标记(AFP)以及肿瘤坏死程度的变化,一般在治疗期间每6-8周进行影像学评估,同时通过动态观察病人的症状、体征、治疗相关不良反应进行综合评估。鉴于索拉非尼、TACE治疗很少能改变肿瘤大小,故建议采用以肿瘤血管生成和密度改变为基础的疗效评估标准(mRecist标准)118,119。对于免疫治疗的评价,可参照irRC(immune-relatedresponse criteria)标准120,121。 2.抗病毒治疗及其他保肝治疗: 合并有乙肝病毒感染且复制活跃的肝癌病人,口服核苷(酸)类似物抗病毒治疗非常重要。宜选择强效低耐药的药物如恩替卡韦、替比夫定或替诺福韦脂等。TACE治疗可能引起乙型肝炎病毒复制活跃,目前推荐在治疗前即开始应用抗病毒药物。抗病毒治疗还可以降低术后复发率69,70(证据等级1)。因此,抗病毒治疗应贯穿肝癌治疗的全过程。 肝癌病人在自然病程中或者治疗过程中可能会伴随肝功能异常,因此应及时适当的应用保肝药物,如异甘草酸镁注射液(甘草酸二铵肠溶胶囊)、复方甘草酸苷、还原型谷胱甘肽、多磷脂酰胆碱等;抗炎治疗药物如广谱水解酶抑制剂乌司他丁等;利胆类药物如腺苷蛋氨酸、熊去氧胆酸等。这些药物可以保护肝功能、提高治疗安全性、降低并发症、改善生活质量。 3.对症支持治疗: 适度的康复运动可以增强机体的免疫功能。另外,应加强对症支持治疗,包括在晚期肝癌病人中的积极镇痛、纠正贫血、纠正低白蛋白血症、加强营养支持,控制合并糖尿病病人的血糖,处理腹水、黄疸、肝性脑病、消化道出血等伴随症状。 对于晚期肝癌病人,应理解病人者及家属的心态,采取积极的措施调整其相应的状态,把消极心理转化为积极心理,通过舒缓疗护让其享有安全感、舒适感而减少抑郁与焦虑。 五、附录: 附录一:证据等级(牛津循证医学中心2011版) (临床)问题 步骤1 步骤2 步骤3 步骤4 步骤5 (等级1*) (等级2*) (等级3*) (等级4*) (等级5*) 这个疾病有多普遍?(患病率) 当地的,当前的随机样本调查(或普查) 与当地情况相匹配调查的系统综述** 当地的,非随机样本调查** 病例系列** N/A 诊断或监测试验是否准确(诊断) 一致地应用了参考标准和盲法的横断面研究的系统综述 一致地应用了参考标准和盲法的横断面研究 非连续病例研究,或研究未能一致地应用参考标准** 病例对照研究,或应用了差的或非独立的参考标准** 基于机制的推理 若不加这个治疗会发生什么?(预后) 起始队列研究的系统综述 起始队列研究 队列研究或随机研究的对照组** 病例系列或病例对照研究,或低质量预后队列研究** N/A 这个治疗有用吗?(治疗效益) 随机试验或单病例随机对照试验的系统综述 随机试验或具有巨大效果的观察性研究 非随机对照队列/随访研究** 病例系列,病例对照研究,或历史对照研究** 基于机制的推理 这个治疗常见的伤害是什么(治疗伤害) 随机试验的系统综述,巢式病例对照研究的系统综述,针对你所提临床问题病人的n-of-1试验,具有巨大效果的观察性研究 单个随机试验或(特殊地)具有巨大效果的观察性研究 非随机对照队列/随访研究(上市后监测)提供,足够数量来排除常见的伤害(对长期伤害需要足够长的随访时间)** 病例系列,病例对照研究,或历史对照研究** 基于机制的推理 这个治疗少见的伤害是什么?(治疗伤害) 随机试验或N-of-1试验的系统综述 随机试验或(特殊地)具有巨大效果的观察性研究 这个试验(早期发现)值得吗?(筛查) 随机研究的系统综述 随机试验 非随机对照队列/随访研究** 病例系列,病例对照研究,或历史对照研究** 基于机制的推理 *根据研究质量,精确度,间接性,各个研究间不一致,或绝对效应值小,证据等级会被调低;若效应值很大,等级会被上调 **系统综述普遍地优于单个研究 附录二:原发性肝癌及相关病变的诊断名词(参照2010版WHO 肝细胞癌癌前病变 大细胞改变;小细胞改变;低度异型增生结节;高度异型增生结节; 异型增生灶;肝细胞腺瘤b 肝细胞癌 特殊亚型 硬化型;淋巴上皮瘤样型;富脂型;肉瘤样型;未分化型 肝细胞癌,纤维板层型 肝内胆管癌癌前病变 胆管上皮内瘤变(低级别和高级别BilIN);胆管内乳头状肿瘤; 胆管黏液性囊性肿瘤 肝内胆管癌 腺癌;肉瘤样癌 混合型肝细胞癌-胆管癌 双表型肝细胞癌 肝母细胞瘤 癌肉瘤 b:WH0将肝细胞腺瘤分为HNFlα失活型、β-catenin活化型、炎症型和未分类型等4种亚型,其中瘤体较大且伴β-catenin活化型肝细胞腺瘤的恶变风险可能会明显增加。 附录三:原发性肝癌的组织学分级 肝细胞癌Edmondson-Steiner分级: Ⅰ级:分化良好,核/质比接近正常,瘤细胞体积小,排列成细梁状。 Ⅱ级:细胞体积和核/质比较Ⅰ级增大,核染色加深,有异型性改变,胞浆呈嗜酸性颗粒状,可有假腺样结构。 Ⅲ级:分化较差,细胞体积和核/质比较Ⅱ级增大,细胞异型性明显,核染色深,核分裂多见。 Ⅳ级:分化最差,胞质少,核深染,细胞形状极不规则,黏附性差,排列松散,无梁状结构。 附录四:肝癌诊断路线图 典型表现:指增强动脉期(主要动脉晚期)病灶明显强化,门脉或延迟期强化下降,呈“快进快出”强化方式。 不典型表现:缺乏动脉期病灶强化或者门脉和延迟期强化没有下降或不明显,甚至强化稍有增加等。 动态MRI:指磁共振动态增强扫描。 动态增强CT:指动态增强三期或四期扫描。 CEUS:指使用超声对比剂实时观察正常组织和病变组织的血流灌注情况。 EOB-MRI:指Gd-EOB-DTPA增强磁共振扫描。 AFP(+):超过血清AFP检测正常值。 附录五:肝癌临床分期及治疗路线图 附录六:《原发性肝癌诊疗规范(2017年版)》编写专家委员会 名誉主任委员:吴孟超汤钊猷刘允怡陈孝平王学浩孙燕郑树森 主任委员:樊嘉 副主任委员:秦叔逵沈锋李强董家鸿周俭王伟林蔡建强滕皋军 外科学组组长:周俭;副组长:杨甲梅别平刘连新文天夫 介入治疗学组组长:王建华;副组长:韩国宏王茂强刘瑞宝陆骊工 内科及局部治疗组组长:秦叔逵;副组长:任正刚陈敏山曾昭冲梁萍 影像学组组长:曾蒙苏;副组长:梁长虹陈敏严福华王文平 病理学组组长:丛文铭;副组长:纪元 委员(按姓氏拼音排序): 成文武戴朝六荚卫东李亚明李晔雄梁军刘天舒吕国悦毛一雷任伟新石洪成孙惠川王文涛王晓颖邢宝才徐建明杨建勇杨业发 叶胜龙尹震宇张博恒张水军周伟平朱继业 秘书长:孙惠川王征 秘书:刘嵘史颖弘肖永胜代智 参考文献(略)
 杨晴 主任医师 珠海市人民医院医疗集团 肝病科1306人已读
杨晴 主任医师 珠海市人民医院医疗集团 肝病科1306人已读 - 精选 胆红素及胆红素升高的原因
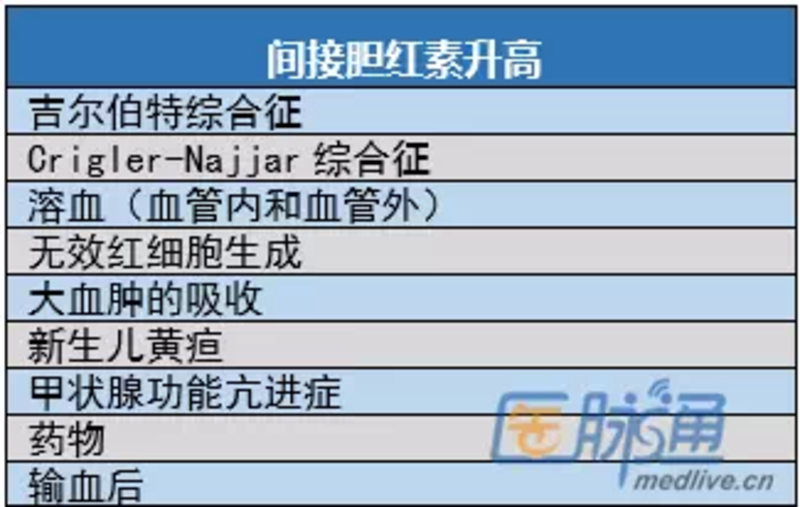
胆红素是临床上最常见的异常肝生化指标之一,是判定黄疸的重要依据,也是肝功能的重要指标。 胆红素的代谢 胆红素是血红素的终末产物,约80%来自红细胞,20%由其他含血红素的蛋白如肌红蛋白、细胞色素P450转换而来。在肝、脾和骨髓的单核吞噬细胞中,微粒体的血红素氧化酶将血红素转换为游离胆红素。这些游离胆红素是脂溶性的,在血浆中以白蛋白为载体输送入肝。由于其结合很稳定,并且难溶于水,因此不能由肾脏排出。胆红素定性试验呈间接阳性反应,称这种未结合胆红素为间接胆红素(IBil)。 未结合胆红素随血液运输到肝脏,在肝细胞内与葡萄糖醛酸结合转化为结合胆红素,这种胆红素的特点是水溶性大,能从肾脏排出,胆红素定性试验呈直接阳性反应,称这种胆红素为直接胆红素(DBil)。结合胆红素经胆道随胆汁排入肠内,在肠道内被葡糖醛酸酶还原为尿(粪)胆原,由尿(粪)排出。 总胆红素是间接胆红素与直接胆红素之和。 胆红素升高的原因 胆红素代谢障碍可能会导致血液胆红素浓度升高,产生高胆红素血症,进而出现黄疸。胆红素升高的评估,首先,应确定是直接胆红素还是间接胆红素升高。胆红素升高的原因如下: 间接胆红素(IBil)升高 间接胆红素升高是由于胆红素的产生过度(例如溶血)、肝重吸收减少或肝结合能力下降所致。间接胆红素升高最常见的原因是吉尔伯特综合征(肝功能不良、遗传性非溶血性高胆红素血症)。但其总胆红素水平几乎不超过6mg/dl,通常<3 mg/dl。空腹或严重疾病可使间接胆红素升高2~3倍,相反,进食或服用苯巴比妥药物可降低间接胆红素水平。 直接胆红素(DBil)升高 与间接型高胆红素血症相反,直接型高胆红素血症通常意味着肝实质损伤或胆汁淤积导致胆红素进入胆管,以及胆红素从肝细胞进入血液循环减少。严重肝损伤(包括酒精性肝炎肝硬化)患者的血清间接胆红素水平可能超过30 mg/dl,或可见于晚期肝硬化合并脓毒症或肾衰竭的患者中。此外,单纯高胆红素血症可见于手术后,通常可以恢复。
 杨晴 主任医师 珠海市人民医院医疗集团 肝病科6849人已读
杨晴 主任医师 珠海市人民医院医疗集团 肝病科6849人已读 - 精选 原发性胆汁性胆管炎的诊断和管理(2017EASL指南)
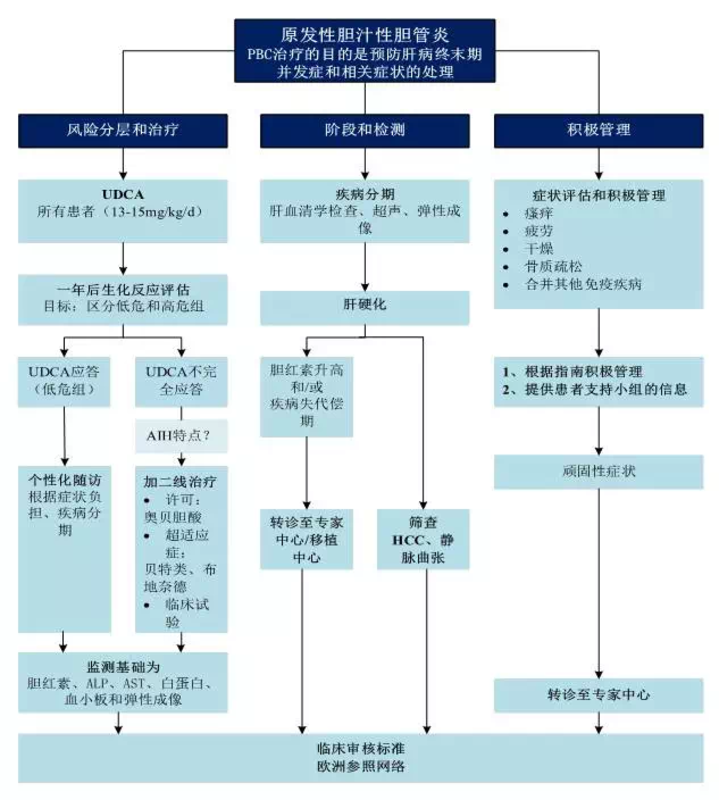
原发性胆汁性胆管炎是一种以胆汁淤积为特点的慢性自身免疫性肝病,如果不治疗将会发展为胆汁性肝硬化。通常根据胆汁淤积的表现及血清抗线粒体抗体阳性做出诊断。由于患者不同的临床表现及病程,为保证对患者个性化治疗,需进行风险分层。治疗的目的是减缓疾病进程、防止发展至终末阶段和改善症状。目前减缓疾病的进展的药物包括已许可的治疗方案(熊去氧胆酸和奥贝胆酸)和超适应症用药的治疗方案(苯氧酸类和布地奈德)。本临床实践指南总结了对PBC患者进行结构化、终生性和个性化治疗重要性的依据及方法(图1),帮助临床医生诊断和有效管理患者。 1对胆汁淤积的诊断方法 (1)EASL推荐在评估生化检验提示胆汁淤积性肝病的患者时,应采集详细的病史和对其进行身体检查(III,1)。 (2)EASL推荐超声作为一线非侵入性影像诊断方法,以区分肝内外胆汁淤积(III,1)。 (3)EASL推荐对所有病因不明的胆汁淤积症患者,通过免疫荧光筛查AMA和PBC特异性ANA(III,1)。 (4)EASL推荐对病因不明的胆汁淤积症可使用MRCP进行影像学检查。超声内镜(EUS)可以替代MRCP来评估远端胆道疾病(III,1)。 (5) EASL推荐在血清学筛查和进一步影像学检查后,对仍然病因不明的肝内胆汁淤积患者进行肝活检(III,1)。 (6)EASL推荐必要时对适合患者进行遗传性胆汁淤积综合征的基因检测(III,1)。 2PBC初始诊断 (7)EASL推荐排除全身性疾病的成年胆汁淤积患者,可以依据ALP升高和AMA滴度>1:40诊断PBC(III,1)。 (8)EASL推荐在正确情况下,特异性ANA免疫荧光(核点型和核周型)或ELISA结果(sp100,gp210)的胆汁淤积患者可以诊断为AMA阴性PBC(III,1)。 (9)EASL不推荐进行肝活检来诊断PBC,除非不存在PBC特异性抗体,或怀疑合并AIH或NASH以及其他(通常是全身性的)合并症(III,1)。 (10)单独AMA反应不足以诊断PBC。EASL推荐,对肝脏血清检查正常的AMA阳性患者进行随访,每年对肝脏疾病进行生化评估(III,1)。 3在实践中PBC的预后工具:指导 (11)PBC的治疗宗旨是预防肝脏末期并发症并治疗相关症状(III,1)。 (12)对所有患者进行发生进展期PBC的风险评估(III,1)。 (13) 发生PBC并发症的风险最大的患者是对治疗生化应答不充分和肝硬化的患者(II-2,1)。 (14)应认识到对治疗生化应答不充分的最严重危险因素是诊断年龄较小(例如,<45岁=和晚期阶段(III,1)。 (15)在基线时和随访期间使用非侵入性检测(胆红素、碱性磷酸酶、AST、白蛋白、血小板计数和弹性成像)来评估所有患者的疾病阶段(III,1)。 (16)血清胆红素和ALP升高可作为PBC患者结局的替代标志物,常规生物化学和血液学指标应巩固临床方法对个体疾病进展风险进行分层(II-2,1)。 (17)ALP<1.5 ULN、胆红素正常的早期PBC患者接受UDCA治疗一年后的无移植生存率与对照健康人群无显着差异(II-2,1)。 (18)使用弹性成像和风险评分(如GLOBE和UK-PBC评分)有助于更好地界定患者未来出现晚期肝病并发症的个体风险(III,1)。 4治疗:减缓疾病进展的治疗 (19)所有PBC患者应以口服UDCA 13-15 mg/kg·d作为一线药物治疗(I,1)。 (20)在一项III期研究中,ALP>1.67 ULN和/或胆红素升高<2 ULN的患者口服OCA的生化疗效证据已得到证实。口服OCA已经有条件地被批准联合UDCA用于对UDCA应答不佳的PBC患者,或单药用于无法耐受UDCA的PBC成人患者。EASL推荐了其在该类患者中的使用剂量(初始剂量5mg;根据6个月后的耐受性逐渐加量至10mg)(I,2)。 (21)尚未公布布地奈德(用于非肝硬化患者)、苯扎贝特以及两者联合UDCA的III期随机试验数据;EASL目前针对治疗方案未作出推荐(II-2,2)。 5特殊情况:妊娠 (22)所有怀孕患者进行专家咨询以指导治疗,值得注意的是非肝硬化PBC患者一般能够耐受妊娠,EASL建议在妊娠期间可继续使用UDCA。瘙痒管理很重要,可能需要专家意见,指出妊娠晚期已有专家使用利福平(III,1)。 (23)肝硬化患者妊娠期间发生母体和胎儿并发症的风险较高。 EASL推荐对患者进行孕前咨询和相关专家监测(III,1)。 6具有自身免疫性肝炎特点的PBC (24)约10%的PBC患者可能出现AIH的临床表现,大多数情况下同时存在,但有时甚至在PBC诊断后数年出现。 EASL推荐在确认AIH特征时必须进行肝活检,ALT和/或IgG不成比例升高患者也可考虑肝活检(III,1)。 (25)除了UDCA外,伴有PBC和AIH典型特征的患者可能受益于免疫抑制治疗。EASL推荐严重界面肝炎患者进行免疫抑制治疗,中度界面性肝炎患者可考虑。 EASL推荐询问并告知患者免疫抑制治疗的副作用(III,2)。 7症状与肝外表现的管理 (26)评估所有患者的症状,特别是瘙痒、干燥和疲劳。尽管终末期肝病与进行性症状负担相关,但症状的严重程度与PBC的疾病阶段不一定相关(III,1)。 (27)对瘙痒进行逐步治疗。EASL推荐将严重瘙痒症患者转诊到专家中心(III,1)。 (28)仅有具有局限性,但考虑到安全性仍推荐消胆安作为治疗瘙痒症的一线治疗,应注意避免与其它药物相互作用(II-2,1)。 (29)利福平作为瘙痒症的二线治疗药物,剂量为每天150 mg-300 mg。因为潜在的肝毒性,EASL推荐在初次使用后(药物开始后6和12周)和剂量增加后监测肝脏血清学检查,如果观察到肝毒性,应停药(II-2,1)。 (30)寻求和治疗疲劳、贫血、甲状腺功能减退和睡眠障碍相关和替代病因(III,1)。 (31)建议疲劳患者开发的应对策略,包括社会隔离障,但可复合疲劳效应(III,2)。 (32)干燥症状可显著降低患者的生活质量;可考虑转诊至专科临床医生(III,1)。 (33)无论疾病严重程度如何,具有耐药症状的患者应转诊进行专科治疗(III,1)。 8肝脏疾病并发症的管理 (34)注意所有PBC患者的骨质疏松症的风险(III,1)。 (35)作为评估骨质疏松症风险的一部分,考虑在初诊和随访时使用DEXA来评估骨密度(III,1)。 (36)根据当地情况,建议PBC患者补充钙和维生素D(III,2)。 (37)双膦酸盐用于PBC患者安全有效,但骨质疏松症骨折风险明显升高,EASL推荐静脉曲张患者慎用。 EASL建议按照特定的骨质疏松指南进行治疗(II-2,1)。 (38)PBC患者可能发生脂溶性维生素吸收不良,特别是长期黄疸的患者。应基于个体因素进行补充(III,2)。 (39)高脂血症是胆汁郁积的一个特征,没有实质证据支持PBC患者心血管疾病的风险升高。对PBC合并代谢综合征(高胆固醇、低HDL胆固醇和高LDL胆固醇)的亚组患者中,推荐在个案基础上采用降低胆固醇的药物治疗(III,2)。 (40)EASL推荐,Baveno-VI关于静脉曲张筛查和管理的指南同样适用于PBC患者(III,2)。 (41)EASL推荐针对疑似肝硬化患者,按照EASL指南进行HCC监测(III,2)。 (42)出现肝硬化并发症(例如胆红素值持续升高>50mmol/L或3mg/dl或MELD>15)或者药物难以控制的严重瘙痒的患者,考虑进行肝移植评估。(II-2,1)。 (43)针对肝移植后经证实复发或可能复发的PBC患者,UDCA的使用安全且可改善肝脏生物化学(II-2,2)。 (44)所有PBC患者都应该进行结构化的终身随访,认识到患者的疾病进展不同,可能需要不同程度的护理(III,1)。 (45)建议根据这些指导方针,为PBC建立护理方法(III,2)。 (46) 治疗PBC患者的临床医生应使用标准化的临床审核工具来对患者提供的质量进行培训和改善(III,2)。 (47) 应向患有PBC的患者通报患者支持小组提供的支持,包括获得患者教育材料(III,2)。 ----摘自2017年5月《临床肝胆病》
 杨晴 主任医师 珠海市人民医院医疗集团 肝病科1.6万人已读
杨晴 主任医师 珠海市人民医院医疗集团 肝病科1.6万人已读 - 精选 2015版中国慢性乙型肝炎防治指南
题目待定 《慢性乙型肝炎防治指南》(2015年版) 慢性乙型肝炎的预防、诊断和抗病毒治疗指南 中华医学会肝病学分会、中华医学会感染病分会 2015年10月22日 本指南为规范慢性乙型肝炎的预防、诊断和抗病毒治疗而制定,涉及慢性乙型肝炎其它治疗策略和方法请参阅相关的指南和共识。 中华医学会肝病学分会和感染病学分会于2005年组织国内有关专家制定《慢性乙型肝炎防治指南》(第一版), 并于2010年第一次修订。近5年来,国内外有关慢性乙型肝炎的基础和临床研究取得很大进展,为此我们对本指南进行再次修订。 本指南旨在帮助临床医生在慢性乙型肝炎诊断、预防和抗病毒治疗中做出合理决策,但不是强制性标准,也不可能包括或解决慢性乙型肝炎诊治中的所有问题。因此,临床医生在面对某一患者时,应在充分了解有关本病的最佳临床证据、认真考虑患者具体病情及其意愿的基础上,根据自己的专业知识、临床经验和可利用的医疗资源,制定全面合理的诊疗方案。我们将根据国内外的有关进展情况,继续对本指南进行不断更新和完善。 本指南中的证据等级分为A、B和C 三个级别,推荐等级分为1和2级别(表1,根据GRADE分级修订) 表1 推荐意见的证据等级和推荐等级 级别 详细说明 证据级别 A高质量 进一步研究不大可能改变对该疗效评估结果的信心 B中等质量 进一步研究有可能使我们对该疗效评估结果的信心产生重要影响 C低质量 进一步研究很有可能影响该疗效评估结果,且该评估结果很可能改变 推荐等级 1 强推荐 充分考虑到了证据的质量、患者可能的预后情况及治疗成本而最终得出 的推荐意见; 2 弱推荐 证据价值参差不齐,推荐意见存在不确定性,或推荐的治疗意见可能会有较高的成本疗效比等,更倾向于较低等级的推荐 一、术语 慢性HBV感染 (chronic HBV infection)—HBsAg和(或)HBV DNA阳性6个月以上。 慢性乙型肝炎 (chronic hepatitis B)—由乙型肝炎病毒持续感染引起的肝脏慢性炎症性疾病。可以分为HBeAg阳性慢性乙型肝炎和HBeAg阴性慢性乙型肝炎。 HBeAg阳性慢性乙型肝炎 (HBeAg positive chronic hepatitis B)—血清HBsAg阳性、HBeAg阳性、HBV DNA阳性,ALT持续或反复升高,或肝组织学检查有肝炎病变。 HBeAg阴性慢性乙型肝炎 (HBeAg negative chronic hepatitis B)—血清HBsAg阳性,HBeAg阴性,HBV DNA阳性,ALT持续或反复异常,或肝组织学检查有肝炎病变。 非活动性HBsAg携带者 (inactive HBsAg carrier)—血清HBsAg阳性,HBeAg阴性,HBV DNA低于检测下限,1年内连续随访3次以上,每次至少间隔3个月,ALT均在正常范围。肝组织学检查显示:组织学活动指数(HAI)评分< 4或根据其他的半定量计分系统判定病变轻微。 乙型肝炎康复 (resolved hepatitis B)—既往有急性或慢性乙型肝炎病史,HBsAg阴性,HBsAb阳性或阴性,抗-HBc阳性,HBV DNA低于最低检测限,ALT在正常范围。 慢性乙型肝炎急性发作 (acute exacerbation or flare of hepatitis)—ALT升至正常上限10倍以上。 乙型肝炎再活动 (reactivation of hepatitis B)—常常发生于非活动性HBsAg携带者或乙型肝炎康复者中,特别是在接受免疫抑制治疗或化疗时。在HBV DNA持续稳定的患者,HBV DNA升高≥2 log10 IU/mL,或者基线 HBV DNA 阴性者由阴性转为阳性且≥100 IU/mL,或者缺乏基线HBV DNA者HBV DNA≥20 000 IU/mL。往往伴有肝脏炎症坏死再次出现,ALT升高。 HBeAg阴转 (HBeAg clearance)—既往HBeAg阳性的患者HBeAg消失。 HBeAg血清学转换 (HBeAg seroconversion)—既往HBeAg阳性的患者HBeAg消失、抗-HBe出现。 HBeAg逆转 (HBeAg reversion)—既往HBeAg阴性、抗-HBe阳性的患者再次出现HBeAg。 组织学应答 (histological response)—肝脏组织学炎症坏死降低≥2分,没有纤维化评分的增高;或者以Metavir评分,纤维化评分降低≥1分。 完全应答 (Complete response) 持续病毒学应答且HBsAg阴转或伴有抗-HBs阳转。 临床治愈 (Clinical cure):持续病毒学应答且HBsAg阴转或伴有抗-HBs阳转、ALT正常、肝组织学轻微或无病变。 原发性无应答(Primary nonresponse)-核苷类药物治疗依从性良好的患者,治疗12周时HBV DNA较基线下降幅度<1 log10IU/mL或24周时HBV DNA较基线下降幅度<2 log10 IU/mL。 应答不佳或部分病毒学应答(suboptimal or partial virological response)-依从性良好的患者,治疗24周时HBV DNA较基线下降幅度>1 log10 IU/mL,但仍然可以检测到。 病毒学应答 (virological response)—治疗过程中,血清HBV DNA低于检测下限。 病毒学突破 (virological breakthrough)—核苷类药物治疗依从性良好的患者,在未更改治疗的情况下,HBV DNA水平比治疗中最低点上升1个log值,或一度转阴后又转为阳性,并在1个月后以相同试剂重复检测加以确定,可有或无ALT升高。 病毒学复发(Viral relapse)-获得病毒学应答的患者停药后,间隔1个月两次检测HBV DNA均大于2 000 IU/mL。 临床复发(Clinical relapse)-病毒学复发并且ALT>2 x ULN,但应排除其他因素引起的ALT增高。 持续病毒学应答(sustained off-treatment virological response)-停止治疗后血清HBV DNA持续低于检测下限。 耐药(Drug resistance)—在抗病毒治疗过程中,检测到和HBV耐药相关的基因突变,称为基因型耐药 (Genotypic resistance)。体外实验显示抗病毒药物敏感性降低、并和基因耐药相关,称为表型耐药 (Phenotypic resistance)。针对一种抗病毒药物出现的耐药突变对另外一种或几种抗病毒药物也出现耐药,称为交叉耐药 (Cross resistance)。至少对两种不同类别的核苷(酸)类似物耐药,称为多药耐药 (multidrug resistance)。 二、流行病学和预防 流行病学 HBV感染呈世界性流行,但不同地区HBV感染的流行强度差异很大。据世界卫生组织报道,全球约20亿人曾感染HBV,其中2.4亿人为慢性HBV感染者1,每年约有65万人死于HBV感染所致的肝衰竭、肝硬化和肝细胞癌 (HCC)2。全球肝硬化和HCC患者中,由HBV感染引起的比例分别为30%和45%2, 3。我国肝硬化和HCC患者中,由HBV感染引起的比例分别为60%和80%4。由于乙型肝炎疫苗免疫,急性HBV感染明显减少,以及感染HBV人口的老龄化,再加上抗病毒治疗的广泛应用,近年HBeAg阴性慢性乙型肝炎患者的所占比例上升5。 2006年全国乙型肝炎血清流行病学调查表明,我国1~59岁一般人群HBsAg携带率为7.18%6, 7。据此推算,我国现有慢性HBV感染者约9300万人,其中慢性乙型肝炎患者约2000万例8。 2014年全国1~29岁人群乙型肝炎血清流行病学调查结果显示,1~4岁、5~14岁和15~29岁人群HBsAg流行率分别为0.32%、0.94%和4.38%(中国CDC)。 HBV主要经血(如不安全注射等)、母婴及性接触传播9。由于对献血员实施严格的HBsAg和HBV DNA筛查,经输血或血液制品引起的HBV感染已较少发生;经破损的皮肤或黏膜传播主要是由于使用未经严格消毒的医疗器械和侵入性诊疗操作不安全注射特别是注射毒品等;其他如修足、文身、扎耳环孔、医务人员工作中的意外暴露、共用剃须刀和牙刷等也可传播10。母婴传播主要发生在围产期,多为在分娩时接触HBV阳性母亲的血液和体液传播,随着乙型肝炎疫苗联合乙型肝炎免疫球蛋白 (HBIG) 的应用,母婴传播已大为减少10。与HBV阳性者发生无防护的性接触,特别是有多个性伴侣者,其感染HBV的危险性增高。 HBV不经呼吸道和消化道传播,因此,日常学习、工作或生活接触,如同一办公室工作 (包括共用计算机等办公用品)、握手、拥抱、同住一宿舍、同一餐厅用餐和共用厕所等无血液暴露的接触,不会传染HBV。流行病学和实验研究未发现HBV能经吸血昆虫 (蚊、臭虫等) 传播9。 预防 (一)乙型肝炎疫苗预防 接种乙型肝炎疫苗是预防HBV感染的最有效方法。乙型肝炎疫苗的接种对象主要是新生儿11,其次为婴幼儿,15岁以下未免疫人群和高危人群(如医务人员、经常接触血液的人员、托幼机构工作人员、器官移植患者、经常接受输血或血液制品者、免疫功能低下者、HBsAg阳性者的家庭成员、男男同性、有多个性伴侣者和静脉内注射毒品者等)。 乙型肝炎疫苗全程需接种3针,按照0、1、6个月程序,即接种第1针疫苗后,间隔1个月及6个月注射第2及第3针疫苗。新生儿接种乙型肝炎疫苗要求在出生后24 h内接种,越早越好。接种部位新生儿为臀前部外侧肌肉内或上臂三角肌,儿童和成人为上臂三角肌中部肌内注射。 单用乙型肝炎疫苗阻断母婴传播的阻断率为87.8%12。对HBsAg阳性母亲的新生儿,应在出生后24 h内尽早(最好在出生后12 h)注射HBIG,剂量应≥100 IU,同时在不同部位接种10 μg重组酵母乙型肝炎疫苗,在1个月和6个月时分别接种第2和第3针乙型肝炎疫苗,可显著提高阻断母婴传播的效果13,14。新生儿在出生12 h内注射HBIG和乙型肝炎疫苗后,可接受HBsAg阳性母亲的哺乳10。 HBV DNA水平是影响HBV母婴传播的最关键因素13。HBV DNA水平较高(>106 U/ml)母亲的新生儿更易发生母婴传播。近年有研究显示,对这部分母亲在妊娠中后期应用抗病毒药物,可使孕妇产前血清中HBV DNA水平降低,提高新生儿的母婴阻断成功率14-17。在充分告知风险、权衡利弊和患者签署知情同意书的情况下,可对HBV DNA高水平孕妇给予抗病毒药物,以提高新生儿的HBV母婴传播的阻断率,具体请参见“特殊人群抗病毒治疗-妊娠相关情况处理”。 对HBsAg阴性母亲的新生儿可用10μg重组酵母乙型肝炎疫苗免疫;对新生儿时期未接种乙型肝炎疫苗的儿童应进行补种,剂量为10μg重组酵母乙型肝炎疫苗或20μg 仓鼠卵巢细胞(CHO)重组乙型肝炎疫苗;对成人建议接种3针20μg重组酵母乙型肝炎疫苗或20μg CHO重组乙型肝炎疫苗。对免疫功能低下或无应答者,应增加疫苗的接种剂量(如60μg)和针次;对3针免疫程序无应答者可再接种1针60μg或3针20μg重组酵母乙型肝炎疫苗,并于第2次接种乙型肝炎疫苗后1~2个月检测血清中抗-HBs,如仍无应答,可再接种1针60μg重组酵母乙型肝炎疫苗。 接种乙型肝炎疫苗后有抗体应答者的保护效果一般至少可持续12年18,因此,一般人群不需要进行抗-HBs监测或加强免疫。但对高危人群可进行抗-HBs监测,如抗-HBs2 000 IU/mL,ALT持续或间歇升高,肝组织学中度或严重炎症坏死,肝纤维化可快速进展,部分可发展为肝硬化和肝衰竭。 低 (非) 复制期:血清HBeAg阴性、抗-HBe阳性,HBV DNA水平低或检测不到(20 000 IU/mL),ALT持续或反复异常,成为HBeAg阴性慢性乙型肝炎30。也可再次出现HBeAg阳转。 并非所有HBV感染者都经过以上4个期。青少年和成年时期感染HBV,多无免疫耐受期,直接进入免疫清除期。 自发性HBeAg血清学转换主要出现在免疫清除期,年发生率约为2%~15%。年龄小于40岁、ALT升高、HBV基因A型和B型者发生率较高28, 31。HBeAg血清学转换后,每年约有0.5%~1.0%发生HBsAg清除32。有研究显示,HBsAg消失10年后,约14%的患者肝脏中仍可检测出cccDNA33。HBsAg消失时患者超过50岁,或已经发展为肝硬化,或合并HCV或HDV感染,尽管发展为肝癌几率低,但仍可能发生34。 慢性乙型肝炎患者肝硬化的年发生率为2%~10%35,危险因素包括宿主(年龄大、男性、发生HBeAg血清学转换时大于40岁36、ALT持续升高37),病毒(HBV DNA >2 000 IU/mL)、HBeAg持续阳性38、基因型C、合并HCV、HDV或HIV感染),以及环境(酒精和肥胖)35, 39。代偿期肝硬化进展为肝功能失代偿的年发生率为3%~5%,失代偿期肝硬化5年生存率为14%~35%35。 非肝硬化HBV感染者的HCC年发生率为0.5%~1.0%35。肝硬化患者HCC年发生率为3%~6%40-42。发生HCC、肝硬化的危险因素相似。此外,罹患肝硬化、糖尿病、直系亲属有肝癌病史、血清HBsAg高水平,以及黄曲霉毒素均与肝癌发生相关35, 39, 43-47。较低的HBsAg水平常反映宿主对HBV复制和感染具有较好的免疫控制。对于HBeAg阴性、HBV DNA低水平(?2000 IU/mL)、B或C基因型HBV感染患者,高水平HBsAg(HBsAg ≥1000 IU/mL)增加肝癌的发生风险46, 47。 发病机制 慢性乙型肝炎的发病机制较为复杂,迄今尚未完全阐明。大量研究表明,HBV不直接杀伤肝细胞,其引起的免疫应答是肝细胞损伤及炎症发生的主要机制。而炎症反复存在是慢性乙型肝炎患者进展为肝硬化甚至肝癌的重要因素。 固有免疫在HBV感染初期发挥作用,并诱导后续的特异性免疫应答。慢性HBV感染者的非特异免疫应答受到损伤48, 49。HBV可通过自身HBeAg、HBx等多种蛋白成分,通过干扰toll-样受体(toll-like receptors,TLRs)、维甲酸诱导基因(retinoic acid inducible gene-I ,RIG-I) 两种抗病毒信号转导途径,来抑制非特异免疫应答的强度。慢性乙型肝炎患者常表现为髓样树突状细胞 (mDc)、浆样树突状细胞 (pDc)在外周血中频数低,mDC存在成熟障碍,pDc产生IFN-a的能力明显降低,机体直接清除病毒和诱导HBV特异性T细胞功能产生的能力下降,不利于病毒清除。 HBV特异性免疫应答在HBV清除中起主要作用50。MHC1类分子限制性的CD8+细胞毒性T淋巴细胞可诱导肝细胞凋亡,也可分泌IFN-γ,以非细胞裂解机制抑制其他肝细胞内HBV基因表达和复制51。慢性感染时,HBV特异性T细胞易凋亡,寡克隆存在,分泌细胞因子功能和增殖能力显著降低,T细胞功能耗竭,HBV持续复制52。 五、实验室检查 (一)HBV血清学检测 HBV血清学标志物包括HBsAg、抗-HBs、HBeAg、抗-HBe、抗-HBc和抗-HBc-IgM。HBsAg阳性表示HBV感染;抗-HBs为保护性抗体,其阳性表示对HBV有免疫力,见于乙型肝炎康复及接种乙型肝炎疫苗者;抗-HBc-IgM阳性多见于急性乙型肝炎及慢性乙型肝炎急性发作;抗-HBc总抗体主要是抗-HBc-IgG,只要感染过HBV,无论病毒是否被清除,此抗体多为阳性。在HBeAg阳性的慢性乙型肝炎患者中,基线抗-HBc抗体的定量对聚乙二醇干扰素(Peg-IFN)和核苷(酸)类似物(NAs)治疗的疗效有一定的预测价值53, 54。血清HBsAg定量检测可用于预测疾病进展、抗病毒疗效和预后9, 55, 56。为了解有无HBV与HDV同时或重叠感染,可进行HDV感染标志物的检测。 (二)HBV DNA、基因型和变异检测 1.HBV DNA定量检测:主要用于判断慢性HBV感染的病毒复制水平,可用于抗病毒治疗适应证的选择及疗效的判断。准确定量需采用实时定量聚合酶链反应(real-time quantitative PCR)法。 2.HBV基因分型和耐药突变株检测:常用的方法有:(1)基因型特异性引物聚合酶链反应(PCR)法;(2)基因序列测定法;(3)线性探针反向杂交法。 (三)生物化学检查 1. 血清ALT和AST:血清ALT和AST水平可部分反映肝细胞损伤程度,但特异性不强,应与心、脑、肌肉损害时的升高鉴别。 2. 血清胆红素:血清胆红素水平与胆汁代谢、排泄程度有关,胆红素升高主要原因为肝细胞损害、肝内外胆道阻塞和溶血。肝衰竭患者血清胆红素可呈进行性升高,每天上升≥1倍正常值上限(ULN),且有出现胆红素升高与ALT和AST下降的分离现象。 3. 血清白蛋白和球蛋白:反映肝脏合成功能,慢性乙型肝炎、肝硬化和肝衰竭患者可有血清白蛋白下降。随着肝损害加重,白蛋白/球蛋白比值可逐渐下降或倒置(2,预示患者已经发生肝硬化。APRI计算公式为[(AST/ULN) ×100/PLT (10^9/L)]64 。 2. FIB-4 指数:基于 ALT、AST、PLT和患者年龄的FIB-4 指数可用于慢性乙型肝炎患者肝纤维化的诊断和分期。FIB4=(年龄 x AST)÷(血小板 x ALT的平方根)。 3. 瞬时弹性成像:瞬时弹性成像(transient elastography,TE)作为一种较为成熟的无创伤性检查,其优势为操作简便、可重复性好,能够比较准确地识别出轻度肝纤维化和进展性肝纤维化或早期肝硬化65, 66;但其测定成功率受肥胖、肋间隙大小以及操作者的经验等因素影响,其测定值受肝脏炎症坏死、胆汁淤积以及脂肪变等多种因素影响。鉴于胆红素异常对TE诊断效能的显著影响,应考虑胆红素正常情况下进行TE检查。TE结果判读需结合患者ALT水平等指标,将TE与其他血清学指标联合使用可以提高诊断效能67, 68。 瞬时弹性成像的临床应用:胆红素正常没有进行过抗病毒治疗者肝硬度测定值(LSM)≥17.5kPa诊断肝硬化,LSM≥12.4kPa(ALT
杨晴 主任医师 珠海市人民医院医疗集团 肝病科6966人已读 - 精选 专家谈自身免疫性肝炎
1、自身免疫性肝炎,诊断是第一位近年来大家对自身免疫性肝炎的认识逐渐增加,而诊断对自身免疫性肝炎是第一位的,治疗相对简单。自身免疫性肝炎的诊断包括几个方面。第一个是单纯的自身免疫性肝炎。这种自免肝相对简单,用激素治疗就可以;第二个是重叠综合征,比如自身免疫性肝炎和原发性胆汁性肝硬化的重叠,和原发性硬化性胆管炎的重叠,甚至和丙型肝炎、乙型肝炎都可能有重叠。第三个是自身免疫性肝炎和药物性肝炎的鉴别诊断。这个是比较难的。药物本身可诱发自身免疫性肝炎,而一部分药物性肝炎有免疫紊乱,表现为免疫介导的肝损害。所以药物性肝炎很像自身免疫性肝炎,但又不完全一样。因此在诊断的时候应该把这几点分清楚。2、相对适应症:需不需要治疗?近15年来,国际指南关于自身免疫性肝炎的治疗建议几乎没有变化。但是我们结合中国的国情和自己的临床经验做了一些修改,这里和大家分享一下。首先,国外指南里的适应症包括绝对适应症和相对适应症。绝对适应症指转氨酶高于正常10倍以上,病理上有明显的多小叶融和性坏死、桥接坏死等炎症坏死表现。绝对适应症需要马上治疗。如果患者转氨酶没达到正常10倍以上,只是正常5倍以上,免疫球蛋白两倍以上,也是必需治疗的人群。对国内外的肝病医生来说,相对适应症需不需要治疗是大学问。相对适应症也分为好几种。第一种是已经有肝损害,有慢性肝炎的明确表现,就需要治疗;第二种是患者年龄比较大,虽然没有肝损害或者慢性肝炎的明确表现,但是出现黄疸等,也一定要治疗;第三种是患者依从性不是很好,这种情况也应该积极地采取干预措施。我们有过这样的经验教训,有位患者第一次来看病时,病情不太严重,自己不想用激素,未接受治疗。过了一段时间这位患者再来复查,病情已经很严重了,有明显的肝炎表现甚至已经出现肝硬化。我们再次建议这位患者用激素治疗,她还是拒绝了。等到这位患者第三次来复查时,就已经是肝硬化出血、消化道大出血了。最后死于消化道出血。这个经验教训告诉我们相对适应症还是要积极地干预治疗的。刚才说的这位患者应该当作绝对适应证来处理。其他症状轻微的患者如果年轻、基础很好、依从性很好可以先观察。但我个人认为一旦明确诊断自身免疫性肝炎,建议都要积极治疗。自身免疫性肝炎患者对治疗的应答非常好,可以有效地控制疾病进展。自身免疫性肝炎有急性发作,也有慢性反复,如果不治疗,患者可能突发重型肝炎、肝衰竭,这样的打击对病人是非常不利的。3、自免肝的治疗:激素±硫唑嘌呤自身免疫性肝炎的治疗方案基本还是以激素为主,加或不加硫唑嘌呤。激素的选择上,国外建议使用强的松或强的松龙,但是国内部分医生尤其是一些风湿免疫科的医生都建议用甲基强的松龙。我查阅相关资料,总结甲基强的松龙与强的松或强的松龙的区别有以下几点。一是甲基强的松龙和强的松龙在半衰期或者副作用方面没有明显区别。但是强的松和强的松龙比甲基强的松龙生物利用度高。二是甲基强的松龙价格也比较贵。三是甲基强的松龙可以静脉用药,冲击治疗的时候可以使用。比如重症黄疸患者可以用甲基强的松龙快速冲击治疗。但实际上自免肝需要药物持续发挥作用,保持持续的免疫抑制状态,不建议甲强冲击疗法,不建议静脉点滴,口服就可以了。所以我还是建议用强的松或者强的松龙。在国外强的松和强的松龙的区别主要是价格,强的松非常便宜,强的松龙比较贵。因为强的松要从肝脏代谢为强的松龙发挥作用,所以如果肝脏功能很差或有肝硬化的病人,直接就建议强的松龙。当然所有的病人都可以使用强的松龙。第二个争议的问题是硫唑嘌呤用不用。因为硫唑嘌呤本身取代不了激素,但是可以辅佐激素来发挥其免疫抑制作用。对于不能大量使用激素,需要较多考虑副作用的患者,可以激素联合硫唑嘌呤治疗,从而使激素减量。虽然个别患者使用硫唑嘌呤会出现白细胞下降,甚至有瘀胆的报告,但硫唑嘌呤总体上是非常安全的。一般来讲50mg/天的剂量是非常安全的。4、激素的使用:剂量、疗程及副作用激素使用的剂量和疗程都很重要。国外建议的激素起始量太大,减量速度太快,不适合中国的患者。我国自免肝患者敏感性比较好,应答比较好,起始剂量30-40mg就可以了。如果联合硫唑嘌呤可以用更少量的激素。在激素减量方面,一般是这样,起始剂量30-40mg两周后复查。如果酶学指标、生化指标有所改善,病情没有恶化就可以减量。再过两周,如果复查病情有所改善,没有恶化,可以继续减量。然后维持这个剂量治疗一个月以上再考虑第三次减量。越往后减量越慢。关于维持剂量的问题,国外建议单用激素维持剂量是20mg。这一剂量非常大,病人肯定耐受不了,国外患者对激素很敏感,所以我认为他们的方法是有问题的。在我国单用激素维持剂量是5-10mg,如果联合硫唑嘌呤,基本5mg都能维持。当激素减量到一定程度的时候一定要监测自免肝相关的指标。减量到5-10mg时,需要监测其免疫指标。不能等到转氨酶反弹,因为一旦反弹就需要从头开始治疗。关于疗程的问题。自身免疫性肝炎患者如果出现肝硬化,基本就不再停药了。在我们门诊,大部分慢性自身免疫性肝炎且基础不太好的患者都需要坚持吃药。因为自身免疫性肝炎复发率比较高,治疗后3-4年的复发率达30%多,而小剂量维持治疗如5mg、7.5mg或者10mg副作用很小。如果出现停药后反弹需要从头治疗,副作用更大。所以长期治疗很重要,轻易不要停药。激素的副作用大家都比较了解,自免肝治疗最需要关注的是激素副作用的预防和处理。我们常规使用抑制胃酸分泌的药物预防消化道出血,但不能用太强的抑酸药如洛赛克、质子泵抑制剂,一般用H2受体阻滞剂就可以了。我们常用的是法莫替丁,晚上睡觉之前吃一粒就可以。对于出现骨质疏松的患者建议服用骨化醇、钙片等5、特殊患者的治疗5.1 自身免疫性肝炎合并肝硬化还有一些特殊情况,比如肝硬化患者,很多基层医生不敢治疗自免肝合并肝硬化的患者,尤其是失代偿期肝硬化,有腹水或出血风险的患者。实际上这些病人治疗受益明显,可以逆转失代偿状态。很多患者起初合并腹水、低蛋白血症、脾大,治疗十几年以后检查各项指标,却看不出他曾有肝硬化或者肝炎。因为肝修复再生能力很强,有效的治疗可以很好的控制病情,甚至可以完全逆转肝硬化,这一点非常重要。肝硬化要治,但是风险也要好好掌控,如果出血风险增加,感染风险增加,及时做出相应处理就可以。肝硬化患者不管到哪一期,都要积极治疗,即使是失代偿期肝硬化也要治疗,只是风险更大而已,跟病人谈知情同意,让他知道用激素的必要性,有可能逆转病情,但是可能出现一些副作用,让病人提前知晓了解。5.2 自身免疫性肝炎孕/产妇还有一些孕妇、产妇的问题。自身免疫性肝炎孕妇也要积极治疗,激素对于胎儿和孕/产妇是安全的,而硫唑嘌呤可能会增加流产的风险,一般不建议使用。要注意妊娠后期妊高症、水钠潴留等问题,要加强对激素副作用的干预。5.3 青少年自身免疫性肝炎青少年自身免疫性肝炎患者肝肾微粒体抗体阳性,这种情况相对比较棘手。青少年自身免疫性肝炎的特点是进展比较快,激素治疗效果不太好,复发率高,而其免疫球蛋白水平不高,没有很好的监测指标。总体来讲,青少年自免肝患者的激素剂量相对大一点,基本是1mg/kg体重,个别用到1.5mg/kg体重,也可以联合硫唑嘌呤。青少年自免肝患者联合硫唑嘌呤要注意监测血象,因为硫唑嘌呤可能导致白细胞降低,增加血生再障的风险。青少年用激素治疗的原则首先是激素相对足量,其次是疗程要长。有一部分患者即使遵循上述原则治疗效果也不太好。如果自身免疫性肝炎患者对激素不敏感,或者耐受性不好,就可以联用骁悉(酶芬酸酯),能增加疗效。此外还可以联用环孢素A等,就是价格比较贵,但大部分患者治疗反应都比较好。5.4 自身免疫性肝炎合并丙肝最后还要说一下自身免疫性肝炎合并丙肝这种比较少见的情况。我们医院已经诊断了好几例这样的患者。有很多医生对自身免疫性肝炎合并丙肝的诊治比较困惑。国外认为自身免疫性肝炎分型I、II、III型,其中II型分IIa、IIb型,IIa为普通的自身免疫性肝炎、青少年自身免疫性肝炎,IIb型为丙肝导致的自身免疫性肝炎,丙肝和自身免疫性肝炎可能有重叠,鉴别起来比较困难,需要做肝活检鉴别。如果自身免疫性肝炎和丙肝重叠,首先治疗自身免疫性肝炎。这一点非常重要。目前我国丙肝治疗的标准方案是干扰素+利巴韦林,而干扰素会加重自身免疫性肝炎,所以必须先治疗自身免疫性肝炎。在使用激素+免疫抑制剂的基础上,如果各方面指标仍不稳定,再考虑加用干扰素和利巴韦林。6、医患良好沟通,提高患者依从性首先,医生要与患者建立良好的沟通,告诉患者自身免疫性肝炎大部分是慢性进展性疾病,很少是自限的,一定要定期检查,三个月检查一次,接受激素治疗的患者也需要三个月复诊一次。患者的依从性很重要,这决定了他的预后,这一点需要跟患者说清楚,定期检查基本可以保证病情不进展到肝硬化。在激素减量过程中,后期激素剂量到10mg时,过3个月、5个月甚至半年再考虑往下递减,这一时期要监测免疫球蛋白等指标。如果初始治疗后免疫球蛋白下降,甚至自身抗体消失,生化指标复常,而随访过程中发现指标有波动,球蛋白升高,就要警惕再发风险。我们的患者一般很少复发,因为不等病情反弹我们就采取干预措施了。其次是按时吃药,患者有时对激素的副作用有所顾忌,比较抗拒服用激素,这一点要好好做工作。要告诉患者激素治疗自身免疫性肝炎效果非常好,能有效控制病情进展,但是要长期用药。另外,我们使用的激素量不大,副作用的风险可控。有些患者对激素的恐惧不太正常,激素导致股骨头坏死常见于大剂量冲击治疗,而自身免疫性肝炎完全用不着冲击疗法,都是维持治疗。这些都要跟病人交代清楚,实际沟通很重要,如果真的出现沟通也无效的时候,医生态度要坚决,不能模棱两可。 ——王贵强教授专访 医脉通 2014-12-16
杨晴 主任医师 珠海市人民医院医疗集团 肝病科1.3万人已读 - 精选 原发性肝癌诊疗指南(2022年版)全文来了!
原发性肝癌诊疗指南(2022年版)国家卫生健康委办公厅一、概述原发性肝癌是目前我国第4位常见恶性肿瘤及第2位肿瘤致死病因,严重威胁我国人民的生命和健康。原发性肝癌主要包括肝细胞癌(hepatocellularcarcinoma,HCC)、肝内胆管癌(intrahepaticcholangiocarcinoma,ICC)和混合型肝细胞癌-胆管癌(combinedhepatocellular-cholangiocarcinoma,cHCC-CCA)三种病理学类型,3者在发病机制、生物学行为、组织病理学、治疗方法及预后等方面差异较大,其中HCC占75%~85%、ICC占10%~15%。本指南中的“肝癌”仅指HCC。为进一步规范我国肝癌诊疗行为,2017年6月原国家卫生和计划生育委员会公布了《原发性肝癌诊疗规范(2017年版)》,国家卫生健康委员会于2019年12月进行了更新。《原发性肝癌诊疗规范(2019年版)》反映了当时我国肝癌诊断和多学科综合治疗及研究的状况,对规范肝癌的诊疗行为、改善肝癌患者预后、保障医疗质量和医疗安全及优化医疗资源发挥了重要作用。自《原发性肝癌诊疗规范(2019年版)》发布以来,国内外在肝癌的诊断、分期及治疗方面出现了许多符合循证医学原则的高级别证据,尤其是适应中国国情的研究成果相继问世。为此,国家卫生健康委员会委托中华医学会肿瘤学分会联合中国抗癌协会肝癌专业委员会、中华医学会超声医学分会、中国医师协会外科医师分会和中国医师协会介入医师分会等组织全国肝癌领域的多学科专家,结合肝癌临床诊治和研究的最新实践,再次修订并更新形成《原发性肝癌诊疗指南(2022年版)》(以下简称指南),旨在推动落实并达成《“健康中国2030”规划纲要》中总体癌症5年生存率提高15%的目标。证据评价与推荐意见分级、制定和评价(GradingofRecommendations,Assessment,DevelopmentandEvaluation,GRADE)方法学是目前使用最广泛的证据评价和推荐意见分级系统。GRADE系统包括两部分,第一部分为证据评价,根据证据中的偏倚风险、不一致性、间接性、不精确性和发表偏倚,将证据质量分为高、中、低和极低4个水平;第二部分为推荐意见分级,考虑医学干预的利弊平衡、证据质量、价值观念与偏好及成本与资源耗费等因素制定推荐意见,并将推荐意见分为强推荐和弱推荐(有条件推荐)两种。医学干预的利弊差别越大、证据质量越高、价值观念与偏好越清晰越趋同、成本与资源耗费越小,则越应该考虑强推荐。反之,则应考虑弱推荐(有条件推荐)。本指南中的循证医学证据等级评估参照了上述GRADE分级的指导原则,采用了《牛津循证医学中心分级2011版》作为辅助工具来具体执行证据分级(附录1)。在从证据转换成推荐意见的方法上,专家组主要参考了上述GRADE分级对推荐意见分级的指导原则,同时结合了美国临床肿瘤学会指南的分级方案,对推荐意见分级做了相应的修改(附录2)。最终将推荐强度分为三个等级,分别是强推荐、中等程度推荐和弱推荐。强推荐代表专家组对该推荐意见反映了最佳临床实践有很高的信心,绝大多数甚至所有的目标用户均应采纳该推荐意见。中等程度推荐代表专家组对该推荐意见反映了最佳临床实践有中等程度的信心,多数目标用户会采纳该推荐意见,但执行过程中应注意考虑医患共同决策。弱推荐代表专家组对该推荐意见反映了最佳临床实践有一定的信心,但是应该有条件地应用于目标群体,强调医患共同决策。二、筛查和诊断(一)肝癌高危人群的筛查与监测对肝癌高危人群的筛查与监测,有助于肝癌的早期发现、早期诊断和早期治疗,是提高肝癌疗效的关键。肝癌高危人群的快速、便捷识别是实施大范围肝癌筛查的前提,而对人群肝癌风险的分层评估是制定不同肝癌筛查策略的基础。在我国,肝癌高危人群主要包括:具有乙肝病毒(hepatitisBvirus,HBV)和(或)丙肝病毒(hepatitisCvirus,HCV)感染、过度饮酒、非酒精性脂肪性肝炎、其他原因引起的肝硬化及有肝癌家族史等人群,尤其是年龄>40岁的男性。目前,尽管抗HBV和抗HCV治疗可显著降低肝癌的发生风险,但仍无法完全避免肝癌的发生。由我国学者研发的适用于多种慢性肝病和各种族的肝癌风险评估模型age-male-AlBi-plateletsscore(aMAP评分),可便捷地将肝病人群分为肝癌低风险(0~50分)、中风险(50~60分)和高风险(60~100分),各组肝癌的年发生率分别为0~0.2%、0.4%~1.0%和1.6%~4.0%,有助于确定肝癌的高风险人群(证据等级2,推荐B)。借助肝脏超声显像和血清甲胎蛋白(alpha-fetoprotein,AFP)进行肝癌早期筛查,建议高危人群至少每隔6个月进行1次检查(证据等级2,推荐A)。通过实现社区、医院一体化筛查新模式,做到应筛尽筛
杨晴 主任医师 珠海市人民医院医疗集团 肝病科299人已读 - 精选 预防、治疗更为积极!慢性乙型肝炎防治指南(2022年版)发布了!
为了规范和更新慢性乙型肝炎的预防、诊断和抗病毒治疗,实现世界卫生组织提出的“2030年消除病毒性肝炎作为公共卫生危害”目标,中华医学会肝病学分会和感染病学分会于2022年组织国内有关专家,以国内外慢性乙型肝炎病毒感染的基础和临床研究进展为依据,结合我国的实际情况,更新形成了《慢性乙型肝炎防治指南(2022年版)》。以更广泛进行筛查、更积极预防和抗病毒治疗为原则,为慢性乙型肝炎的预防、诊断和治疗提供重要依据。现摘要转载指南推荐意见如下:推荐意见1:对HBsAg阴性母亲的新生儿,应在出生后12h内尽早接种10μg重组酵母乙型肝炎疫苗,在1、6个月时分别接种第2和第3剂乙型肝炎疫苗(A1)。危重症新生儿,如超低体质量儿(<1000g)、严重出生缺陷、重度窒息、呼吸窘迫综合征等,应在生命体征平稳后,尽早接种第1剂乙型肝炎疫苗(A1)。推荐意见2:对HBsAg阳性或不详母亲的新生儿,应在出生后12h内尽早注射一剂次100IUHBIG,同时在不同部位接种10μg重组酵母乙型肝炎疫苗。在1、6个月时分别接种第2和第3剂乙型肝炎疫苗(A1)。建议对HBsAg阳性或不详母亲所生儿童,于接种第3剂乙型肝炎疫苗后1~2个月时进行HBsAg和抗-HBs检测。若HBsAg阴性、抗-HBs<10mIU/ml,可按0、1、6个月免疫程序再接种3剂乙型肝炎疫苗;若HBsAg阳性,为免疫失败,应定期监测(A1)。推荐意见3:HBsAg阳性或不详母亲的早产儿、低体质量儿(<2500g)也应在出生后12h内尽早接种HBIG和第1剂乙型肝炎疫苗。早产儿或低体质量儿满1月龄后,再按0、1、6个月程序完成3剂次乙型肝炎疫苗免疫(A1)。推荐意见4:新生儿在出生12h内接种了HBIG和乙型肝炎疫苗后,可接受HBsAg阳性母亲的哺乳(B1)。推荐意见5:对于未接种或未完成全程乙型肝炎疫苗接种的儿童,应及时进行补种。第1剂与第2剂间隔时间应≥28d,第2剂与第3剂间隔应≥60d(A1)。推荐意见6:对3剂免疫程序无应答者,可再接种1剂60μg或3剂20μg乙型肝炎疫苗,并于完成第2次接种程序后1~2个月时检测血清抗-HBs,如仍无应答,可再接种1剂60μg重组酵母乙型肝炎疫苗(A1)。推荐意见7:意外暴露于HBV者可按照以下方法处理:(1)在伤口周围轻轻挤压,排出伤口中的血液,再对伤口用等渗盐水冲洗,然后用消毒液处理(A1)。(2)应立即检测HBsAg、HBVDNA,3~6个月后复查(A1)。(3)如接种过乙型肝炎疫苗并有应答者,且已知抗-HBs阳性(抗-HBs≥10mIU/ml)者,可不再注射HBIG或乙型肝炎疫苗。如未接种过乙型肝炎疫苗,或虽接种过乙型肝炎疫苗,但抗-HBs<10mIU/ml或抗-HBs水平不详者,应立即注射HBIG200~400IU,同时在不同部位接种1剂乙型肝炎疫苗(20μg),于1个月和6个月后分别接种第2剂和第3剂乙型肝炎疫苗(20μg)(A1)。推荐意见8:在不涉及入托、入学和入职的健康体格检查或就医时,应进行HBsAg筛查。对一般人群均应进行HBsAg筛查,特别是人类免疫缺陷病毒(humanimmunodeficiencyvirus,HIV)感染者、男男性行为者、静脉药瘾者、HBV感染者的性伴侣和家庭接触者、接受免疫抑制剂或抗肿瘤药物、抗丙型肝炎病毒(hepatitisCvirus,HCV)药物治疗者等,以及孕妇和育龄期、备孕期女性(B1)。推荐意见9:对HBsAg阳性者,包括正在接受抗病毒治疗的CHB患者,应尽可能采用高灵敏且检测线性范围大的HBVDNA检测方法(定量下限为10~20IU/ml)(A1)。十|抗病毒治疗的适应证|推荐意见10:对于血清HBVDNA阳性,ALT持续异常(>ULN),且排除其他原因所致者,建议抗病毒治疗(B1)。推荐意见11:对于血清HBVDNA阳性者,无论ALT水平高低,只要符合下列情况之一,建议抗病毒治疗:(1)有乙型肝炎肝硬化家族史或HCC家族史(B1);(2)年龄>30岁(B1);(3)无创指标或肝组织学检查,提示肝脏存在明显炎症(G≥2)或纤维化(F≥2)(B1);(4)HBV相关肝外表现(如HBV相关性肾小球肾炎等)(B1)。推荐意见12:临床确诊为代偿期和失代偿期乙型肝炎肝硬化患者,无论其ALT和HBVDNA水平及HBeAg阳性与否,均建议抗病毒治疗。同时应注意寻找并治疗肝硬化的其他病因(如酒精、肥胖、糖尿病、自身免疫或遗传代谢性肝病等)(B1)。推荐意见13:HBeAg阳性CHB患者首选NAs(ETV、TDF、TAF或TMF)治疗(A1)。大多数患者需要长期用药,最好至HBsAg消失再停药。如因各种原因希望停药,治疗1年HBVDNA低于检测下限、ALT复常和HBeAg血清学转换,再巩固治疗至少3年(每隔6个月复查1次)仍保持不变,且HBsAg<100IU/ml,可尝试停药,但应严密监测,延长疗程可减少复发(B2)。推荐意见14:HBeAg阳性CHB患者也可采用Peg-IFN-α治疗。治疗24周时,若HBVDNA下降<2log10 IU/ml且HBsAg定量仍>2×104 IU/ml,建议停用Peg-IFN-α治疗,改为NAs治疗(A1)。Peg-IFN-α有效患者疗程为48周,可以根据病情需要延长疗程,但不宜超过96周(B1)。推荐意见15:HBeAg阴性CHB患者首选NAs(ETV、TDF、TAF或TMF)治疗(A1)。建议HBsAg消失和/或出现抗-HBs,且HBVDNA检测不到,巩固治疗6个月仍检测不到者,可停药随访(B1)。推荐意见16:HBeAg阴性CHB患者也可采用Peg-IFN-α治疗。治疗12周时,若HBVDNA下降<2log10 IU/ml,或HBsAg定量下降<1log10 IU/ml,建议停用Peg-IFN-α治疗,改为NAs治疗(B1)。有效者疗程为48周,可以根据病情需要延长疗程,但不宜超过96周(B1)。推荐意见17:在一些符合条件的患者中,如:NAs治疗后HBVDNA定量<检测下限、HBeAg阴转,且HBsAg<1500IU/ml时,结合患者意愿可考虑加用Peg-IFN-α治疗,以追求临床治愈。治疗24周后,若HBsAg<200IU/ml或下降>1log10 IU/ml,建议继续NAs联合Peg-IFN-α治疗至48~96周;治疗24周后,若HBsAg仍≥200IU/ml,可考虑停用Peg-IFN-α,继续NAs治疗(B2)。推荐意见18:代偿期乙型肝炎肝硬化患者,推荐采用ETV、TDF、TAF进行长期抗病毒治疗;如果采用Peg-IFN-α治疗,需密切监测相关不良反应(A1)。推荐意见19:失代偿期乙型肝炎肝硬化患者,推荐采用ETV或TDF长期治疗,禁用Peg-IFN-α治疗(A1),若必要可以应用TAF治疗(B1)。推荐意见20:CHB患者应用ETV、TDF、TAF或TMF治疗48周,HBVDNA可检出者(HBVDNA>20IU/ml),排除依从性和检测误差后,可调整NAs治疗(应用ETV者换用TDF或TAF,应用TDF或TAF者换用ETV,或两种药物联合使用)(B1)。也可以联合Peg-IFN-α治疗(B1)。推荐意见21:乙型肝炎肝硬化患者应用ETV、TDF或TAF治疗24周,若HBVDNA仍可检出(HBVDNA>20IU/ml),排除依从性和检测误差后,建议调整NAs治疗(应用ETV者换用TDF或TAF,应用TDF或TAF者换用ETV,或两种药物联合使用)(C2)。推荐意见22:所有接受化学治疗、靶向药物及免疫抑制剂治疗的患者,开始治疗前均应常规筛查HBsAg、抗-HBc和/或HBVDNA(A1)。对于HBsAg和/或HBVDNA阳性者,在开始化学治疗、靶向药物及免疫抑制剂治疗前至少1周、特殊情况可同时应用ETV、TDF或TAF抗病毒治疗(A1)。对于HBsAg阴性、抗-HBc阳性患者,若使用B淋巴细胞单克隆抗体或进行造血干细胞移植,或伴进展期肝纤维化/肝硬化,建议应用ETV、TDF或TAF抗病毒治疗(B1)。推荐意见23:慢性HBV感染者准备近期妊娠,或妊娠期间有抗病毒指征时,在充分沟通并知情同意后,可以使用TDF治疗(B1)。如合并肾功能不全,可考虑使用TAF治疗(B2)。推荐意见24:抗病毒治疗期间意外妊娠的患者,若使用TDF治疗,建议继续妊娠;若使用ETV,可不终止妊娠,建议换用TDF治疗(B1)。若应用干扰素治疗,建议向孕妇和家属充分告知风险,由其决定是否继续妊娠。若继续妊娠,应停用干扰素,换用TDF治疗(C2)。推荐意见25:妊娠中晚期HBVDNA定量>2×105 IU/ml,在充分沟通并知情同意的基础上,于妊娠第24~28周开始应用TDF抗病毒治疗(A1)。建议HBeAg阳性慢性HBV感染者(免疫耐受期)母亲于产后可考虑即刻或1~3个月时停药,停药后应至少每3个月检测肝脏生物化学和HBVDNA等指标,直至产后6个月,发生肝炎活动者应立即启动抗病毒治疗(A2);HBeAg阳性或阴性CHB母亲,在充分沟通和知情同意的基础上,产后可继续治疗。应用TDF治疗者,母乳喂养不是禁忌证(C2)。推荐意见26:对于进展期肝病或肝硬化患儿,无论年龄大小,均应及时进行抗病毒治疗,但需考虑长期治疗的安全性及耐药问题。1岁及以上儿童可考虑普通干扰素α治疗;2岁及以上儿童可选用ETV或TDF治疗;5岁及以上儿童可选用Peg-IFN-α-2a;12岁及以上儿童可选用TAF治疗(A1)。推荐意见27:对于HBVDNA阳性,ALT<ULN的患儿需进行肝组织学评估,如肝脏组织学分级G≥1,应该抗病毒治疗(B1);对于年龄1~7岁的患儿,即使缺少肝脏病理学检查结果,在充分沟通及知情同意的前提下,也可考虑抗病毒治疗。使用抗病毒药物和方案参照儿童进展期CHB(C1)。推荐意见28:慢性肾脏病患者、肾功能不全或接受肾脏替代治疗的CHB患者,推荐ETV或TAF抗HBV治疗,不建议应用ADV或TDF(B1)。对于存在肾脏损伤高危风险的CHB患者,应用任何NAs抗病毒过程中均需监测肾功能变化。已应用ADV或TDF的患者发生肾脏或骨骼疾病或存在高危风险时,建议改用ETV或TAF(B1)。推荐意见29:HCV和HBV合并感染者应用DAA治疗HCV时,若HBsAg阳性,需给予NAs治疗以预防HBV再激活,DAA治疗结束12周后,可考虑停止NAs治疗(B2);HBsAg阴性、抗-HBc阳性者应用DAA期间,需密切监测HBVDNA和HBsAg定量,如HBsAg阳转,建议应用NAs治疗(B2)。推荐意见30:HBV和HIV合并感染者,建议选择对HIV和HBV均有效的抗病毒药物组合,同时选择2种抗HBV活性的药物(A1)。推荐意见31:HBV相关急性、亚急性、慢加急性和慢性肝衰竭患者,若HBsAg阳性建议应用ETV、TDF或TAF抗病毒治疗(A1)。推荐意见32:HBV相关HCC患者,若HBsAg阳性,建议应用ETV、TDF或TAF进行抗病毒治疗(A1)。推荐意见33:因HBV相关感染进行肝移植患者,若HBsAg阳性,建议在肝移植前开始应用ETV、TDF或TAF进行抗病毒治疗(A1)。
 杨晴 主任医师 珠海市人民医院医疗集团 肝病科686人已读
杨晴 主任医师 珠海市人民医院医疗集团 肝病科686人已读 - 引用 中药并非无毒,中药的肝毒性不可小觑
在很多人的观念里,中药都是纯天然、安全无毒的,因而比西药安全,可以放心服用,所以有不少人明明身体健康,却把中药当成滋补品长期服用,或当做预防疾病的灵丹妙药,而且认为:中药是用来调理身体的,那么药量和服药时间可以很随意。但事实上,中药并非无毒,也不比西药更安全,其中中药的肝毒性就是临床上值得关注的问题之一。据统计,我国中草药和膳食补充剂引起的肝损伤,可能占药物性肝损害的26.81%[6]。目前关于中药肝毒性,临床报道比较多的是何首乌。其实,随着中药毒性研究逐渐深入,一些传统的、被认为无毒的中药,也陆续被发现有潜在的毒性。总结至今临床发现的可致肝损伤常用中药有:黄药子、菊三七、苍耳子、何首乌、雷公藤、艾叶、望江南、苍术、天花粉、桑寄生、贯众蒲黄、麻黄、柴胡、番泻叶、蜈蚣、合欢皮、丁香,川楝子、鸦胆子、冬青、蓖麻子、黎芦、丹参、罂粟、桑寄生、姜半夏、泽泻、大黄虎杖、贯众、艾叶、千里光、防己、土荆芥、肉豆蔻、商陆、常山、大枫子、朱砂、斑蝥、穿山甲、黄芩、缬草、乌头、白果等及含有以上成分的中药复方制剂如壮骨关节丸、小柴胡汤、大柴汤、复方青黛胶囊(丸)、克银丸、消银片(丸)、消核片等。这些药物所含有的含萜类化合物或含生物碱类或含蒽醌类化合物,均不同程度的具有一定肝毒性,如果使用不当极有可能导致肝损伤[7]。值得注意的是,虽然大多数肝毒性药物导致肝损伤多与长期或过量服用有关,但也有部分是特异质型肝损伤,一般与药物剂量无关,而与个体特异质相关。特异质型是指只对少数特异质机体产生肝毒性,可能很少的剂量就有可能导致肝损伤,而对正常非特异质机体不产生明显的影响。中药药物性肝损害的治疗原则药物性肝损伤(DILI)的治疗原则:包括立即停用有关或可疑药物(治疗关键)、促进致肝损药物清除和应用解毒剂、应用肝细胞保护剂、治疗肝功能衰竭。中药所导致的肝损伤同样遵循这些原则。1.立即停药:一旦确诊或怀疑与用药有关,应立即停用一切可疑的损肝药物,多数病例在停药后能恢复。2.支持治疗:注意休息,对重症患者应绝对卧床休息;补充足量热量、足量的蛋白质、多种维生素等以利肝细胞修复和再生。3.解毒治疗:急性中毒的患者可采取洗胃、导泻、活性炭吸附等措施消除胃肠残留的药物,采用血液透析、腹腔透析、血液灌流、血浆置换等方法快速去除体内的药物。4.药物治疗[8](1)抗自由基损伤药:重型患者可试用硫普罗宁、N-乙酰半胱氨酸(NAC)等抗自由基损伤药物。推荐使用NAC,可清除多种自由基,临床越早应用效果越好,成人一般用法:50-150mg/kg/d,总疗程不低于3天,治疗过程中应严格控制给药速度,以防不良反应。(2)抗炎保肝药:异甘草酸镁可较好地降ALT,可用于治疗ALT明显升高的急性肝细胞型或混合型药物性肝损伤;经验表明,轻-中度肝细胞损伤型或混合型药物性肝损伤,炎症重者可试用双环醇和甘草酸制剂,炎症轻者可试用水飞蓟素。(3)促进胆红素及胆汁酸代谢药:胆汁淤积型药物性肝损伤,可选用具有促进胆红素及胆汁酸代谢的S-腺苷蛋氨酸、熊去氧胆酸等。5. 对出现肝性脑病和严重凝血功能障碍的急性肝损伤,以及失代偿性肝硬化者,可考虑肝移植[8]。
杨晴 主任医师 珠海市人民医院医疗集团 肝病科1675人已读 - 引用 慢性乙型肝炎临床治愈(功能性治愈)专家共识
本共识为规范慢性乙型肝炎(慢乙肝)临床治愈(或功能性治愈)的治疗策略和技术原则而制订。本共识旨在帮助临床医生在提高慢乙肝临床治愈的抗病毒治疗中做出合理决策。本共识制订的循证医学证据主要来源于慢乙肝核苷类药物经治患者或核苷类药物先行治疗患者。本共识中的证据等级分为A、B和C三个等级,推荐等级分为1和2两个级别(表1,根据GRADE分级修订)。随着HBV疫苗联合乙型肝炎免疫球蛋白的母婴阻断措施的普及和强效抗病毒药物的应用,HBV感染的防治取得了长足的进步,然而慢性HBV感染仍是全球重大公共卫生问题。全世界约有2.4亿慢性HBV感染者,每年约超过65万人死于HBV相关终末期肝病,包括肝功能衰竭、肝硬化和肝细胞癌(HCC)。慢乙肝的治疗目标是延缓或减少肝硬化失代偿、肝功能衰竭和HCC的发生,从而改善患者生活质量和延长生存时间。HBsAg阴转与肝脏功能改善、组织病理改善以及长期预后改善相关,是目前国内外最新慢乙肝防治指南推荐的理想治疗目标,即功能性治愈或称为临床治愈。然而直接抗病毒药物(DAA)[如核苷(酸)类似物(NA)]或免疫调节剂[如聚乙二醇化干扰素α(PEG-IFN)]单独使用实现临床治愈的作用有限。理论上,NA和PEG-IFN针对HBV发挥不同的抗病毒作用机制,合理联用能够产生协同和互补的效应。临床实践证明,以NA和PEG-IFN序贯或联合治疗的优化方案针对部分优势人群显示出良好的疗效,并积累了诸多成功实现HBsAg阴转的案例和经验,开展了系列随机对照临床研究。本共识阐述了联合治疗方案的最新循证医学依据,总结了慢乙肝临床治愈路线图的专家共识,指导临床医师治疗决策的制订,以帮助慢乙肝患者实现临床治愈。1 HBV感染的临床转归和临床治愈1.1 HBV感染的临床转归作为一种独特的嗜肝DNA病毒,HBV感染人体后通过肝细胞膜上受体,如钠离子-牛磺酸-协同转运蛋白(NTCP)侵入肝细胞内,其基因组部分双链的松弛环状DNA(rcDNA)进入细胞核并形成病毒复制的模板——共价闭合环状DNA(cccDNA),HBV cccDNA与宿主组蛋白和非组蛋白结合形成病毒微染色体,具有高度稳定性,cccDNA半衰期较长,无需新的病毒进入肝细胞即可自我补充,保持一定数量的转录模板。此外,HBV基因组在宿主细胞酶的作用下,病毒双链线性DNA还可整合至宿主DNA中,整合的病毒基因组片段缺少核心蛋白的启动子和增强子,无法成为病毒复制的模板,但因其含有HBsAg的启动子区域,可持续表达HBsAg,是HBeAg阴性患者HBsAg的主要来源。HBV独特复杂的基因组和复制模式使得病毒难以从体内彻底清除。HBV感染人体后可导致不同的临床结局,包括急性自限性感染和慢性HBV感染,后者还可分为慢性/非活动性HBV携带者、HBeAg阳性/阴性慢乙肝、隐匿性肝炎、乙型肝炎肝硬化等状态。90%的围生期感染和25%~30%的婴幼儿感染发展为慢性感染;而5岁以后感染者绝大多数可自发清除HBV,仅有5%~10%发展为慢性感染。HBV感染的临床转归和疾病进程主要取决于病毒复制和宿主免疫应答之间的相互作用。HBV急性感染后,机体通过产生有效的抗病毒免疫应答,包括天然免疫和适应性免疫应答,在清除病毒、控制疾病进程中发挥重要作用。急性自限性感染是理想的HBV感染的自然转归,一般无需抗病毒治疗,患者多在感染后半年内发生HBsAg阴转,多数伴有HBsAg血清学转换,尽管不代表体内HBV被彻底清除,但患者长期预后良好。与急性自限性感染相比,慢性HBV感染时,HBV持续复制介导了淋巴细胞亚群功能失衡及紊乱,HBV特异性T细胞和B细胞应答的特异性和强度显著降低、功能耗竭,从而不能有效发挥抗病毒作用,最终导致免疫耐受状态和感染慢性化。1.2 慢乙肝的临床治愈大多数慢乙肝患者通过抗病毒治疗可获得生化学应答和病毒学应答,即ALT复常、HBV DNA持续低于检测值下限(基本的治疗终点),部分患者可获得HBeAg阴转和(或)血清学转换并达到可靠的停药终点(满意的治疗终点),最终获得肝组织学改善并降低肝硬化和HCC的发生风险。随着治疗个体化方案不断优化和追求的目标不断推进,以及现阶段高效、安全的慢性丙型肝炎治愈性抗病毒治疗的成功,为探索慢乙肝的治愈策略增强了信心。慢乙肝治愈的类型主要包括完全治愈(又称为病毒学治愈)和临床治愈(又称为功能性治愈或免疫学治愈)。完全治愈即血清HBsAg检测不到,肝内和血清HBV DNA清除(包括肝内cccDNA和整合HBV DNA),血清抗-HBc持续阳性,伴或不伴抗-HBs出现。由于cccDNA持续稳定存在,且目前缺乏针对cccDNA的特异性靶向药物,因此完全治愈难以实现。临床治愈即完成有限疗程治疗后,血清HBsAg和HBV DNA持续检测不到,HBeAg阴转,伴或不伴HBsAg血清学转换,残留cccDNA可持续存在,肝脏炎症缓解和肝组织病理学改善,终末期肝病发生率显著降低。临床治愈类似于急性HBV感染后自发性病毒清除的状态,标志着慢乙肝的持久免疫学控制,是目前国内外指南推荐的理想治疗目标。然而HBsAg阴转发生的年龄≥50岁是HBsAg转阴患者HCC发生的危险因素之一。因此对于适合的优势人群应尽可能追求早期临床治愈。与完全治愈不同,临床治愈可在优势慢乙肝人群中通过优化治疗方案实现。1.3 现有抗病毒药物实现临床治愈的局限性目前批准的慢乙肝抗病毒药物包括免疫调节剂(如PEG-IFN)以及直接作用于病毒复制周期不同靶点的DAA(如NA)。有限疗程的PEG-IFN或长期NA治疗可获得持续生化学和病毒学应答,肝脏组织学改善,显著降低但无法彻底消除HCC发生风险。然而单独应用PEG-IFN或DAA均难以实现HBsAg清除。NA使用方便且耐受性良好,目前约有80%以上的接受抗病毒治疗的患者应用NA治疗。作为逆转录酶抑制剂,NA可强效抑制HBV复制,然而即使是恩替卡韦(ETV)、富马酸替诺福韦酯(TDF)或替诺福韦艾拉酚胺(TAF)等一线NA,均不能直接抑制cccDNA的转录活性,从而无法有效抑制病毒蛋白如HBsAg的表达。尽管长期NA治疗cccDNA和HBsAg水平逐渐下降,但HBsAg阴转率仅0~3%,且NA治疗难以获得持久的免疫学控制,停药后复发率高,因此绝大多数患者需要长期甚至终身服用。如何进一步提高NA经治患者的治疗疗效并尽可能实现临床治愈是临床亟待解决的热点和难点问题。干扰素通过增强免疫细胞功能和促进细胞因子的表达、诱导干扰素刺激基因(ISGs)的产生并经干扰素信号通路编码多种抗病毒蛋白等环节作用于HBV复制、转录等重要生物学过程,从而发挥免疫调节和抗病毒的双重作用。此外,干扰素可通过增强HBV前基因组RNA(pgRNA)和核心颗粒的降解,或通过对cccDNA的表观遗传修饰来抑制HBV转录并减少病毒蛋白如HBsAg的表达。与NA相比,干扰素疗程有限,血清学应答较高且应答更持久,但干扰素单独使用仅在部分患者中有效,且耐受性相对较差。干扰素治疗优势人群的特点包括相对年轻(包括青少年)、A或B基因型、基线高ALT水平[2~10倍正常值上限]、低HBV DNA滴度、低HBsAg水平等。PEG-IFN单药治疗HBsAg阴转率为3%~7%,稍高于NA治疗。上述慢乙肝优势人群在无干扰素使用禁忌证的情况下建议优先考虑PEG-IFN治疗,治疗原则请参见相关干扰素治疗指南。现阶段因缺乏可清除HBV cccDNA和整合的HBV DNA的药物,只有打破免疫耐受状态使机体产生有效的固有和适应性抗病毒免疫应答,才能真正达到完全控制病毒复制甚至实现临床治愈的目的。单独应用NA或PEG-IFN对宿主免疫的影响不同,且对免疫应答的恢复作用有限。PEG-IFN主要激活天然免疫应答,如增强CD56bright自然杀伤(NK)细胞的抗病毒活性,但可能导致效应性CD8+T细胞功能消耗,对HBV特异性CD8+T细胞功能的恢复作用有限。NA单独应用不能修复NK细胞的抗病毒活性,但对于ALT升高的患者,替比夫定(LdT)能一定程度上恢复CD56bright NK细胞的功能。经过NA长期治疗获得病毒学应答的患者,受损的HBV特异性CD8+T细胞功能部分恢复提示病毒载量和HBsAg下降可能有助于HBV特异性CD8+T细胞的功能重建。此外,NA抑制HBV复制,可以直接增强PEG-IFN诱导的天然免疫激活效应,上述免疫学发现为两类药物合理联用可能发挥相加或协同效应提供了理论依据。研究表明对于获得HBsAg清除的患者,阿德福韦酯(ADV)和PEG-IFN联合治疗可促进HBV特异性T细胞功能部分恢复。ETV和PEG-IFN序贯治疗诱导的血清学应答与治疗早期固有和适应性免疫细胞的功能修复以及ISGs的表达变化密切相关,PEG-IFN序贯治疗激活CD56brightNK细胞的功能,后者通过直接和间接途径促进HBsAg和cccDNA的清除。总而言之,诸多数据证实了联合治疗在恢复宿主抗病毒免疫应答和清除病毒方面的优势。推荐意见(1)作为慢乙肝抗病毒治疗理想的终点,临床治愈即完成有限疗程治疗后,血清HBsAg和HBV DNA持续检测不到、HBeAg阴转、伴或不伴HBsAg血清学转换,残留cccDNA可持续存在,肝脏生化学和组织病理学改善,终末期肝病发生率显著降低。(A1级)(2)慢乙肝临床治愈可以通过恢复宿主固有和适应性免疫应答从而持久控制HBsAg的产生而实现。(A1级)(3)NA和PEG-IFN对固有和适应性免疫影响不同,且NA强效抑制病毒复制可协助PEG-IFN的免疫调节作用,为两类药物合理联用提供了理论依据。(A1级)2 慢乙肝的临床治愈策略及路线图DAA(如NA)和免疫调节剂(PEG-IFN)两类药物的联合治疗通过整合强效抑制病毒和恢复宿主免疫应答的效应,是现阶段最可能实现临床治愈的有前景的治疗策略。临床实践中,NA和PEG-IFN联合治疗方案积累了诸多成功实现HBsAg阴转以及NA安全停药的案例和经验。十余年来,国内外肝病学者就联合策略陆续进行了大量的探索,尤其是中国学者针对NA和PEG-IFN联合个体化治疗策略不断进行优化,在选择何种药物联用、如何进行联用等方面开展了多项多中心随机对照临床研究。目前NA和PEG-IFN联合治疗方式主要包括初始联合治疗策略和序贯联合治疗策略,后者包括“换用”策略(即NA换用PEG-IFN)和“加用”策略(即NA加用PEG-IFN)。2.1 NA和PEG-IFN初始联合治疗策略早期评估初始联合治疗策略的相关研究重点探索如何提高病毒学应答或HBeAg血清学应答,未采用HBsAg阴转作为治疗疗效终点。LAM(或ADV)和PEG-IFNα-2a初始联合治疗的相关研究表明,较PEG-IFNα-2a单药相比,初始联合治疗策略治疗过程中病毒学应答率更高,但未能提高停药后的持续应答率。一项提前终止的研究评估了HBeAg阳性初治患者接受LdT和PEG-IFNα-2a联合治疗的疗效和安全性,与PEG-IFNα-2a单药相比,联合治疗能显著降低病毒载量和血清HBsAg水平,然而意外增加了严重周围神经病变的风险,因而这两种药物应避免同时联用。一项随机对照研究纳入HBeAg阴性初治患者,与PEG-IFNα-2b单药相比,ETV和PEG-IFNα-2b联合治疗病毒学应答率更高,然而HBsAg阴转率两组间差异无统计学意义(9.5% vs 4.8%)。新近一项随机对照试验纳入HBeAg阳性和阴性初治患者,结果显示与TDF或PEG-IFNα-2a单药治疗以及TDF联合PEG-IFNα-2a治疗16周相比,TDF联合PEG-IFNα-2a治疗48周可显著提高HBsAg下降幅度及停药后24周HBsAg阴转率(9.1%),尤其对于基因A型的患者。继续随访至120周,10.4%接受48周联合治疗的患者实现HBsAg阴转。另一项小样本研究纳入26例基因C型慢乙肝患者,ETV和PEG-IFNα-2a或-2b联合治疗48周后,HBsAg阴转的5年累积率达15%。上述研究提示NA(TDF除外)和PEG-IFN初始联合治疗HBsAg阴转率与单用PEG-IFN相当,针对干扰素使用优势人群可考虑初始单用PEG-IFN,如何提高非优势人群的临床治愈率需进一步探索,其中联合治疗的给药时机可能是影响治疗疗效的关键因素之一。2.2 “换用”治疗策略近年来,多项研究显示对于长期接受NA治疗获得病毒学应答的患者,换用PEG-IFN可实现持续HBsAg阴转并有助于NA安全停药。一项小样本单臂研究纳入既往IFN治疗无应答患者,LAM和IFNα序贯治疗可实现持续病毒学应答和HBsAg血清学转换(3/14)。OSST研究表明,ETV经治获得持续病毒学应答且HBeAg水平较低(<100 PEIU/ml)的HBeAg阳性患者,与ETV单药治疗相比,换用PEG-IFNα-2a治疗48周可显著提高HBeAg血清学转换率和HBsAg阴转率(8.5%)。OSST研究随访1年的数据显示,HBeAg血清学转换率由治疗结束时17.7%增加到停药后1年的38.7%,且85.7%治疗结束前发生HBsAg阴转的患者维持该应答。上述数据和新近多项临床研究结果均为长期NA治疗序贯PEG-IFN可促进HBsAg水平下降和清除提供了直接循证学依据。换用时机可能是决定序贯治疗策略疗效的关键因素之一。一项随机对照研究表明,HBeAg阳性初治患者接受ETV治疗21周后序贯PEG-IFNα-2a治疗48周,与PEG-IFN单药治疗相比在停药后持续应答上未显示出明显优势。NEW SWITCH研究探索了干扰素“换用”策略的最佳时机及治疗疗程,研究表明针对NA经治获得HBeAg阴转的患者,延长序贯PEG-IFNα-2a治疗疗程至96周较48周治疗疗程并未显著提高HBsAg阴转率(14.4% vs 20.7%)。一项前瞻性研究纳入41例HBeAg阳性经ETV治疗后获得HBeAg血清学转换的患者,序贯PEG-IFNα-2a治疗48周,停药后24周6例(15%)患者实现HBsAg阴转。Endeavor研究随机纳入接受长期ETV治疗并获得HBeAg阴转的患者,与换用IFNα-2b单药或继续ETV单药治疗相比,IFNα-2b、重组人白细胞介素-2和治疗性疫苗的序贯联合治疗HBsAg阴转率更高(9.38%)。2.3 “加用”治疗策略“加用”治疗策略即在NA实现持续病毒学应答后加用PEG-IFN,该策略与继续NA单药治疗相比在HBsAg下降或清除方面显示出更好的疗效。一项观察性研究结果表明,12例接受NA治疗的患者加用PEG-IFNα-2a后,2例患者发生HBsAg血清学转换。一项前瞻性研究纳入10例经长期NA治疗获得HBV DNA持续抑制的HBeAg阴性患者,加用PEG-IFNα-2a后6例患者实现HBsAg阴转及NA安全停药。PEGON研究表明,ETV或TDF经治HBeAg阳性患者,加用PEG-IFNα-2b联合治疗48周后,与NA单药治疗相比HBeAg血清学转换率无显著提高。一项回顾性配对研究显示,长期接受ETV治疗未实现HBeAg血清学转换的HBeAg阳性患者,与ETV单药治疗相比,加用PEG-IFNα-2a治疗可显著提高HBeAg血清学转换率(44% vs 65%)和HBsAg阴转率(0 vs 4%)。且基线HBsAg低水平(<1000 IU/ml)和12周HBsAg下降>0.5 log10 IU/ml能预测最有可能实现HBsAg阴转的患者。HERMES研究表明,NA经治基因D型HBeAg阴性的慢乙肝患者,加用PEG-IFNα-2a可显著降低其HBsAg水平。PEGAN研究结果则显示,使用NA治疗并获得病毒学应答的HBeAg阴性患者,加用PEG-IFNα-2a治疗48周,96周时HBsAg阴转率与继续NA单药治疗相比差异无统计学意义(7.8% vs 3.2%),但HBsAg水平下降更显著。ARES研究表明针对HBeAg阳性患者,NA治疗第24周开始加用PEG-IFNα-2a至48周,较NA单药治疗相比,HBeAg血清学应答率显著提高,且HBV DNA和HBsAg水平下降更明显。新近一项随机对照研究纳入HBeAg阳性初治患者,接受TDF治疗12周后加用PEG-IFNα2b治疗24周,该方案较TDF单药治疗HBsAg阴转率更高(7.5% vs 1.9%)。另一项小样本随机对照研究则纳入长期接受TDF治疗的HBeAg阳性患者,20%加用PEG-IFNα-2a的患者实现HBsAg阴转,而继续TDF单药治疗的患者无1例出现HBsAg阴转。2.4 联合治疗的最佳策略近期一项荟萃分析纳入了24项涉及NA和干扰素联合治疗的临床研究,结果表明序贯联合策略与初始联合策略相比在治疗48周或52周时能实现更高的HBsAg阴转率(11% vs 8%)。此外序贯联合策略中,“换用”策略第48周或第52周的HBsAg阴转率(14%)显著高于“加用”策略(8%)。一项回顾性研究纳入ETV经治HBeAg阴性患者,结果表明无论是“换用”PEG-IFNα-2a治疗(9%)还是“加用”治疗(15%),其HBsAg阴转率均显著高于ETV单药治疗(0)。72周时“换用”、“加用”和ETV单药治疗组的应答率(HBsAg水平下降>1 log10 IU/ml)分别为60%、40%和2%。另一项针对NA经治获得病毒学应答的HBeAg阴性患者的非随机研究显示,80.0%(8/10)换用PEG-IFNα-2a的患者和18.2%(2/11)加用PEG-IFNα-2a的患者HBsAg水平下降>1 log10 IU/ml,表明“换用”策略较“加用”策略更可能促进HBsAg水平降低。研究者推测由于“换用”策略中,停用NA可能通过激活宿主免疫应答从而有助于提高PEG-IFN的疗效。一项正在进行的随机对照研究(SWAP研究)纳入接受长期NA治疗的患者,中期分析数据表明,加用PEG-IFN组(9.0%)和换用PEG-IFN组(8.9%)的HBsAg阴转率均高于NA单药治疗对照组(0),而换用组的病毒学复发率(30.2%)显著高于对照组(3.3%)和加用组(2.0%)。根据现有的相关研究难以明确最佳的联合治疗策略,由于NA抑制HBV复制可直接增强PEG-IFN介导的天然免疫激活效应, NA只有经长期治疗才能获得持续病毒学抑制并降低HBsAg水平,从而部分恢复HBV特异性T细胞功能,可以推测:药物选择(强效NA联合PEG-IFN)、给药时机(NA先行治疗后序贯PEG-IFN)以及患者筛选(持续病毒学抑制及低抗原血症)是影响联合治疗疗效的关键因素。2.5 慢乙肝临床治愈路线图基线及治疗早期HBsAg定量或HBsAg快速下降可作为预测干扰素序贯联合治疗HBsAg阴转和制订个体化治疗决策的重要标志物。OSST研究和NEW SWITCH研究分层分析结果表明,长期NA治疗序贯PEG-IFNα-2a时,基线HBeAg阴转且HBsAg<1500 IU/ml的患者治疗48周时HBsAg阴转率较高(22.2%~26.5%),而HBsAg≥1500 IU/ml的患者HBsAg阴转率较低(1.6%~3.8%)。此外,治疗第12周或24周时HBsAg<200 IU/ml的患者最有可能获得HBsAg阴转(48.9%~77.8%)。相反,第12周时HBsAg≥1500 IU/ml或24周时HBsAg≥200 IU/ml的患者难以实现HBsAg阴转(0~1.7%),因此建议这群患者停用PEG-IFN治疗。与上述结果一致,新近一项研究采用换用PEG-IFN治疗作为NA停药策略,结果同样表明20%基线HBsAg<1500 IU/ml的患者可实现HBsAg清除,而基线HBsAg<500 IU/ml是预测HBsAg阴转的最佳指标(HBsAg阴转率达50%)。据此本共识提出DAA(如ETV/TDF)序贯联合免疫调节剂(如PEG-IFN)治疗过程中基于HBsAg动态变化的慢乙肝临床治愈路线图,其中整合了基线特征指导治疗(BGT)和应答指导治疗(RGT)策略(图1)。基于该路线图,基线HBsAg低水平且HBeAg阴性的优势患者接受序贯PEG-IFN治疗更有可能实现临床治愈,该理论被多项研究进一步证实。Endeavor研究显示基线HBsAg水平<1500 IU/ml的患者HBsAg阴转率高达27.3%。目前正在开展的多项研究针对优势人群采用序贯联合治疗进一步证实了BGT策略的有效性。一项随机对照研究纳入NA经治获得病毒学应答且HBsAg<2000 IU/ml的患者,换用PEG-IFNα-2b治疗60周促进治疗结束时HBsAg阴转(32.6%)和HBsAg血清学转换(27.9%)。Anchor研究则随机纳入NA经治低HBsAg水平(<3000 IU/ml)的患者,与ETV单药治疗(HBsAg阴转率或转换率为0)相比,序贯联合96周PEG-IFNα-2b加或不加粒细胞-巨噬细胞集落刺激因子能显著提高HBsAg阴转率(21.21%~27.78%)和HBsAg血清学转换率(19.44%~21.21%)。ICURE研究纳入NA经治低HBsAg水平(<1000 IU/ml)且HBeAg阴性患者,接受序贯联合PEG-IFNα-2b治疗后,66.67%的患者实现了临床治愈。治疗结束后,80%的患者在停药随访第24周仍维持应答。为验证RGT策略,近期PYRAMID研究纳入NA经治后获得病毒学应答HBsAg<5000 IU/ml且HBeAg<100 PEIU/ml的HBeAg阳性患者,第24周时HBsAg<200 IU/ml的患者,56.5%于第72周时实现HBsAg阴转;若第24周时HBsAg≥200 IU/ml者,继续联合治疗组仅4.5%的患者获得HBsAg阴转;而第24周时停用PEG-IFN的患者均未能实现HBsAg阴转。上述数据证实,基于24周时HBsAg<200 IU/ml的RGT策略可以帮助预测能继续使用联合治疗并可能获益的患者。此外,NA经治患者联合PEG-IFN治疗后12周或者24周HBsAg下降的幅度同样可能是预测48周或72周的有效指标。Anchor研究中期数据显示,序贯联合PEG-IFNα-2b治疗12周和24周HBsAg下降≥1 log10 IU/ml,80.00%和62.50%的患者治疗72周时可实现HBsAg阴转,反之,仅8.43%和3.03%的患者可获得HBsAg阴转。大样本多中心真实世界COST临床研究也将为路线图的验证提供有力的循证医学证据。推荐意见(4)联合治疗药物选择包括DAA(如强效NA、ETV和TDF等)和免疫调节剂(如PEG-IFN)。(A1级)(5)对于接受NA治疗后HBV DNA检测不到,尤其是HBeAg阴转且HBsAg水平低(<3000 IU/ml)的患者,“加用”或“换用”PEG-IFN的序贯联合治疗策略可以提高临床治愈率。“换用”策略可能出现病毒学复发,应注意随访和监测。(A1级)(6)整合基于HBsAg动态变化的BGT和RGT策略的路线图可用于指导DAA(如强效NA)序贯联合免疫调节剂(如PEG-IFN)的治疗决策。(A1级)(7)DAA(如强效NA)序贯联合免疫调节剂(如PEG-IFN)治疗,基线低HBsAg水平(<1500 IU/ml)且HBeAg阴转,或治疗早期(12或24周)HBsAg<200 IU/ml或HBsAg下降>1 log10IU/ml可预测最有可能获得HBsAg阴转的患者。(A1级)(8)治疗24周时HBsAg ≥ 200 IU/ml的患者获得HBsAg阴转的可能性小,应考虑停用PEG-IFN,或选用其他治疗药物(如NA)。(A1级)3 慢乙肝临床治愈的监测和长期随访在实现临床治愈的治疗过程中应定期和长期随访。肝活体组织病理学检查(肝活检)由于有创性和风险性而难以普及,临床实践中定量监测肝内cccDNA和总HBV DNA水平仍是重大挑战。为了更好地评估患者接受抗病毒治疗后是否获得临床治愈,需要探索新的无创替代标志物。3.1 预测指标和定期监测血清HBsAg水平一定程度上反映cccDNA转录以及mRNA翻译活性。基线和治疗早期HBsAg低水平或显著下降是预测HBeAg血清学转换后HBsAg阴转的有效标志物,可帮助识别干扰素治疗的优势人群。即使是基线HBsAg<1000 IU/ml的非活动性携带者,接受96周PEG-IFNα-2a单药或联合ADV治疗后,44.7%的患者可获得HBsAg阴转。对于初始使用PEG-IFNα-2a的患者,治疗24周时是否获得HBsAg<1500 IU/ml且HBV DNA <105拷贝/ml的应答可以指导后续治疗,并提高临床获益。而对于NA经治患者,基线HBsAg<1500 IU/ml、治疗12周/24周HBsAg<200 IU/ml的患者序贯PEG-IFN治疗实现HBsAg阴转的可能性大。此外,NA治疗结束时HBsAg水平可预测停药后持续应答率并识别停药后可能获得HBsAg阴转的患者。除外HBsAg定量,一项大型队列研究表明,HBeAg血清学清除后ALT持续复常的患者在其后20年内HBsAg阴转率较高(70.3%)。基线抗-HBc抗体水平是预测HBeAg阳性患者NA或PEG-IFN抗病毒治疗疗效的新型生物学标志物。对于HBeAg阴性的慢乙肝初治患者,抗-HBc定量水平可预测HBV DNA阴转及HBsAg清除。由HBV核心抗原(HBcAg)、HBeAg和相对分子质量22×103前核心蛋白组成的HBV核心相关抗原(HBcrAg),与肝内cccDNA水平具有良好的相关性。HBcrAg水平联合HBsAg定量可帮助预测NA停药后的复发风险。血清HBV RNA是反映肝内cccDNA转录活性的良好生物学标志物,可早期预测抗病毒治疗期间HBeAg血清学转换以及停药后病毒学复发和HBsAg逆转。在应用PEG-IFN单药或联合治疗前,需评估疗效和安全性相关重要指标,包括HBsAg、HBeAg和HBV DNA水平、血常规、生化学指标、肝脏超声和瞬时弹性成像、甲状腺功能、精神状态、自身免疫抗体、眼底检查以及其他常规检测,排除糖尿病、高血压等其他基础疾病,对于制订合适的治疗决策和预测治疗疗效至关重要。此外,PEG-IFN治疗过程中也应定期监测上述指标,以评估不良事件的严重程度以及治疗疗效。3.2 长期随访对于实现HBsAg阴转或血清学转换的患者,治疗结束后第1年每3个月随访1次,第2年每6个月随访,此后若没有HBsAg逆转的患者可延长至每年随访1次。如果在随访期间出现病毒学或临床复发,综合评估后可考虑再治疗。近期一项研究表明干扰素停药后52周内HBsAg仍有发生逆转的风险,建议在此期间仍应密切监测HBsAg定量。一旦失去对HBV感染的免疫学控制,即便是获得HBsAg阴转的患者仍有可能发生HBsAg和HBV DNA逆转。因此,HBsAg阴转患者除外监测HBsAg,每年还应监测HBV DNA和ALT定量水平。大量研究表明,尽管HBsAg阴转能显著降低HCC和肝脏疾病的发生风险,但仍有一部分获得HBsAg阴转的慢乙肝患者会进展为HCC。对于已确诊肝硬化、HBsAg清除时年龄大于50岁、男性或有HCC家族史的慢乙肝患者应密切监测HCC发生风险。对于已实现HBsAg阴转的进展期肝纤维化或肝硬化患者,应每间隔3~6个月通过甲胎蛋白、肝脏超声、必要时CT或MRI等辅助检查监测HCC发生风险,对于基础合并食管静脉曲张的患者,则应定期行内镜检查对食管静脉曲张进行长期监测。若存在其他肝脏疾病的风险因素,如饮酒、肥胖和(或)2型糖尿病、非酒精性脂肪性肝病(NAFLD)或非酒精性脂肪性肝炎(NASH)的慢乙肝患者则需要进行更全面的评估。最近一项研究显示,接受抗病毒治疗并获得完全病毒学抑制的患者HCC以及肝脏事件发生风险更低,在此基础上获得HBsAg阴转可进一步减少HCC发生风险,但并未降低肝脏事件发生风险以及肝脏相关死亡率,提示肝脏炎症和损伤可能是发生肝脏事件的主要驱动因素。此外,有无肝硬化仍是患者发生肝脏事件和肝脏相关死亡的主要危险因素。因此,HBsAg阴转后仍应持续监测HBV DNA和ALT水平。中国开展的大样本多中心真实世界OCEAN临床研究将提供远期转归的循证医学数据。HBsAg阴性、抗-HBc阳性的患者接受免疫抑制剂治疗或肿瘤化疗时存在HBV再激活的风险。开始相关治疗之前应当评估患者的ALT、HBV DNA和HBsAg水平,治疗期间和治疗结束后也应密切监测上述指标。推荐意见(9)联合免疫调节剂(如PEG-IFN)治疗之前,需评估包括HBsAg滴度、HBV DNA、HBeAg、血常规、生化学指标、肝脏超声及瞬时弹性成像、甲状腺功能、精神状态、自身免疫抗体、眼底检查等重要基线指标用以指导治疗决策、预测治疗疗效等。治疗期间仍需定期监测上述指标以评估治疗的安全性和有效性。(A1级)(10)即使获得HBsAg阴转,仍需长期监测HBV再激活、HCC以及其他肝脏事件。建议治疗结束后第1年每3个月随访1次,第2年每6个月随访1次,此后若HBsAg持续阴性可延长至每年随访1次。若出现复发,综合评估后可考虑再治疗。(A1级)4 展望清除cccDNA和打破宿主免疫耐受的两大难题是实现慢乙肝治愈的主要障碍。只有持续深度抑制HBV复制,并诱导有效的抗病毒免疫应答,才能彻底控制HBV感染。目前,诸多全新的抗病毒治疗手段,包括针对HBV生命周期不同阶段,如HBV进入(NTCP抑制剂)、HBV cccDNA生成及加工(cccDNA抑制剂)、病毒复制及病毒蛋白表达(衣壳组装调节剂、RNA干扰、核酸聚合物等)的DAA药物,以及恢复或提高宿主抗病毒免疫应答的免疫调节剂等,正在通过动物或细胞模型进行筛选,部分已经进入早期临床试验,这些新的治疗药物将有助于进一步优化和完善现有的慢乙肝临床治愈抗病毒治疗方案,并最终清除cccDNA,实现慢乙肝的完全治愈。5 拟待解决的问题(1)评估免疫学和病毒学生物标志物对治疗起始、临床治愈或治疗失败的预测价值。(2)需大样本研究进一步验证DAA药物(如NA)和免疫调节剂(如PEG-IFN)的序贯/联合治疗路线图。DAA药物(如TAF)与PEG-IFN等免疫调节剂联合使用的疗效及安全性有待进一步研究。(3)评估治疗结束后HBsAg阴转的持续应答率,探索预测停药后持续应答的生物学标志物。(4)开展长期随访研究评估联合治疗实现临床治愈后HCC和肝脏事件的发生风险及相关风险因素。(5)治愈慢乙肝任重道远,迫切需要研发针对HBV生命周期靶点的新型DAA药物或旨在重建机体抗HBV免疫应答的免疫调节剂。
杨晴 主任医师 珠海市人民医院医疗集团 肝病科3000人已读



