云南省第二人民医院呼吸与危重...科普号
- 精选 肺结核治疗多久可以和小孩相处呢?1段语音 共1分钟邢西迁 主任医师 云南大学附属医院 呼吸与危重症医学科2634人已收听
- 精选 孕妇有肺结核会不会传染给胎儿?1段语音 共1分钟邢西迁 主任医师 云南大学附属医院 呼吸与危重症医学科2374人已收听
- 精选 硬质气管镜快速铲除气管肿瘤,迅速缓解呼吸困难
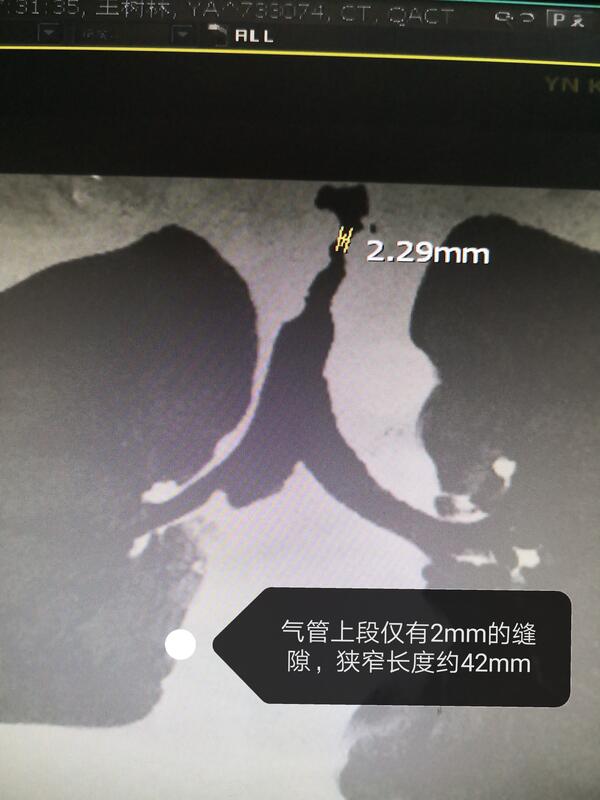
49岁男性,右中下叶肺癌切除术后,出现重度呼吸困难,不能平卧。CT示气管肿瘤长度约4cm,最窄处气管直径仅2mm。以硬质气管镜快速铲除肿瘤,高效率的切除,缩短手术时间,同时硬质气管镜可以压迫止血。术后患者呼吸顺畅。
 邢西迁 主任医师 云南大学附属医院 呼吸与危重症医学科1817人已读
邢西迁 主任医师 云南大学附属医院 呼吸与危重症医学科1817人已读 - 精选 T管置入治疗气管闭锁,患者恢复正常说话能力
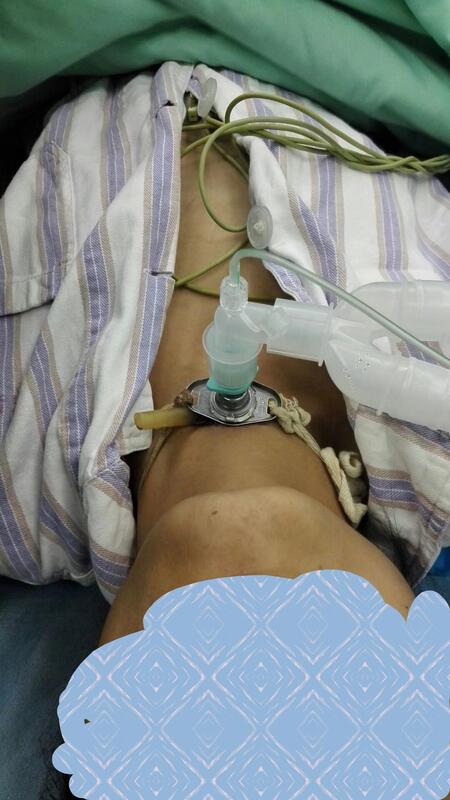
病人年仅25岁,已行气管切开两年,气管上段长约2cm完全瘢痕闭锁,不能言语交流。因气切口偏向气管右侧壁,闭锁的气管上段偏向气管左侧壁,气管上、下段不在同一条线上,故打通气管上段风险较高,易发生气管纵隔瘘、气管食管瘘等。前期经过三次硬质气管镜下介入治疗,联合耳鼻喉科主任,采用内外联合、上下同治的方法,打通并扩张气管上段。今天放置Montgomery T管后,患者终于可以正常说话,生活质量大大提高。期待一年后可以顺利拔除T管。
 邢西迁 主任医师 云南大学附属医院 呼吸与危重症医学科3053人已读
邢西迁 主任医师 云南大学附属医院 呼吸与危重症医学科3053人已读 - 精选 气管Y型金属支架置入治疗双侧主支气管狭窄、闭塞
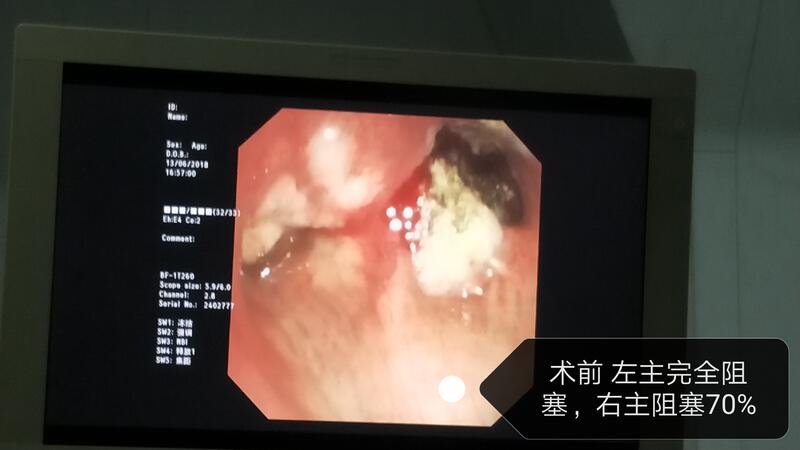
患者左主支气管被肿瘤完全阻塞,右主支气管被肿瘤阻塞约70%,患者重度呼吸困难。先以氩气刀消融左、右主支气管肿瘤,将左主支气管打通,然后置入Y型覆膜金属支架,支架置入后左、右主支气管管腔通畅。患者呼吸困难消失。
 邢西迁 主任医师 云南大学附属医院 呼吸与危重症医学科2084人已读
邢西迁 主任医师 云南大学附属医院 呼吸与危重症医学科2084人已读 - 精选 罕见支气管肿瘤:子宫内膜间质肉瘤支气管内转移
这是我们治疗的一例罕见的支气管肿瘤,世界上第一例报道。患者为43岁女性,3年前曾诊断为子宫肌瘤。最近5个月出现呼吸困难,呼吸困难逐渐加重。胸部CT示右中间支气管阻塞,支气管镜见右中间支气管一息肉样新生物完全阻塞管腔,经支气管镜下高频电刀、氩气刀、冷冻切除等治疗后,患者呼吸困难症状消失,后续行放疗,患者已无症状存活4年多。该病例我们发表在国际呼吸领域的顶尖期刊Thorax上。治疗前,右中间支气管阻塞。治疗后,右中间支气管通畅。支气管镜见右中间支气管被肿瘤完全阻塞。
邢西迁 主任医师 云南大学附属医院 呼吸与危重症医学科1692人已读 - 精选 冷冻技术在肺部疾病诊治中的应用
冷冻治疗技术已经广泛应用于诊断和治疗特定的肺部疾病,尤其是气道腔内良、恶性病变,以硬质支气管镜和(或)可弯曲支气管镜为介入媒介,是一种相对安全、有效及容易掌握的治疗技术。1986年英国学者Maiwand首先报道用冷冻姑息性治疗气管内肿瘤,并取得成功经验。经支气管镜腔内冷冻容易操作,并发症少,费用低,目前CO2冷冻已在国内得到广泛应用。另外,经支气管冷冻肺活检作为一项新技术在临床上开展,可取得较大的活检标本,提高经支气管肺实性病灶活检诊断阳性率。本文目的旨在对冷冻技术在肺部疾病的诊断及治疗方面的新进展作一综述。一、设备及低温生物学1. 设备:冷冻设备包括:操作台,制冷剂和冷冻探头。操作台对冷冻治疗进行监控。一氧化二氮或二氧化碳、液氮作为制冷剂使温度在几秒钟之内分别达到-70℃~-89℃和-196℃。冷冻技术基于焦耳-霍普森效应,压缩的气体高速流出并迅速扩散,进而产生低温促使探头与组织发生黏附。中断气流和降低压力后,继发释放热量并除霜。在此冻-融循环中取出组织。冷冻探头分为刚性、半刚性及软性三种,探头尖端直径分别为1.9mm、2.4mm、5.5mm,总长度为90cm、50~60cm的软性探头和刚性探头。直探头适用于气管、主支气管和下叶病变以及进行经支气管(肺)活检。成角度的探头主要用于上叶病变。硬支气管镜不受低温影响,而可弯曲支气管镜可因工作孔道中形成结晶而受损。2. 低温生物学:冷冻产生的效果包括:细胞损伤和血管损伤。细胞损伤是瞬时的,由冷热交替所致。血管损伤因微循环障碍、血流停滞并继发坏死而产生延迟效应。随温度下降至0℃以下,细胞间隙的水结晶,在0~-20℃温度下发生脱水,进而发生细胞破坏。温度达-20℃细胞内水完全结冰,细胞死亡。解冻时,细胞外张力首先减低,自由水进入受损细胞而使细胞膜破裂[1-2]。冷冻致血管内皮损伤,血管壁通透性增高,血管水肿,血小板聚集,血栓形成,进而循环停滞。小血管解冻后3-4h完全形成血栓,此时组织坏死达高峰[3,4]。由于延迟效应,需要在冷冻治疗后7-10天再次行气管镜检查以清除坏死组织。细胞死亡取决于冷冻时间、解冻时间、所达最低温度、冻融重复次数及组织水含量,冷冻损伤范围通常为5-8mm[5]。含水较高的组织(如皮肤,肉芽组织,黏膜,神经,内皮层,肿瘤组织)易发生冷冻,而软骨、结缔组织、纤维组织、脂肪、神经鞘不易冷冻[6]。二、冷冻技术冷冻可以用来治疗、诊断各种肺部疾病(表1)。表1. 冷冻技术适应症诊断经支气管冷冻活检治疗治疗气道内病变(良性或恶性)冻融疗法冷冻清除疗法(再通)冷冻喷雾术中治疗实质肿瘤经皮实质肿瘤治疗三、冷冻技术诊断肺部疾病经支气管冷冻肺活检可用于诊断肺移植排斥、肺癌及间质性肺病。探头可在荧光镜精确引导下到达距离胸壁大约10-20mm的肺叶,探头冷冻4s后随气管镜同时收回。活检标本在生理盐水中解冻并保存在福尔马林溶液中。Chou等[7]的一项回顾性研究显示冷冻技术可作为气道内肿物诊断及治疗一个很好的手段,且诊断阳性率比传统活检方式高。经支气管镜活检钳活检诊断肺部疾病常受限于标本大小及组织破坏。冷冻肺活检在诊断方面可能优于活检钳活检,其优势在于所取组织标本更大,更多肺泡细胞,以及由于人工挤压少而质量更高[8]。然而,其在不同肺部疾病的有效性及安全性需进一步评估。动物研究显示纤维支气管镜冷冻活检是安全的[9]。1. 肺移植:经支气管镜活检钳肺活检是目前肺移植前评估同种异体移植肺的金标准,但所获取标本质量受机械牵拉及标本大小的限制。因而,建议至少进行10次活检以优化诊断。而每增加一次活检将逐步增加出血及继发气胸的风险。冷冻肺活检因其所取得标本更大及对组织的保护性而成为肺移植患者的优选方案。最近,Yarmus等[10]关于肺移植患者冷冻活检的安全性及诊断效益研究显示,冷冻肺活检安全且取得标本更大。其标本大小及开放肺泡的百分比与活检钳活检相比更有意义(P<0.05)。虽然肺移植患者经支气管活检出血风险较高,但两种活检方法出血风险相当。Fruchter等[11]报道冷冻活检比活检钳活检组织有更大的直径(10mm2 vs 2mm2,P<0.05)以及更多的肺泡组织(64% vs 34%,P<0.05)。较大的标本保留了小血管及终末细支气管,这对于识别肺移植患者的同种异体肺排异反应是必不可少的。同时对于诊断移植肺的慢性功能紊乱及闭塞性细支气管炎也是必要的。清醒镇静下纤维支气管镜或硬质支气管镜进行冷冻活检是安全的[12]。2. 间质性肺疾病:经支气管肺活检在诊断间质性肺疾病(interstitial lung diseases ,ILD)方面起到的作用很小,主要用于排除肉芽肿性疾病及感染。外科肺活检因其所取标本较大而作为诊断ILD的金标准。然而,很多病人因疾病进展而不能承受外科肺活检术。由于冻肺活检比传统活检钳肺活检获得的标本大,可作为诊断ILD的替代手段。在可行性研究中,Babiak等[12]的研究显示41例ILD患者进行冷冻活检时仅有2例发生气胸,诊断阳性率为95.1%(39/41)。这可能是由于冷冻活检提供的组织标本大,两者标本大小分别为15.11mm2 ,5.82 mm2。Pajare等[13]比较了两种活检方法在弥漫性间质性肺疾病的诊断阳性率,结果显示冷冻肺活检有更高的诊断阳性率,且并发症发生率并未升高。3. 肺癌:冷冻活检的另一个重要应用是诊断肺部肿瘤。在诊断中心支气管外生型病变方面,Aktas等[14]的研究报道了冷冻活检有较高诊断阳性率,且未增加并发症的发生。Hetzel等[15]的前瞻性随机双盲多中心试验同样显示,冷冻活检有更高的诊断阳性率,取得更高质量的组织而促进腺癌分子靶点的确定。Schumann等[16]也发现冷冻活检对肺癌有更高的诊断阳性率,而出血风险比传统活检方式小或者两者相当(表2)。四、冷冻技术治疗肺部疾病1. 良性病变:气管支气管的良性病变相对少见[17]。处理这类病变需排除恶性病变,病变致气道阻塞时需要治疗。尽管实性病变需要外科切除,单纯的管内型病变可采用一种或联合内镜下治疗,比如内镜下铲除术,电凝止血,Nd-YAG激光或冷冻切除。Fu等[18]等的研究显示冷冻治疗联合球囊扩张及电凝治疗气管支气管结核所致气管狭窄的有效率达94.6%。2. 非移植相关的管腔内病变:Moorjani等[19]报道的20位各类气道良性病变患者,包括骨化性气管支气管病(4)、结节病(4)、息肉(3)、乳头状瘤(2)、非移植相关肉芽组织(2)、淀粉样变性(1)、脂肪瘤(1),平滑肌瘤(1)、插管后气管狭窄(1)以及血管瘤(1)。经冷冻治疗后,所有的患者均表示至少有1种症状(呼吸困难、咳嗽、喘鸣、咯血、胸痛)得到改善。所有病人的肺功能测定指标均有改善。15位(75%)患者完全移除病变,5位患者因残存的病变需进一步治疗。无大出血或气道撕裂。其他还有冷冻治疗复发性呼吸道乳头状瘤、支气管内脂肪瘤及错构瘤的个案报道[20-22]。3. 肺移植相关气道并发症:肺移植后气道并发症发生率为7%-18%,相关死亡率为2%-4%[23,24]。支气管狭窄是最常见并发症,发生率波动于1.6%~32%,且通常发生继发性坏死,吻合口裂开或感染[25]。球囊扩张是支气管狭窄首选干预措施,但是其效果难以维持,通常需要其他治疗措施,比如冷冻治疗、电烧灼、激光或近距离放射治疗[26]。多达20%的肺移植患者,几个月内发生支气管吻合口处良性肉芽组织增生引起症状性气道阻塞。此种情形可用钳切法、冷冻或Nd-YAG激光处理[27,28]。4. 恶性病变:肺癌是世界致死率第一的癌性疾病[29]。中央气道恶性肿瘤可引起气道阻塞症状,冷冻切除可有效解除中央气道阻塞。支气管内减瘤手术可用冷冻探头(冻融有延迟效应,冻切可快速起效)或冷冻喷雾进行。冻融、冷冻清除(再通)或冷冻喷雾均可用于治疗气道内病灶及管腔内浸润性病变。但不宜用于气道外压性病变。冻融疗法用于肉芽组织或气道内良/恶性病变的治疗。冷冻切除可快速清除肿瘤开通气道,但可能导致出血而需止血治疗(如氩离子凝固术(APC)、稀释肾上腺素灌注或者球囊压迫)。冷冻喷雾疗法可用于破坏气道中多余组织,喷洒液氮范围为2-3cm的椭圆形区域,冷冻深度可达5mm[30]。液氮转化为氮气取代氧气而增加气道中气压,需进行负压抽吸。除了支气管内冷冻治疗,用于肺部恶性病变的冷冻技术包括经皮冷冻治疗和直接胸内冷冻。直接冷冻疗法用于术中不能进行手术的患者。随着影像引导技术及冷冻技术的进展,经皮冷冻手术可作为肺癌早期或晚期的治疗选择[31]。总之,冷冻疗法适用于各阶段肺癌,包括不能手术的晚期患者及有并发症不能手术的早期肺癌患者[32,33-42]。几个经皮冷冻手术联合化疗和放疗的研究结果显示,经皮冷冻手术安全有效且利于提高中位生存期[38,43-46]。五、中央气道阻塞的冷冻疗法冷冻治疗对于气管内肿瘤可起到有效的减瘤作用。因存在延迟效应,不作为严重大气道窄的首选治疗方法。正确应用可缓解症状且安全性极高。唯一的缺点是需要在1-2周后再进行支气管镜下清除坏死组织,对于残留病变肿瘤需要反复治疗[29,38-40]。冷冻疗法也可用于重度气道阻塞患者。从中央气道清除肿瘤组织使气道再通,从而快速改善症状及疾病评分。冻切过程中的出血可用APC等方法处理[41]。冷冻治疗可与其它减瘤技术联合应用,但目前尚无成熟的经验及大样本的研究。六、直接冷冻疗法治疗肺部肿瘤直接胸内冷冻术用于预计可切除但术中未能完全切除病灶的补救治疗[32,47]。这需要精确的定位及测量,评估肿瘤与周边大血管关系。冷冻探头置于肿瘤边缘或与肿瘤的表层接触,持续冷冻直到冰球完全包裹肿瘤且超过正常肺组织边缘5-10mm。推荐进行2个循环的冻融以防止较大的出血。较大肿瘤需要多个冷冻探头同时进行冷冻。坏死组织可机械切除。冷冻手术可作为电视胸腔镜及开胸手术过程中无法进行手术患者的选择。Maiwand等将直接冷冻手术运用于开胸探查的15位患者,术中发现无法切除肿瘤并以直接冷冻手术代替肺切除。最终显示FEV1、FVC、卡氏评分及WHO评分均有提高,术后无并发症,15例患者中有3位肿瘤体积减小[32]。七、经皮冷冻疗法治疗肺部肿瘤因并发症无法进行手术的肺癌患者,可选择局麻下CT引导经皮冷冻消融术。经皮冷冻治疗是指局麻或全麻下经CT引导直接将冷冻探头送达肿瘤部位。基于焦耳-霍普森原理,冷冻探头使用高压氮气和氦气进行冷冻、融化。此过程包括:5分钟的冷冻后缓慢融化使温度升高达20℃并重复1次,随后进行10分钟冻融。由于肺泡中的空气阻断低温传导,重复冻融引起肺泡出血。使用2-3mm的冷冻探头可能会形成2.5-3cm大的冰球,2cm以内的肿瘤常用1个探头进行治疗,大的肿瘤可用多个冷冻探头同时进行治疗。冷冻治疗与其他治疗如激光、APC相比有更大优势。花费少,无着火风险,可以使用高FiO2,因软骨及胶原组织具有耐低温性,气道穿孔风险小[48]。但气胸和血胸是潜在并发症[31,49]。Niu等[31]发表的最大样本的研究显示840例ⅡA-Ⅳ期的非小细胞肺癌患者进行冷冻治疗后体积变大,随后缩小并形成空腔。86例(14.4%)完全缓解,588例(70%)部分缓解;47.2%患者肿瘤复发,其中28.3%为冷冻治疗在病灶周边;冷冻治疗的生存率高于化疗或化疗联合放射治疗,总生存期为5~61个月(平均23个月)。另一个研究显示ⅢA-Ⅳ期的非小细胞肺癌患者经皮冷冻疗法2年生存率为64%[11]。然而并发症发生率较高,如气胸(12%~25.9%),胸腔积液及血胸(分别为16.2%,22.5%)[31,49]。八、冷冻技术在支气管异物取出中的应用异物及分泌物(粘液栓或血凝块)均可以通过冷冻取出。支气管内物体冷冻后与冷冻探头(1.9mm或2.4mm)充分粘合在一起,探头及异物随气管镜一起退出。据异物大小及形状有时可能需要硬质支气管镜。异物吸入通常发生在儿童。吸入的异物包括有机物(粘液、血液、食物)、无机物(牙、针状物)。根据异物的位置、属性及形状,需用不同的工具,如钳子、Fogarty球囊导管、异物篮、磁材或冷冻探头。冷冻探头通过使含水异物结冰并发生粘附随支气管镜取出[50]。党焱等[51]报道了26例气道难取性异物通过冷冻法均成功取出,操作简单,安全有效,费用低。九、冷冻疗法的局限性和并发症1. 局限性:尽管冷冻疗法安全、易于操作,且较其他内窥镜技术价格低,但也有其局限性。从设备角度来说,一些操作台没有计时器,冷冻时间的控制完全依赖于操作者;因此,治疗程度不标准化。治疗时间过长可能增加并发症发生率。由于冻融治疗的延迟效应,需多次进行支气管镜检查以清除坏死组织,限制了冷冻疗法在重度中央气道狭窄患者的应用且会增加总费用。冷冻治疗用于气道再通时,可发生出血而需要其他措施(如APC)以帮助止血。2. 并发症:冷冻疗法用于诊断及治疗的安全性已得到证实。最常见并发症为出血、气胸、坏死组织阻塞气道导致呼吸衰竭、纵隔气肿、气体栓塞等。另外,气道撕裂是冷冻治疗过于暴力(尤其对于混合性恶性阻塞)的潜在并发症。冷冻雾化治疗期间需要被动通气以避免如心动过速、低血压及气胸等并发症。十、展望作为诊断肺部疾病的一项新技术,冷冻技术有很大的潜在应用范围。已经有研究显示其在诊断移植排斥患者、ILD及肺癌方面与传统钳取术具有可比性。因其比传统钳取术获得更大标本,这类患者以及病情危重而无法外科肺活检的患者可从冷冻活检中获益。尽管大多数操作者冷冻时间为4s,延长冷冻时间有助于取得更大组织。这需要进一步研究以规范不同情况下的冷冻持续时间。
邢西迁 主任医师 云南大学附属医院 呼吸与危重症医学科5731人已读 - 精选 放置6年的气管金属支架取出(云南首例),置入气管硅酮支架
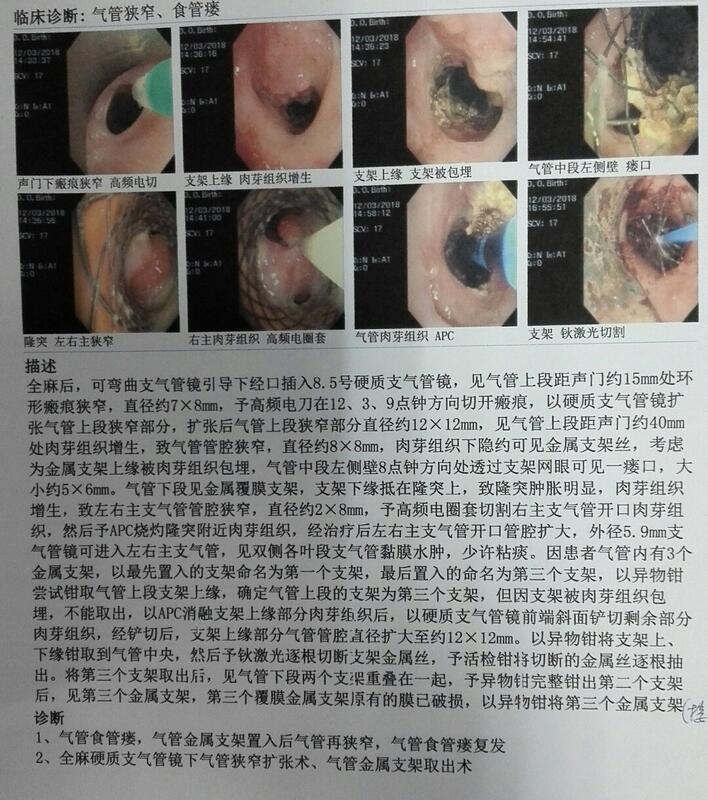
28岁青年男性,6年前因外伤行气管插管发生气管狭窄,行气管切开后发生气管食管瘘,曾放置3个金属支架,最先放置的两个金属支架下移到隆突,导致隆突肿胀、肉芽组织增生,左右主支气管重度狭窄,且隆突几乎被金属支架切割断裂,已经到了不得不取出金属支架的境地。因最后放置的金属支架上缘被肉芽组织严重包裹,不能完整取出,如强行取出易发生气管壁严重撕裂、大出血等,以激光将金属支架丝逐根打断,逐根抽出支架的金属丝。取出金属支架后,患者虽然禁食,但胆汁不断从瘘口流入双下肺,导致双肺化学性损伤严重,呼吸困难严重,放置硅酮支架前患者氧饱和度70%左右。紧急放置放置气管Y型硅酮支架,因Y型硅酮支架最大气管部直径18mm,而气管下段被原金属支架扩张到20多mm,虽不能完全阻塞瘘口,但大部分瘘口被堵住。术后患者呼吸困难症状明显缓解。再放置食管支架封堵瘘口。后续最理想的处理方法是外科把瘘口切掉,但需患者气管狭窄情况稳定。 硅酮支架因组织相容性好,置入气管后不易发生肉芽组织增生,且硅酮支架取出容易。因此,目前良性中央气道狭窄如需置入气管支架,宜首先选择硅酮支架。
 邢西迁 主任医师 云南大学附属医院 呼吸与危重症医学科4183人已读
邢西迁 主任医师 云南大学附属医院 呼吸与危重症医学科4183人已读 - 精选 长期白天干咳怎么办?
白天干咳,夜间不咳,与进食相关,咳嗽多超过8周,最多见于胃食管返流病所致咳嗽,如果伴有烧心、反酸、呃逆等症状就可以考虑服用奥美拉唑,吗丁啉经验性治疗。能做24小时食管PH检测或胃镜检查更好。慢性咳嗽的常见病因还有咳嗽变异性哮喘、上气道咳嗽综合征、嗜酸粒细胞性支气管炎、变应性咳嗽等,确诊后就对症下药了。建议到正规医院呼吸内科就诊。你可以在邓毅书大夫个人网站上看到我提供的这方面的文章,但愿对您的诊治有帮助。
邓毅书 主任医师 云南大学附属医院 呼吸与危重症医学科7448人已读 - 精选 什么是气道高反应性
气道高反应性是气道受到某种刺激而发生缩窄的程度,如果这种刺激在正常人呈无反应状态或反应程度较轻,而在某些人却引起了明显的支气管狭窄,称为气道高反应性(Airway Hyper Reactivity AHR )。气道高反应性表现气道高反应性表现为气道对各种刺激影子出现过强或过早的收缩反应,是哮喘患者发生发展的一个重要因素,可直接反应支气管哮喘严重程度.当气道中以EOS为主的炎性细胞增多时,气道高反应性也随之出现,因而呈现间歇性可逆性的气流受限;指气道对各种刺激因子出现过强或过早的收缩反应。
邓毅书 主任医师 云南大学附属医院 呼吸与危重症医学科1万人已读



